 |
|
Билет 25: Литий-ионные аккумуляторы (принцип действия, электродные материалы, электролиты).
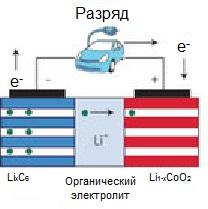 Принцип действия литий-ионных аккумуляторов основан на разделении окислительно-восстановительных реакций в пространстве: на аноде (имеется ввиду процесс разрядки аккумулятора) происходит процесс образования ионов Li+, которые по электролиту переходят к катоду и образуют устойчивое соединение. Реакция образования ионов лития на аноде выгодна из-за энтропийных факторов, поэтому около анода создается двойной электрический слой: отрицательно заряженный электрод и положительно заряженные ионы около поверхности электрода в электролите. В свою очередь за счет образования соединения на катоде создается аналогичный двойной электрический слой. За счет наличия внешней цепи возможно дальнейшее протекание этой реакции: с отрицательно заряженного анода электроны переходят на положительно заряженный катод по внешней цепи, а ионы лития - по электролиту. Литий-ионные аккумуляторы обладают большой удельной емкостью, цикличностью (низкой потерей емкости от цикла к циклу), отсутствует эффект памяти (например, у никель-металлгидридных аккумуляторов он есть), рабочим диапазоном температур −0 … +60 °C(при отрицательных температурах заряд батарей невозможен, разряд возможен до ~-20)
Принцип действия литий-ионных аккумуляторов основан на разделении окислительно-восстановительных реакций в пространстве: на аноде (имеется ввиду процесс разрядки аккумулятора) происходит процесс образования ионов Li+, которые по электролиту переходят к катоду и образуют устойчивое соединение. Реакция образования ионов лития на аноде выгодна из-за энтропийных факторов, поэтому около анода создается двойной электрический слой: отрицательно заряженный электрод и положительно заряженные ионы около поверхности электрода в электролите. В свою очередь за счет образования соединения на катоде создается аналогичный двойной электрический слой. За счет наличия внешней цепи возможно дальнейшее протекание этой реакции: с отрицательно заряженного анода электроны переходят на положительно заряженный катод по внешней цепи, а ионы лития - по электролиту. Литий-ионные аккумуляторы обладают большой удельной емкостью, цикличностью (низкой потерей емкости от цикла к циклу), отсутствует эффект памяти (например, у никель-металлгидридных аккумуляторов он есть), рабочим диапазоном температур −0 … +60 °C(при отрицательных температурах заряд батарей невозможен, разряд возможен до ~-20)
Литий-ионный аккумулятор должен содержать следующие элементы: катод,анод и электролит. От анода и катода требуется, чтобы реакции, происходящие при разрядке аккумулятора были обратимые. Обычно катодные материалы наносятся на медную или никелевую фольгу.
Аноды:
В качестве анодного материала изначально применялся металлическиой литий,
который оказался непригоден из-за низкой циклической устойчивости и опасности в эксплуатации
Сейчас наиболее широко используется графит:
LiC6->C6+Li+ - удельная емкость 372 мА*ч/г
кремниевые аноды - удельная емкость от 2000 до 3500 (литий внедряется в аморфный кремний) - менее распространены из-за плохой цикличности
Катоды:
В качестве катодных материалов применяются:
LiCoO2->0,5Li++Li0,5CoO2
LiMn2O4
LiFePO4
(так же Li3V2(PO4)3 и LiFe2(SO4)3) - все катодные реакции сопровождаются окислительно-восстановительными процессами в металлах (Co2+->Co3+ и т.д.)
Электролиты:
Электролиты в литий-ионных аккумуляторах должны обладать следующими свойствами: во-первых, они не должны реагировать с электродными материалами, с ионами лития и с металлическим литием; они должны быть хорошими ионными проводниками и в то же время не проводить электроны, т.е. быть диэлектриками. Так же электролит должен содержать ионы носителя заряда, то есть лития (чаще всего - раствор соли) Возможно использование жидких и твердых электролитов. Наиболее широко используются жидкие, т.к. они позволяют решить проблемы с изменением объема электрода при зарядке-разрядке.
Ввиду этих требований обычно электролит представляет из себя раствор литиевой соли в органическом растворителе.
Обычно используются LiClO4, LiBF4, LiPF6. В качестве органического растворителя - пропилен-, этилен-, диметил-, диэтил-карбонат. Для понижения вязкости (чем больше вязкость - тем меньше ионная проводимость) могут добавляться различные вещества, например диметоксиэтан.