 |
|
Эксперементальная часть.
4.1. Схема количественного анализа
 Навеска
Навеска

 Раствор
Раствор
| Аликвотная часть Гравиметрическое определение | Аликвотная часть Титриметрическое определение |


| Расчет содержания | Расчет содержания |
4.2. Расчет и результаты взвешивания навески образца
Для гравиметрического определения меди была взята навеска 0,2 г.
Для титриметрического определения кобальта была взята навеска 0,2 г.
4.3. Методика разложения и растворения образца
Точную навеску сплава перенесли в химический стакан, добавили 100 мл HCl (конц.) , закрыли часовым стеклом и нагревали на плитке до полного растворения навески.
4.4. Методика гравиметрического определения меди
Был выбран метод гравиметрического определения меди с помощью органического осадителя 8 – оксихинолина. Этот метод достаточно прост и наиболее селективен, не опасен и в большей степени чувствителен, т.к. медь легирующий элемент в данном образце.
В щелочной среде осаждается никель с помощью 1% этанольного раствора диметилглиоксима. Раствор проверяется на полноту осаждания несколькими каплями 1% этанольного раствора диметилглиоксима. Кобальт и железо осаждаются действием реагента 1 – нитрозо – 2 – нафтол. Осадки отфильтровываются через фильтр «синяя лента». Марганец маскируется с помощью триэтаноламином . Медь в щелочном растворе pH = 12 осаждается с помощью приливания ацетона 20 мл и раствора осадителя (8 – оксихинолин) до появления осадка. Осадок отфильтровывается фильтром «синяя лента». Высушивается и прокаливается в тигле при 800˚С, доведённом до постоянной массы.
4.5.Результаты взвешивания, расчет содержания определяемого элемента
Доведения тигля до постоянной массы:
m1 = 47,87280 г;
m2 = 47,86630 г;
m3 = 47,86628 г;
m тигля = 47,86628г.
Масса тигля с веществом:
m1 = 47,87633 г;
m2 = 47,87126 г;
m3 = 47,86971 г;
m4 = 47,86933 г;
mтигель + вещество = 47,86933г.
mвещества = 47,86933 – 47,86628 = 0,00305 г. ≈ 0,003 г.
mопред.формы = mгравим.форм × F; =0,003*0,181 = 0,000543 г.

W%(Cu) = 0,000543*100/0,2 = 0,27%
4.6.Методика тириметрического определения кобальта; приготовление первичного стандартного раствора; результаты тирования; расчет содержания определяемого элемента.
Для титриметрического определения кобальта был выбран метод обратного титрования из – за невысокой скорости химической реакции.
Точная навеска 0,2 г. растворяется в 100 мл соляной кислоты. Далее выполняется маскирование и осаждение мешающих элементов.
Проведению метода мешают ионы меди, железа, марганца и никеля. Никель осаждается диметилглиоксимом, медь маскируется тиомочевинной, добавленной в сухом виде на кончике шпателя. Железо частично убирается при осаждении никеля, но маскируется дополнительно с помощью солей винной кислоты. Марганец маскируется триэтаноламином.
К анализируемому раствору прибавляют в небольшом избытке 0,1 М раствор комплексона III. Если полученный раствор имеет кислую реакцию, то его нейтрализуют раствором NaOH и прибавляют на каждые 100 мл раствора 2 мл буферного раствора с pH 10. Избыток комплексона III быстро оттитровывают раствором Zn2+ в присутствии эриохрома чёрного Т до перехода окраски раствора из голубой в красную.
Реагенты:
ЭДТА 0,1 н;
ZnCl2 0,09н;
Эриохромовый чёрный Т.
Приготовление ЭДТА
Фиксанал с точной концентрацией 0,1н разбивается и количественно переносится в колбу вместимостью 1000 мл.
Приготовление соли Zn2+
По формуле m = Cн  M
M  Э
Э  V = 0,1
V = 0,1  65+35,5+35,5)/2)
65+35,5+35,5)/2)  1 = 6,8 г.
1 = 6,8 г.
6,8 г. соли ZnCl2 растворяем в 1000 мл H2O.
Cтрандартизация ZnCl2
Аликвотную часть раствора (10 мл) переносят в коническую колбу для титрования, прибавляют цилиндром 20 мл воды, 5 мл буферного раствора и на кончике шпателя 20-30 мг индикаторной смеси (эриохромовый чёрный Т). При растворении тируют ЭДТА до изменения окраски из вино-красной в голубую или синюю. Определяют концентрацию цинка в исследуемом растворе.
VT1 = 8,5 мл;
VT2 = 9 мл;
VT3 = 9,5 мл.
VT среднее = 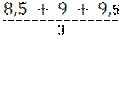 = 9 мл.
= 9 мл.
С0V0 = CTVT

Определение содержания кобальта
В коническую колбу добавляем:
10 мл аликвоты;
20 мл H2O;
12 мл ЭДТА;
5 мг эриохромовый черный Т
Титруем солью Zn2+ до перехода окраски из синей в красную.
VT1 = 6,5 мл;
VT2 = 6,6 мл;
VT3 = 6,7 мл.
VT среднее = 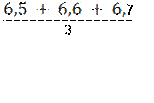 = 6,6 мл.
= 6,6 мл.
С0V0 = С1V1 - CTVT ;
С0 =  =
=  = 0,0212 н.
= 0,0212 н.
nэ = 0.00212
m (Co) = Cн 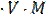 э = 0,00212
э = 0,00212  29,5
29,5  10-2 = 0,0006254 г. в 10 мл H2O
10-2 = 0,0006254 г. в 10 мл H2O
в 100 мл H2O 0,0006254  10 = 0,006254 г.
10 = 0,006254 г.
W% (Co) =  = 3,127%.
= 3,127%.
Заключение. Обобщение результатов анализа.
На основании проведённого качественного анализа содержание меди, определенное гравиметрическим методом, составило :
W % (Cu) = 0,27%;
Содержание кобальта, определенного титриметрическим методом, составило:
W % (Co) = 3,127%;
6.Список литературы.
1. Посыпайко В. И., Васина Н. А. Аналитическая химия и технический анализ. Издательство «Высшая школа», 1979. С.288-313
2. Золотов Ю. А. Основы аналитической химии. Москва «Высшая школа», 2004. С.204
3. Золотов Ю. А. Основы аналитической химии. Практическое руководство. Москва «Высшая школа», 2001. С.17-71
4. Пятницкий И. В. Аналитическая химия кобальта. Издательство «Наука», 1965. С. 87-126
5. Малютина Т. М., Конькова О. В. Аналитический контроль в металлургии цветных и редких металлов. Москва «Металлургия», 1988. С. 86-140.