 |
|
ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Первое начало термодинамики устанавливает связь между теплотой, работой и изменением внутренней энергии тел. Однако не всякий процесс, удовлетворяющий первому началу термодинамики, может быть реализован. Второе начало термодинамики устанавливает направление самопроизвольных процессов в природе и условия осуществления превращения теплоты в работу, с которыми приходится иметь дело на практике.
С другой стороны, первое начало термодинамики устанавливает существование у всякой системы однозначной функции состояния – внутренней энергии. Второе начало термодинамики устанавливает существование у всякой равновесной системы другой однозначной функции состояния – энтропии, которая не изменяется у изолированно системы только при равновесных процесса и всегда возрастает при неравновесных процессах в ней. Таким образом, если первое начало термодинамики есть закон сохранения энергии в применении к термодинамическим системам, то второе начало термодинамики представляет собой закон об энтропии.
Также как и 1-е начало термодинамики 2-е начало является обобщением опытных данных.Многолетняя человеческая практика привела к установлению определённых закономерностей превращения теплоты в работу и работы в теплоту. В результате анализа их закономерностей и было сформулировано второе начало термодинамики в виде закона о существовании энтропии и её не убывании при любых процессах в изолированных системах.
Обратимые и необратимые процессы
Обратимым термодинамическим процессом называется процесс, допускающий возможность возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения.
Обратимым может быть лишь равновесный процесс, так как при равновесном процессе система проходит непрерывную последовательность состояний, бесконечно мало отличающихся друг от друга. Примером обратного механического процесса может быть свободное падение тела в пустоте (без трения). Следует отметить, что всякий механический процесс, в котором отсутствует трение обратим. Если тело испытывает упругий удар о горизонтальную поверхность, то оно возвращается в исходную точку траектории, причём форма тела и поверхности после удара восстанавливается. Каких-либо изменений в окружающих телах не произойдёт.
Запишем первое начало для процесса, переводящего систему из состояния 1 в состояние 2:  , здесь Q12 –количество теплоты, полученное системой,
, здесь Q12 –количество теплоты, полученное системой, 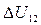 - изменение внутренней энергии системы, А12 – работа, совершаемая системой.
- изменение внутренней энергии системы, А12 – работа, совершаемая системой.
Изменяя величины воздействия, можно вернуть тело из состояния 2 в первоначальное состояние 1. Тогда:
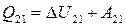
Внутренняя энергия есть функция состояния тела, тогда:
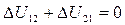 .
.
Поэтому:
 .
.
Процессы, не удовлетворяющие приведенному условию равновесности, называется необратимыми.Примеры необратимых процессов: расширение газа в пустоту, диффузия двух газов, теплопередача.
Переход от более упорядоченных состояний к менее упорядоченным – в этом состоит сущность необратимости. Необратимость есть результат проявления статистических закономерностей, свойственных системам с большим числом частиц.
Существует ряд формулировок второго начала термодинамики, которые подчёркивают различные стороны проблемы.
Формулировка Клаузиуса(1850 г.): процесс, при котором в системе не происходит никаких изменений, кроме передачи теплоты от горячего тела к холодному, является необратимым; иначе говоря, теплота не может самопроизвольно перейти от более холодного к более горячему телу без каких-либо изменений в системе.
Формулировка Томсона(1851 г.): процесс, при котором теплота переходит в работу, является необратимым; иначе говоря, невозможно преобразовать в работу всю теплоту, взятую от тела с однородной температурой, не производя никаких других изменений в состоянии системы.
Второе начало термодинамики исторически было сформулировано на основе анализациклических процессов. Все возможные процессы делятся на обратимые и необратимые. Соответственно второе начало термодинамики формулируется для обратимых и необратимых процессов.