 |
|
Изучение закона Столетова
Методика лабораторного эксперимента
1. Установите режим ускоряющего напряжения.
2. Разместите на оптической скамье лампу накаливания и фотоэлемент на расстоянии друг от друга примерно 300 – 400 мм. Установите напряжение на фотоэлементе, соответствующее току насыщения.
3. Установите максимальный накал лампы. Измерьте фототок насыщения.
4. Отодвигая фотоэлемент каждый раз на 40 – 50 мм (и сохраняя при этом ориентацию фотоэлемента на источник света), измеряйте фототок при различных расстояниях r от источника света до фотоэлемента. Результаты измерений записывайте в табл. 10.
Таблица 10
Зависимость фототока фотоэлемента от расстояния от осветителя
| Расстояние r, м | |||||||
| Величина 1/r2 | |||||||
| Фототок IН, мкА |
5. Постройте график зависимости IH = f (1/r2).
6. В выводе отразите, есть ли соответствие полученной зависимости закону Столетова.
Контрольные вопросы
1. Что такое световой поток?
2. Какова связь между длиной волны, частотой и скоростью света.
3. Что такое фотон (квант света)?
4. Чему равна энергия фотона?
5. В чем заключается явление фотоэффекта?
6. Сформулируйте законы Столетова для фотоэффекта.
7. Сформулируйте и объясните уравнение Эйнштейна для фотоэффекта.
8. Что такое граничная частота?
9. Что понимают под красной границей фотоэффекта?
10. Объясните термин "задерживающая разность потенциалов".
11. Как найти задерживающий потенциал?
12. Как зависит задерживающий потенциал от частоты падающего света?
13. От чего зависит скорость фотоэлектронов?
14. Чему равен угловой коэффициент зависимости Uз = f(v)?
15. Что называется спектральной и вольт-амперной характеристиками фотоэлемента?
16. Какой вид имеет вольт-амперная характеристика при освещении его светом:
а) с частотой, большей граничной;
б) с частотой, меньшей граничной;
в) равной граничной частоте?
17. Как устроен вакуумный фотоэлемент?
Лабораторная работа №6
ИЗУЧЕНИЕ СПЕКТРОВ ИСПУСКАНИЯ
Цель работы: градуировка спектрометра, измерение длин волн оптических спектров, определение постоянной Ридберга.
Оборудование:спектрометр, водородная и ртутная лампы, источник питания.
Введение
Излучение различных источников света состоит из электромагнитных волн с различными длинами λ. Получение спектра, путем разложения его на отдельные монохроматические пучки, осуществляют обычно с помощью призмы, либо дифракционной решетки.
Спектр испускания света ионизированного газа имеет наиболее простой вид и представляет из себя линейчатый спектр, т.е. представляет из себя набор линий, каждой из которых соответствует определенная длина волны λ. Некоторые из этих линий лежат в видимой части спектра, но большая часть их находится в инфракрасной или ультрафиолетовой областях спектра и непосредственно глазом не воспринимаются. Закономерности расположения линий хорошо изучены в спектре наиболее простого атома – водорода.
Спектр атома водорода содержит несколько серий, для каждой из которых длина волны выражается как функция натуральных чисел:
 , ,
| (23) |
где R = 1,0967∙107 м-1 – постоянная Ридберга, n и k – целые числа: n – номер серии n = 1, 2, 3,…; k = n+1, n+2, n+3,…
Несколько линий спектра атомов водорода схематично изображены на рис. 16. Самую длинноволновую линию серии называют головной и обозначают λα, далее следует λβ, λγ и так далее.
λδ λγ λβ λα λδ λγ λβ λα λδ λγ
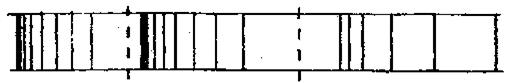
Серия Лаймана Серия Бальмера Серия Пашена λ →
Рис. 16. Участок спектра излучения атома водорода
Первая квантовая теория атома водорода, объясняющая линейчатый спектр испускания и сериальную формулу (23), разработана Н.Бором на основе планетарной модели строения атома. В основе теории Бора лежат следующие постулаты, разрешающие только квантовые состояния атома:
1. электрон, вращаясь вокруг ядра, находится в одном из стационарных состояний, для которых момент импульса электрона квантован:
 ; ;
| (24) |
электрон движется по любой стационарной орбите, не излучает и не поглощает энергию;
2. при переходе электрона с одной из дальних стационарных орбит на более близкую к ядру атом излучает квант энергии, который равен разности энергий электрона на стационарных состояниях:
 . .
| (25) |
Метод измерений
Из теории Бора следует, что числа k и n в формуле (23) – это номера орбит, между которыми происходит переход электрона. Полагая в формуле (23) n = 1, k = 2, 3,…– получим выражение, позволяющее рассчитать длины волн, входящих в серию Лаймана. Все линии этой серии расположены в ультрафиолетовой области спектра. Полагая n = 2, k = 3, 4,…– получаем серию Бальмера, часть линий которой находится в ультрафиолетовой области спектра, а четыре линии –в видимой части спектра. Из них числу k = 3 соответствует красная линия, которую обозначают λα, k = 4 – синяя, k = 5 – сине-фиолетовая и так далее. Эта часть спектра атома водорода изучается в эксперименте. В инфракрасной области спектра атома водорода находятся все остальные серии.
Описанные переходы электронов в атоме водорода можно показать на диаграмме энергетических состояний (рис. 17), где горизонтальные линии означают уровень энергии, а стрелки – направление электронных переходов, которые сопровождаются излучением света. Измеряя длины волн в спектре атома водорода, можно с помощью формулы (23) определить постоянную Ридберга.