 |
|
ТЕПЛОВЫЕ ЯВЛЕНИЯ В ТВЕРДЫХ ТЕЛАХ И ЖИДКОСТЯХ
(введение к работам № 27-31)
Теплоемкостью тела C называется величина, численно равная количеству тепла, которое нужно сообщить телу, чтобы изменить его температуру на один градус:
 (1).
(1).
Теплоемкость тела является аддитивной величиной, пропорциональной массе тела. Тепловые свойства вещества характеризуются удельной теплоемкостью, то есть теплоемкостью единицы массы тела. Очевидно, что между удельной теплоемкостью c и теплоемкостью тела C существует соотношение:
С=mc (2)
где m - масса тела.
Определение теплоемкости посредством формулы (1) само по себе еще недостаточно, так как требуемое для нагревания количество тепла зависит не только от изменения температуры, но и от других условий, в которых производится нагревание. Поэтому определяют теплоемкость с указанием условий, при которых производится нагревание, в частности: теплоемкость при постоянном давлении, теплоемкость при постоянном объеме.
В дальнейшем преимущественно будем пользоваться молярной теплоемкостью – теплоемкостью одного моля, обозначая ее C с соответствующим индексом: так Cv - молярная теплоемкость при постоянном объеме, Cp - молярная теплоемкость при постоянном давлении.
Из первого начала термодинамики dQ=dE+PdV следует, что при постоянном объеме V количество тепла dQ равно приращению внутренней энергии тела dE. Поэтому, если вещество взято в количестве одного моля, то:
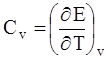 (3)
(3)
Индекс v у производной означает, что дифференцирование производится при постоянном объеме. Это указание необходимо, так как внутренняя энергия тела может зависеть не только от его температуры, но и от других величин, характеризующих состояние тела. Поэтому результат дифференцирования зависит от того, какая именно из этих величин предполагается постоянной.
Если тело нагревается при постоянном давлении Р, то
dQ=dE+PdV=d(E+PV) (P=const)
Мы видим, что количество тепла, полученное телом, оказывается равным приращению величины W=E+PV, которая называется энтальпией тела (употребляется также название теплосодержание).
Таким образом,
 (4)
(4)
Всегда выполняется соотношение
Cp ³ Cv (5)
Можно установить общее соотношение между удельными теплоемкостями Cp и Cv:
 (6)
(6)
где Т – абсолютная температура тела, r - его плотность,  - термический коэффициент объемного расширения,
- термический коэффициент объемного расширения,  - изотермическая сжимаемость тела.
- изотермическая сжимаемость тела.
У всех твердых тел коэффициент теплового расширения мал (  град-1), поэтому Cp и Cv незначительно отличаются друг от друга (у железа, например, отношение теплоемкостей Cp/Cv=1,02) и можно не делать между ними различия, говоря просто об удельной теплоемкости твердого тела С.
град-1), поэтому Cp и Cv незначительно отличаются друг от друга (у железа, например, отношение теплоемкостей Cp/Cv=1,02) и можно не делать между ними различия, говоря просто об удельной теплоемкости твердого тела С.
Согласно теореме Нернста Cv® 0 при T® 0, поэтому Cv с понижение температуры должна убывать. В диэлектриках с достаточно простыми кристаллическими решетками Cv~(T/TD)3 (закон кубов Дебая) при малых Т, а в области высоких температур Cv=3R (закон Дюлонга и Пти). Низкими или, соответственно, высокими являются температуры, которые удовлетворяют соответственно неравенствам:
T<<TD, T>>TD,
где TD - так называемая температура Дебая. Различные вещества имеют разные температуры Дебая, которые для большинства веществ лежат в области 100-1000 К.

|
Если рассматривать зависимость Cv от T/TD, то она оказывается универсальной для всех твердых тел с простыми кристаллическими решетками. На рис.1 приведен график зависимости молярной теплоемкости кристалла с простой кристаллической решеткой от температуры.
В молекулярных кристаллах зависимость CV от Т носит более сложный характер. В металлах вклад в теплоемкость вносят также и электроны проводимости. Правда этот вклад весьма мал, так что его следует учитывать либо при очень низких температурах, когда теплоемкость кристаллической решетки становится очень малой, что имеет место при температурах порядка нескольких градусов Кельвина, либо при очень точных измерениях в области высоких температур (T>TD)[4]. Все эти особенности поведения теплоемкости при низких температурах объясняются квантовыми эффектами.
Если тело нагрето неравномерно, то в нем возникает поток тепла, направленный из мест с высокой температурой в места с низкой температурой. Соотношение между потоком тепла dQ, протекающим за время dt, через однородную пластинку толщины dx и площади S при разности температур dT на ее поверхностях определяется законом Фурье:
 (7)
(7)
где k – коэффициент, характеризующий свойства среды и называемый коэффициентом теплопроводности.
Процесс теплопроводности в жидкостях и газах носит более сложный характер, т.к. наличие различных температур в разных точках жидкости обычно приводит к возникновению макроскопических движений в жидкости.(конвекции). Перенос тепла при конвекции обусловлен движением жидкости (газа) и не подчиняется закону Фурье. Теплообмен твердого тела с газом или жидкостью подчиняется закону Ньютона, согласно которому q - тепло теряемое (или поглощаемое) единицей площади поверхности тела в единицу времени определяется разностью температур DT тела и окружающей его среды:
Q=a×DT (8),
где a - коэффициент, зависящий от свойств поверхности тела и среды.
Нагревание твердого тела приводит к изменению его размеров (тепловое расширение), а при достаточно высоких температурах происходит плавление тела. Причины теплового расширения твердых тел можно понять, если учесть ангармоничность тепловых колебаний атомов в кристаллической решетке. Если обозначить через x смещение атома от его положения равновесия, то с учетом ангармонизма потенциальную энергию атомов можно записать в виде:
U(x)=ax2 – bx3 (9)
где а и b - положительные константы. Второе слагаемое описывает асимметрию потенциальной энергии, т. е. учитывает ангармонизм колебаний. Обычно это слагаемое мало по сравнению с первым членом разложения[5].
Оценим среднее смещение атома от положения равновесия, считая среднюю за период колебаний силу, действующую на атом, равной нулю:
 (10)
(10)
Так как ангармоничность колебаний мала, то их в первом приближении можно считать гармоническими и воспользоваться теоремой о равнораспределении тепловой энергии по степеням свободы, согласно которой:

Откуда
 (11)
(11)
Подставляя это соотношение в (10), получим:
 (12)
(12)
Равновесное положение каждого атома в решетке определяется взаимодействием его с соседними атомами. Поэтому áxñ показывает изменение среднего расстояния между атомами решетки. Как следует из (12) среднее увеличение равновесного расстояния между атомами áxñ растет с ростом температуры по линейному закону, что представляет собой обычное свойство теплового расширения: размер тела растет линейно с ростом температуры. Кроме того, соотношение (12) показывает, что тепловое расширение обусловлено именно ангармонизмом тепловых колебаний, т. к. áxñ ~ b. Связать подобным же образом постоянные а и b с температурой плавления тела не удается, хотя ясно, что плавление тоже связано с эффектами ангармонизма колебаний решетки.
Переход тела из одного агрегатного состояния в другое (фазовый переход) происходит при определенной температуре, которая зависит от давления. Эта зависимость описывается уравнением Клапейрона-Клаузиуса:
 (13),
(13),
где V2 и V1 удельные (на единицу массы) объемы тела в соответствующих агрегатных состояниях (фазах), l - удельная теплота фазового перехода из состояния 1 в состояние 2, т.е. то количество тепла, которое необходимо сообщить единице массы тела, чтобы осуществить этот переход.
Если при фазовом переходе T=const, то и P=const. Но тогда количество тепла, полученное телом при фазовом переходе:
l=Q=DE+P×DV=D(E+PV)=DW.
Иными словами, удельная теплота фазового перехода равна приращению энтальпии тела при фазовом переходе.
Следует иметь в виду, что достижение температуры, при которой возможен фазовый переход еще не означает, что этот переход непременно осуществится. Дело в том, что образование новой фазы начинается в отдельных точках тела, где образуются зародыши новой фазы. Размеры этих зародышей малы, поэтому, благодаря действию сил поверхностного натяжения давление в них будет больше, чем в окружающем их веществе. Это нарушает тепловое равновесие зародыша и тела, и зародыши начинают уменьшаться вплоть до исчезновения. Образованию и росту зародышей способствуют различные дефекты в теле (примеси и т. д.). Кроме того, большинство твердых тел смачивается их расплавом полностью, а это означает, что плавление начинается с поверхности тел. В самом деле, если, например, при плавлении капля расплава образовалась на поверхности тела, то она растечется по его поверхности и давление в ней будет равно атмосферному, так как радиус кривизны такой капли R очень велик, а поверхностное давление ~1/R, окажется пренебрежимо малым. Наблюдать перегрев в таких веществах можно лишь в том случае, когда нагрев тела производится изнутри, например, электрическим током, а поверхность его при этом интенсивно обдувается холодным воздухом. Также в случае окисленной поверхности возможен перегрев тела при плавлении, т.к. температура плавления окисла несколько отличается от температуры плавления чистого кристалла. Тогда плавление может начаться изнутри, а в этом случае важную роль будет играть эффект поверхностного натяжения, который и приведет к перегреву. Аналогичные процессы имеют место и при фазовых переходах жидкость – газ.
РАБОТА № 27