 |
|
Первое начало термодинамики
96. (a, l). Укажите правильное определение работы. Работой называется...
96.1. ... форма передачи энергии без изменения внешних параметров системы, т.е. на микроскопическом уровне;
96.2. ...форма передачи энергии без изменения внешних параметров системы, т.е. на макроскопическом уровне;
96.3. ...форма передачи энергии, связанная с изменением внешних параметров системы, т.е. на макроскопическом уровне;
96.4. ...форма передачи энергии, связанная с изменением внешних параметров системы, т.е. на микроскопическом уровне;
96.5. ...форма передачи энергии, связанная с изменением внешних и внутренних параметров системы.
97. (a, l). Укажите правильное определение теплоты. Теплотой называется ...
97.1. ...форма передачи энергии без изменения внешних параметров системы, т.е. на микроскопическом уровне;
97.2. ...форма передачи энергии без изменения внешних параметров системы, т.е. на макроскопическом уровне;
97.3. ... форма передачи энергии, связанная с изменением внешних параметров системы, т.е. на макроскопическом уровне;
97.4. ... форма передачи энергии, связанная с изменением внешних параметров системы, т.е. на микроскопическом уровне;
97.5. ... форма передачи энергии, связанная с изменением внешних и внутренних параметров системы.
98. (a, l). Укажите правильную формулировку первого начала термодинамики.
98.1. Количество теплоты, подведенное к системе, расходуется на изменение ее внутренней энергии;
98.2. количество теплоты, подведенное к системе, расходуется на совершение системой работы против внешних сил;
98.3. количество теплоты, подведенное к системе, расходуется на изменение ее внутренней энергии и на совершение системой работы против внешних сил;
98.4. внутренняя энергия системы изменяется за счет работы внешних сил;
98.5. внутренняя энергия системы изменяется за счет подведенной к системе теплоты;
98.6. внутренняя энергия системы есть функция состояния, которая изменяется за счёт внешних воздействий;
98.7. внутренняя энергия системы есть функция состояния, которая изменяется за счёт работы внешних сил и подведенной к системе теплоты;
98.8. внутренняя энергия системы есть функция процесса.
99. (a, l). Укажите правильную запись первого начала термодинамики.
99.1.dU = dQ+dA; 99.2.dQ = dU+dA; 99.3.dQ = dU-dA; 99.4. dA = dU+dQ; 99.5. dA = dU -dQ; 99.6. dU = dQ-dA; 99.7. dA = dQ - dU; 99.8. dQ =dU+dA.
100. (a, l). Отметьте правильное суждение относительно знака работы в термодинамических процессах.
100.1. dA < 0 - работа совершается системой против внешних сил;
100.2. dA > 0 - работа совершается системой против внешних сил;
100.3. dA > 0 - внешние силы совершают работу над системой;
100.4. dA = 0 - работа совершается системой против внешних сил;
100.5. для определения знака работы нужно знать массу газа;
100.6. система расширяется, при этом она совершает положительную работу против внешних сил;
100.7. объём системы увеличивается, что приводит к совершению положительноцй работы против внешних сил;
100.8. для определения знака работы нужно знать сорт газа.
101. (a, l). Отметьте правильное суждение относительно знака работы в термодинамических процессах.
101.1. dA < 0 - внешние силы совершают работу над системой;
101.2. dA > 0 - внешние силы совершают работу над системой;
101.3. dA < 0 - работа совершается системой против внешних сил;
101.4. dA = 0 - внешние силы совершают работу над системой;
101.5. для определения знака работы нужно знать массу газа;
101.6. система сжимается, при этом внешние силы совершают отрицательную работу над системой;
101.7. объём системы уменьшается, что соответствует совершению внешними силами отрицательной работы над системой;
101.8. для определения знака работы нужно знать сорт газа.
102. (a, l). Отметьте правильное суждение относительно знака теплоты, которой система обменивается с окружающей средой в термодинамических процессах.
102.1. dQ < 0 - теплота подводится к системе;
102.2. dQ > 0 - теплота отдается системой;
102.3. dQ > 0 - теплота подводится к системе;
102.4. dQ = 0 - теплота подводится к системе;
102.5. для определения знака теплоты нужно знать массу газа;
102.6. так как Q –алгебраическая величина, принято следующее правило знаков: dQ > 0 -внешняя среда передаёт теплоту системе;
102.7. dQ > 0 – система получает теплоту от внешней среды;
102.8. для определения знака теплоты нужно знать сорт газа.
103. (a, l). Отметьте правильное суждение относительно знака теплоты, которой система обменивается с окружающей средой в термодинамических процессах.
103.1. dQ < 0 - теплота отдается системой;
103.2. dQ > 0 - теплота отдается системой;
103.3. dQ < 0 - теплота подводится к системе;
103.4.dQ = 0 - теплота отдается системой;
103.5. для определения знака теплоты нужно знать сорт газа;
103.6. dQ < 0 - внешняя среда получает тепло от системы;
103.7. так как Q –алгебраическая величина, принято следующее правило знаков: dQ < 0 –система отдаёт тепло окружающей среде;
103.8 для определения знака теплоты нужно знать массу газа.
104. (a, l). Укажите правильную запись.
104.1.  ; 104.2.
; 104.2.  ; 104.3.
; 104.3.  ; 104.4.
; 104.4.  ; 104.5.
; 104.5.  ; 104.6. так как работа - функция процесса, то
; 104.6. так как работа - функция процесса, то  есть работа при переходе системы из состояния 1 в состояние 2;
есть работа при переходе системы из состояния 1 в состояние 2;
104.7.  ; 104.8. так как работа - функция состояния, то
; 104.8. так как работа - функция состояния, то  .
.
105. (a, l). Укажите правильную запись.
105.1.  ; 105.2.
; 105.2.  ; 105.3.
; 105.3.  ; 105.4.
; 105.4.  ; 105.5.
; 105.5.  ;
;
105.6. так как теплота - функция процесса, то  есть теплота, полученная или отданная системой при переходе её из состояния 1 в состояние 2;
есть теплота, полученная или отданная системой при переходе её из состояния 1 в состояние 2;
105.7. в разных процессах теплота, полученная или отданная системой, будет разной, поэтому  есть теплота, полученная или отданная системой при переходе её из состояния 1 в состояние 2;
есть теплота, полученная или отданная системой при переходе её из состояния 1 в состояние 2;
105.8. так как теплота - функция состояния, то  .
.
106. (b, l). Укажите правильное определение теплоемкости вещества. Теплоемкостью вещества называется ...
106.1. ...количество теплоты, которое нужно подвести к данной массе вещества, чтобы изменить его температуру на один градус;
106.2. ... количество теплоты, которое нужно подвести к данной массе вещества;
106.3. ... количество теплоты, которое нужно подвести к единице массы вещества:
106.4. ... количество теплоты, которое нужно подвести к единице массы вещества, чтобы изменить его температуру на один градус;
106.5. ... количество теплоты, которое нужно подвести к одному молю вещества.
107. (b, l). Укажите правильное определение молярной теплоемкости вещества. Молярной теплоемкостью вещества называется ...
107.1. ...количество теплоты, которое нужно подвести к единице массы вещества;
107.2. ... количество теплоты, которое нужно подвести к единице объема вещества, чтобы изменить его температуру на один градус;
107.3. .количество теплоты, которое нужно подвести к одному молю вещества, чтобы изменить его температуру на один градус;
107.4. ... количество теплоты, которое нужно подвести к данной массе вещества;
107.5. ... количество теплоты, которое нужно подвести к одному молю вещества;
107.6. .количество теплоты, которое нужно подвести к одному молю вещества, чтобы изменить его температуру на один кельвин;
107.7. отношение количества теплоты, подведённого к одному молю вещества, к соответствующему изменению температуры;
107.8. количество теплоты, которое нужно подвести к единице объема вещества.
108. (b, l). Укажите правильное определение удельной теплоемкости вещества. Удельной теплоемкостью вещества назовется ...
108.1. ...количество теплоты, которое нужно подвести к одному молю вещества, чтобы изменить его температуру на один градус;
108.2. ...количество теплоты, которое нужно подвести к единице объема вещества;
108.3. ... количество теплоты, которое нужно подвести к данной массе вещества, чтобы изменить его температуру на один градус;
108.4. ... количество теплоты, которое нужно подвести к единице массы вещества, чтобы изменить его температуру на один градус;
108.5. ... количество теплоты, которое нужно подвести к единице массы вещества;
108.6.... количество теплоты, которое нужно подвести к единице массы вещества, чтобы изменить его температуру на один кельвин;
108.7. отношение количества теплоты, подведённого к единице массы вещества, к соответствующему изменению температуры;
108.8. ... количество теплоты, которое нужно подвести к единице объема вещества, чтобы изменить его температуру на один градус.
109. (b, l). Чему равна молярная теплоемкость одноатомного идеального газа в изохорическом процессе?
109.1.  ; 109.2.
; 109.2.  ; 109.3.
; 109.3.  ; 109.4.
; 109.4. 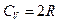 ; 109.5.
; 109.5.  ;
;
109.6.  ; 109.7.
; 109.7.  ; 109.8.
; 109.8.  .
.
110. (b, l). Чему равна молярная теплоемкость двухатомного идеального газа в изохорическом процессе?
110.1. 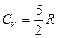 ; 110.2.
; 110.2.  ; 110.3.
; 110.3.  ; 110.4.
; 110.4.  ; 110.5.
; 110.5. 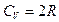 ;
;
110.6. 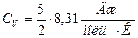 ; 110.7.
; 110.7.  ; 110.8.
; 110.8.  .
.
111. (b, l). Чему равна молярная теплоемкость трехатомного идеального газа в изохорическом процессе?
111.1.  ; 111.2.
; 111.2. 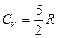 ; 111.3.
; 111.3. 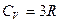 ; 111.4.
; 111.4.  ; 111.5.
; 111.5.  ;
;
111.6.  ; 111.7.
; 111.7.  ; 111.8.
; 111.8.  .
.
112. (b, l). Чему равна молярная теплоемкость одноатомного идеального газа в изобарическом процессе?
112.1.  ; 112.2.
; 112.2.  ; 112.3.
; 112.3.  ; 112.4.
; 112.4.  ; 112.5.
; 112.5.  ; 112.6.
; 112.6.  ; 112.7.
; 112.7.  ; 112.8.
; 112.8.  .
.
113. (b, l). Чему равна молярная теплоемкость двухатомного идеального газа в изобарическом процессе?
113.1.  ; 113.2.
; 113.2.  ; 113.3.
; 113.3.  ; 113.4.
; 113.4.  ; 113.5.
; 113.5. 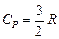 ;
;
113.6.  ; 113.7.
; 113.7.  ; 113.8.
; 113.8.  .
.
114. (b, l). Чему равна молярная теплоемкость трехатомного идеального газа в изобарическом процессе?
114.1.  ; 114.2.
; 114.2.  ; 114.3.
; 114.3.  ; 114.4.
; 114.4.  ; 114.5.
; 114.5.  ;
;
114.6.  ; 114.7.
; 114.7.  ; 114.8.
; 114.8.  .
.
115. (b, l). Чему равна молярная теплоемкость идеального газа в изохорическом процессе (i - число степеней свободы молекулы)?
115.1.  ; 115.2.
; 115.2.  ; 115.3.
; 115.3.  ; 115.4.
; 115.4.  ; 115.5.
; 115.5.  ;
;
115.6.  ; 115.7.
; 115.7.  ; 115.8.
; 115.8.  .
.
116. (b, l). Чему равна молярная теплоемкость идеального газа в изобарическом процессе (i - число степеней свободы молекулы)?
116.1.  ; 116.2.
; 116.2.  ; 116.3.
; 116.3.  ; 116.4.
; 116.4.  ; 116.5.
; 116.5.  ;
;
116.6. 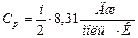 ; 116.7.
; 116.7. 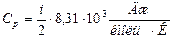 ; 116.8.
; 116.8.  .
.
117. (b, l). Укажите правильную формулу (g - показатель степени в уравнении адиабаты, i - число степеней свободы молекулы).
117.1.  ; 117.2.
; 117.2.  ; 117.3.
; 117.3.  ; 117.4.
; 117.4. 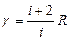 ; 117.5.
; 117.5.  ; 117.6.
; 117.6.  ; 117.7.
; 117.7.  ; 117.8.
; 117.8. 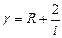 .
.
118. (d, m). Молот массой 2 т падает на стальную болванку массой 10 кг с высоты 3 м. На сколько градусов нагреется болванка при ударе, если на нагревание идет 50 % энергии молота? Удельная теплоемкость стали равна 460 Дж/кг×К.
118.1. 12,8 К; 118.2. 19,0 К; 118.3. 3,2 К; 118.4. 6,4 К; 118.5. 9,5 К;
118.6. 6,40C; 118.7. 6,4 К = 6,40C; 118.8. 3,20C.
119. (b, l). Укажите правильную формулу.
119.1.  ; 119.2.
; 119.2.  ; 119.3.
; 119.3.  ; 119.4.
; 119.4.  ; 119.5.
; 119.5.  ; 119.6.
; 119.6.  ; 119.7.
; 119.7.  ; 119.8.
; 119.8.  .
.
120. (b, l). Какой физический смысл имеет универсальная газовая постоянная R?
120.1. R численно равна изменению внутренней энергии одного моля идеального газа при его изобарном нагревании на 1 К;
120.2. R численно равна количеству теплоты, которое нужно подвести к одному молю идеального газа для его изохорного нагревания на 1 К;
120.3. R численно равна работе изобарического расширения одного моля идеального газа при его нагревании на 1 К;
120.4. R численно равна количеству теплоты, которое нужно подвести к одному молю идеального газа при для его изобарного нагревания на 1 К;
120.5. R численно равна изменению внутренней энергии одного моля идеального газа при его изохорном нагревании на 1 К;
120.6. в изохорическом процессе тепло, подведённое к системе, расходуется на измерение внутренней энергии системы, а в изобарическом процессе часть теплоты идёт на совершение работы, поэтому R численно равна работе изобарического расширения одного моля идеального газа при его нагревании на 1 К;
120.7. так как R есть разность между молярными теплоёмкостями при постоянном давлении и при постоянном объёме, то из первого начала термодинамики следует, что R численно равна работе изобарического расширения одного моля идеального газа при его нагревании на 1 К;
120.8. R численно равна работе при изохорном нагревании на 1 К одного моля идеального газа.
121.(d, m). 10 молей одноатомного идеального газа нагрели на 500 С. Процесс изобарический. Какое количество теплоты получил газ?
121.1. 6,3 кДж; 121.2. 10,5 кДж; 121.3. 18,9 кДж ; 121.4. 15,3 кДж; 121.5. 16,8 кДж;121.6. 10,5∙103 Дж; 121.7. 10,5∙10 -3 МДж; 121.8. 10,5 .Дж
122.(d, m). Определить работу, которую совершает один моль идеального газа при изобарном нагревании на 10 К.
122.1. 83,1 Дж; 122.2. 124,65 Дж; 122.3. 55,4 Дж; 122.4. 138,5 Дж; 122.5. 69,25 Дж;122.6. 0,0831 кДж; 122.7. 83,1∙10 -3 кДж; 122.8. 83,1 кДж.
123.(d, m). Одноатомный идеальный газ получил от нагревателя 2 кДж тепловой энергии. На сколько изменилась его внутренняя энергия? Процесс изобарический.
123.1. На 800 Дж; 123.2.на 1200 Дж; 123.3. на 1000 Дж; 123.4. на 600 Дж; 123.5. на 1600 Дж; 123.6. на 1,2 кДж; 123.7. на 1,2∙103 Дж; 123.8. на 100 Дж.
124.(d, m). На сколько изменится внутренняя энергия 1 моля двухатомного идеального газа при его изобарном нагревании на 10 К?
124.1. На 124,65 Дж; 124.2. на 55,4 Дж; 124.3. на 249,3 Дж; 124.4. на 83,1 Дж; 124.5. на 207,7 Дж; 124.6. на 0, 208 кДж; 124.7. на 2,08∙102 Дж; 124.8. на 20,8 Дж.
125.(d, m). Что можно сказать о количестве теплоты, необходимой для нагревания газа до одной и той же температуры в сосуде, прикрытом поршнем, если поршень не перемещается (Q1) и если поршень легко подвижный (Q2)?
125.1. Q1 > Q2; 125.2. Q1 = Q2; 125.3. Q1 < Q2 ; 125.4. необходимо знать массу газа; 125.5. для разных газов могут быть разные ответы; 125.6. Q2 > Q1;
125.7. в изохорных условиях тепло, подведённое к системе, расходуется только на измерение внутренней энергии системы, а в изобарных условиях часть теплоты идёт на совершение работы, поэтому Q1 < Q2 ;
125.8. необходимо знать молярную массу газа.
126.(a, l). Укажите правильную формулу для адиабатного процесса.
126.1.  ; 126.2.
; 126.2.  ; 126.3.
; 126.3.  ; 126.4.
; 126.4.  ; 126.5.
; 126.5.  ; 126.6.
; 126.6.  ; 126.7.
; 126.7.  ; 126.8.
; 126.8.  .
.
127.(d, m). Удельная теплоемкость некоторого двухатомного газа сP = 14×103 Дж/(моль×К). Найти молярную массу этого газа.
127.1. 4×10-3 кг/моль; 127.2. 28×10-3 кг/моль; 127.3. 14×10-3 кг/моль; 127.4. 2×10-3 кг/моль; 127.5. 16×10-3 кг/моль; 127.6. 2 г/моль; 127.7. 0.002 кг/моль; 127.8. 4 г/моль.
128.(d, m). Найти отношение удельных теплоемкостей  для кислорода.
для кислорода.
128.1. g = 1,33; 128.2. g = 1,67; 128.3. g = 1,4; 128.4. g = 2,01; 128.5. g = 1,87;128.6.  ; 128.7.
; 128.7.  ; 128.8.
; 128.8.  .
.
129.(d, m). Какое количество теплоты Q нужно сообщить массе m = 12 г кислорода, чтобы нагреть его на  = 500С при постоянном объеме?
= 500С при постоянном объеме?
129.1. 545 Дж; 129.2. 467 Дж; 129.3. 234 Дж; 129.4. 623 Дж; 129.5. 390 Дж;129.6. 0,39 кДж; 129.7. 390∙10-3 кДж; 129.8. 39 Дж.
130.(d, m). В закрытом сосуде объемом V = 2 л находится азот, плотность которого
r = 1,4 кг/м3. Какое количество теплоты Q нужно сообщить азоту, чтобы нагреть его на DT = 100 К?
130.1. 208 Дж; 130.2. 145 Дж; 130.3. 104 Дж; 130.4. 290 Дж; 130.5. 324 Дж;130.6. 0,208 кДж; 130.7. 208∙10-3 кДж; 130.8. 145 кДж.
131.(b, l). Отметьте правильную формулу для нахождения работы в изотермическом процессе для одного моля идеального газа.
131.1.  ; 131.2.
; 131.2.  ; 131.3.
; 131.3.  ; 131.4.
; 131.4.  ; 131.5.
; 131.5.  ; 131.6.
; 131.6.  ; 131.7.
; 131.7.  ; 131.8.
; 131.8.  .
.
132.(d, m). К идеальному газу в изотермическом процессе подводится тепло (dQ > 0). Укажите, как изменится объем, давление, внутренняя энергия и какой будет знак у совершенной работы.
132.1. dV > 0, dр < 0, dU > 0, dA > 0 ; 132.2. dV > 0, dр < 0, dU = 0, dA > 0 ;
132.3. dV < 0, dр < 0, dU < 0, dA < 0 ; 132.4. dV < 0, dр > 0, dU > 0, dA = 0 ;
132.5. dV = 0, dр > 0, dU > 0, dA = 0; 132.6. dU = 0, dр < 0, dV > 0, dA > 0;
132.7. dр < 0, dU = 0, dA > 0, dV > 0; 132.8. dU < 0, dр < 0, dV > 0, dA > 0.
133.(b, l). Укажите правильную формулу для нахождения работы в адиабатном процессе для одного моля идеального газа.
133.1.  ; 133.2.
; 133.2.  ; 133.3.
; 133.3.  ; 133.4.
; 133.4.  ; 133.5.
; 133.5.  ; 133.6.
; 133.6.  ; 133.7.
; 133.7.  ; 133.8.
; 133.8.  .
.
134.(d, m). Газ расширяется из одного и того же начального состояния в одном случае изобарно, в другом - изотермически, в третьем - адиабатно. Конечные объемы во всех трех случаях одинаковы. Какое соотношение будет между конечными давлениями р1, р2 и р3?
134.1. р1 > р2 > р3 ; 134.2. р1 < р2 < р3 ; 134.3. р1 < р2 > р3 ; 134.4. р1 > р2 < р3 ;
134.5. р1 > р2 > р3 ; 134.6. р3 < р2 < р1 ; 134.7. р2 > р3 < р1; 134.8. р1 = р2 > р3 .
135.(d, m). Укажите рисунок, на котором правильно изображены изотерма и адиабата.







 135.1. р dT = 0 135.2. р dQ = 0 135.3. р dT = 0
135.1. р dT = 0 135.2. р dQ = 0 135.3. р dT = 0
dQ = 0 dT = 0
dQ = 0
 |

 V V V
V V V




 135.4. р 135.5. р dQ = 0
135.4. р 135.5. р dQ = 0
dT = 0 
dQ = 0
dT = 0

 V V
V V
136.(d, m). На адиабате (см. рис.) изображен процесс перехода системы из состояния 1 в состояние 2. Укажите, как изменилась температура, внутренняя энергия, подведено или отведено тепло и какого знака совершена работа.

 р 136.1. dT > 0, dU > 0, dQ >.0, dA > 0;
р 136.1. dT > 0, dU > 0, dQ >.0, dA > 0;
· 1 136.2. dT < 0, dU < 0, dQ.< 0, dA > 0;
136.3. dT < 0, dU < 0, dQ.= 0, dA > 0;
136.4. dT = 0, dU = 0, dQ.> 0, dA > 0;
136.5. dT < 0, dU < 0, dQ.= 0, dA < 0;
· 2 136.6. dU < 0, dT < 0, dQ.= 0, dA > 0;
 V 136.7. dA > 0, dT < 0, dU < 0, dQ.= 0;
V 136.7. dA > 0, dT < 0, dU < 0, dQ.= 0;
136.8. dU > 0, dT > 0, dQ >.0, dA > 0.
137.(d, m). Какое соотношение будет между работами в изотермическом и адиабатном расширении, а также при сжатии, из одного и того же начального состояния? Конечные объемы при изотермическом и адиабатном расширении одинаковы (аналогично для сжатия).
137.1. (Арасш)адиаб >(Арасш)изот , (Асжат)адиаб < (Асжат)изот ; 
137.2. (Арасш)адиаб <(Арасш)изот , (Асжат)адиаб > (Асжат)изот ;
137.3. (Арасш)адиаб <(Арасш)изот , (Асжат)адиаб = (Асжат)изот ;
137.4. (Арасш)адиаб >(Арасш)изот , (Асжат)адиаб = (Асжат)изот ;
137.5. (Арасш)адиаб =(Арасш)изот , (Асжат)адиаб > (Асжат)изот ;
137.6. (Арасш)изот > (Арасш)адиаб , (Асжат)адиаб > (Асжат)изот ;
137.7.(Арасш)изот > (Арасш)адиаб , (Асжат)изот < (Асжат)адиаб;
137.8. (Арасш)изот > (Арасш)адиаб , (Асжат)изот > (Асжат)адиаб.
138.(d, m). Строго адиабатных оболочек нет. При каком соотношении между количеством тепла dQ, прошедшим через оболочку, и величиной работы dА, совершенной системой, реальный процесс будет ближе к адиабатному?
138.1. Когда  ; 138.2. когда
; 138.2. когда  ; 138.3. когда
; 138.3. когда  ;
;
138.4. когда 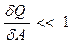 ; 138.5. когда
; 138.5. когда 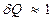 . 138.6. когда
. 138.6. когда  ;
;
138.7. когда подведённое к системе тепло много больше совершённой системой работы
138.8. когда подведённое к системе тепло много меньше совершённой системой работы.
139.(d, m). Объем V1 = 7,5 л кислорода адиабатический сжимается до объема V2 = 1л, причем в конце сжатия установилось давление p2 = 1,6 МПа. Под каким давлением p1 находился газ до сжатия?
139.1. 16 МПа; 139.2. 16 кПа; 139.3. 95 кПа; 139.4. 3,2 МПа; 139.5. 32 кПа;139.6. 95∙103 Па; 139.7. 0,095 МПа; 139.8. 95 МПа.
140.(a, l). Отметьте правильное определение политропного процесса. Политропным называется процесс ...
140.1. ... который описывает все процессы;
140.2. ... без теплообмена с окружающей средой;
140.3. ... при постоянной температуре;
140.4. ... при постоянном давлении;
140.5. ... при постоянной теплоемкости.
141.(b, l). Укажите правильную самую общую формулу для политропного процесса.
141.1. 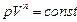 ; 141.2.
; 141.2.  ; 141.3.
; 141.3.  ; 141.4.
; 141.4.  ; 141.5.
; 141.5.  ; 141.6.
; 141.6.  ; 141.7.
; 141.7.  ; 141.8.
; 141.8.  .
.
142.(b, l). Укажите правильное выражение для показателя степени n в уравнении поли-
тропного процесса.
142.1.  ; 142.2.
; 142.2.  ; 142.3.
; 142.3.  ; 142.4.
; 142.4.  ; 142.5.
; 142.5.  . 142.6.
. 142.6.  ; 142.7.
; 142.7.  ; 142.8.
; 142.8.  .
.
143.(b, l). Укажите правильную формулу для теплоемкости С политропного процесса.
143.1. 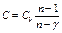 ; 143.2.
; 143.2.  ; 143.3.
; 143.3.  ; 143.4.
; 143.4.  ; 143.5.
; 143.5.  ; 143.6.
; 143.6.  ; 143.7.
; 143.7.  ; 143.8.
; 143.8.  .
.
144.(d, m). Укажите рисунки, на которых для всех изолиний (изохора, изобара, изотерма и адиабата) правильно указаны значения показателя политропы n.






 144.1. p n=g 144.2. p n=±¥
144.1. p n=g 144.2. p n=±¥
n=1 n=g
n=0 n=1
 |  |
n=±¥ n=0

 V V
V V






 144.3. p n=±¥ 144.4. p n=±¥
144.3. p n=±¥ 144.4. p n=±¥
n=1 n=1
n=g n=0 
 |
n=0
 V n=g V
V n=g V



 144.5. p n=1
144.5. p n=1

n=0
n=±¥ 
n=g
 V
V
145.(b, l). Укажите ответ, в котором правильно указано значение показателя политропы n для изохорного процесса.
145.1. p = const, n = ±¥ ; 145.2. V = const, n = ±¥ ; 145.3. V = const, n = 1 ;
145.4. T = const, n = 0 ; 145.5. V = const, n = g .; 145.6. dV = 0, n = ±¥ ;
145.7. изохора, n = ±¥ ; 145.8. dp = 0, n = ±¥.
146.(b, l). Укажите ответ, в котором правильно указано значение показателя политропы n для изобарного процесса.
146.1.p = const, n = 0; 146.2. p = const, n = ±¥ ; 146.3. V = const, n = 0 ;
146.4. p = const n = g ; 146.5. T = const, n = 0 , 146.6. dp = 0, n = 0;
146.7. изобара, n = 0; 146.8. dТ = 0, n = 0.
147.(b, l). Укажите ответ, в котором правильно указано значение показателя политропы n для изотермического процесса.
147.1. T = const, n = ± ¥ ; 147.2. T = const, n = 0 ; 147.3. T = const, n = g ;
147.4. T = const, n = 1; 147.5. V = const, n = 1 ; 147.6. dТ = 0, n = 1;
147.7. изотерма, n = 1; 148.8. dV = 0, n = ± ¥ .
148.(b, l). Укажите ответ, в котором правильно указано значение показателя политропы n для адиабатного процесса.
148.1. dQ = 0, n = 1; 148.2. dQ = 0, n = ± ¥ ; 148.3. dQ = 0, n = g ;
148.4. dQ = 0, n = 0; 148.5. dT = 0, n = g . 148.6. dQ = 0,  ;
;
148.7. dQ = 0,  ; 148.8. T = const, n = g .
; 148.8. T = const, n = g .
149.(b, l). Укажите ответ, в котором правильно указано значение показателя политропы n для уравнения изопроцесса.
149.1. Изохора, V = const, n = 0; 149.2. изобара, p = const, n = ±¥ ;
149.3. изотерма,  = const, n = g ; 149.4. адиабата,
= const, n = g ; 149.4. адиабата,  = const, n = g ;
= const, n = g ;
149.5. изохора, pV = const, n = 1; 149.6. изохора, V = const, n = ±¥ ;
149.7. изобара, p = const, n = 0; 149.8.изотерма,  = const, n = 0.
= const, n = 0.
150.(b, l). Укажите правильное значение теплоемкости для изохорного процесса.
150.1. V = const, C = CP ; 150.2.V = const, C = CV ; 150.3. V = const, C = 0 ; 150.4. V = const, C = ±¥ ; 150.5. p = const, C = CV ; 150.6. V = const,  ;
;
150.7. V = const,  ; 150.8. р = const,
; 150.8. р = const,  .
.
151.(b, l). Укажите правильное значение теплоемкости для изобарного процесса.
151.1. p = const, C = CP ; 151.2. p = const, C = CV ; 151.3. p = const, C = ±¥ ; 151.4. T = const, C = 0; 151.5. V = const, C = CP ; 151.6. p = const,  ;
;
151.7. р = const,  ; 151.8. V = const,
; 151.8. V = const,  .
.
152.(b, l). Укажите правильное значение теплоемкости для изотермического процесса.
152.1. T = const, C = ± ¥ ; 152.2. T = const, C = 0 ; 152.3. T = const, C = CP ; 152.4. T = const, C = CV ; 152.5. p = const, C = ± ¥ ; 152.6. dT = 0, C = ± ¥ ;
152.7. изотерма, C = ± ¥ ; 152.8. dр = 0, C = 0.
153.(b, l). Укажите правильное значение теплоемкости для адиабатного процесса.
153.1. dQ = 0, C = ±¥ ; 153.2. dQ = 0, C =0; 153.3. dQ = 0, C = CV ; 153.4. dQ = 0, C = CP ; 153.5. dT = 0, C = 0 ; 153.6. адиабата, C =0;
153.7.dS = 0, C =0; 153.8. T = const, C = ± ¥ .
154.(b, l). Укажите правильное значение теплоемкости для различных изопроцессов.
154.1. Изохора, С = ± ¥ ; 154.2. изобара, С = CV ; 154.3. изотерма, С = CP ; 154.4. адиабата, С = ± ¥ ;154.5. адиабата, С = 0; 154.6. изохора, С = CV ;
154.7. изотерма, С = ± ¥ ; 154.8. изотерма, С = 0.


 155.(d, m). Укажите правильные кривые зависимости теплоемкости политропного процесса от показателя политропы.
155.(d, m). Укажите правильные кривые зависимости теплоемкости политропного процесса от показателя политропы.
С


 155.1. С 155.2.
155.1. С 155.2.
Сp

 СV
СV

 CP CV
CP CV
 1 g n 1 g n
1 g n 1 g n 





 155.3. С 155.4. С
155.3. С 155.4. С
CP СV

 СV CP
СV CP 

 g 1 n
g 1 n  g 1 n
g 1 n


 155.5. C
155.5. C
СV 

1 g n 
156.(b, l). При каких значениях показателя политропы теплоемкость процесса будет отрицательная?
156.1.1< n < g ; 156.2.  ; 156.3. 0 < n < g ; 156.4. 0 > n > g ; 156.5.1< n < ¥ ; 156.6.
; 156.3. 0 < n < g ; 156.4. 0 > n > g ; 156.5.1< n < ¥ ; 156.6.  ; 156.7.
; 156.7.  ; 156.8.
; 156.8.  .
.
Модуль 4 А