 |
|
Оксид сульфуру(VІ). Сульфатна кислота
Оксид сульфуру(VІ). Оксид сульфуру (VI), або триоксид сульфуру, — це безбарвна рідина, що перетворюється при температурі нижчій 17 °С на тверду кристалічну масу. Він дуже сильно поглинає вологу, утворюючи сульфатну кислоту:
SO3 + Н2О = H2SO4,
тому його зберігають у запаяних колбах.
Оксид сульфуру(VІ) виявляє всі властивості кислотних оксидів. Добувають його окисненням SO2. Він є проміжним продуктом у виробництві сульфатної кислоти.
Молекула SO3 має форму трикутника, в центрі якого розміщений атом сульфуру:
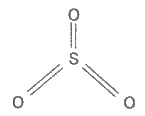
Така будова зумовлена взаємним відштовхуванням зв’язуючих електронних пар. Для її утворення атом сульфуру надав усі шість зовнішніх електронів.
Сульфатна кислота. Найбільше значення має контактний спосіб добування сульфатної (сірчаної) кислоти. Цим способом можна добути H2SO4 будь-якої концентрації, а також олеум, тобто розчин SO3 в H2SO4. Процес складається з трьох стадій: 1) добування SO2;2) окиснення SO2 в SO3; 3) добування H2SO4.
Оксид сульфуру(ІV) SO2 добувають випалюванням піриту FeS2 у спеціальних печах:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2.
Для прискорення випалювання пірит попередньо подрібнюють, а для повнішого вигоряння сірки вводять значно більше повітря (кисню), ніж потрібно для реакції. Газ, що виходить з печі випалювання, складається з оксиду сульфуру(ІV), кисню, азоту, сполук арсену (з домішок у колчедані) і водяної пари. Він називається випалювальним газом.
Випалювальний газ піддають ретельному очищенню; оскільки навіть мізерні кількості сполук арсену, що містяться в ньому, а також пил і волога отруюють каталізатор. Від сполук арсену і від пилу газ очищають, пропускаючи його крізь спеціальні електрофільтри і промивну башту; волога поглинається концентрованою сульфатною кислотою у сушильній башті. Очищений газ, що містить кисень, нагрівається в теплообміннику до 450°С і надходить до контактного апарата. Всередині контактного апарата є решітчасті полички, заповнені каталізатором.
Раніше як каталізатор використовували тонко подрібнену металічну платину. Пізніше вона була замінена сполуками ванадію — оксидом ванадію(V) V2O5 або сульфатом ванадилу VOSO4, які дешевші, ніж платина, і повільніше отруюються.
Реакція окиснення SO2 в SO3 оборотна:
2SO2 + O2 ⇆2SO3.
Збільшення кількості кисню у випалювальному газі підвищує вихід оксиду сульфуру(VІ): при температурі 450°С він звичайно досягає 95% і більше. Оксид сульфуру(VІ) SO3 поглинається концентрованою сульфатною кислотою — утворюється олеум. Розводячи олеум водою, можна дістати розчин кислоти необхідної концентрації. Слід зазначити, що поглинати оксид сульфуру(VІ) концентрованою H2SO4, а не водою доцільніше, тому що він виходить із контактного апарата дрібно розпиленим і з водя ною парою утворює туман, що складається з дрібних краплин сульфатної кислоти, який не поглинається водою. При поглинанні SO3концентрованою сульфатною кислотою туман не утворюється. Концентровану сульфатну кислоту перевозять залізницею у стальних цистернах.