 |
|
Материальный баланс приготовления и спекания шихты
| Поступает | Выходит |
| 1. Боксит mб | 1. Технологические газы mг |
| 2. Сода mс | 2. Спек (по разности) mсп = mш – mг |
| 3. Известняк mизв | |
| Всего шихты mш | Всего продуктов mn |
5. Приготовить шихту рассчитанного состава путем смешения, усреднения и дополнительного измельчения компонентов в фарфоровой ступке. Загрузить шихту в алундовый или шамотный тигель и провести спекание в течение 30-40 мин при температуре 1100 °С. По окончании выдержки тигель охладить, полученный спек взвесить  (практическое количество спека). Рассчитать количество практически полученных технологических газов:
(практическое количество спека). Рассчитать количество практически полученных технологических газов:
 (32)
(32)
и практический выход спека от расчетного количества:
 (33)
(33)
6. Провести выщелачивание спека. Для этого рассчитать количество и состав оборотной промывной воды, обеспечивающей получение алюминатно-щелочного раствора заданного состава с aк = 1,5¸1,7.
Определить aк раствора, образующегося при выщелачивании спека чистой водой:

 , (34)
, (34)
где  – количество Na2O, введенное с содой, г;
– количество Na2O, введенное с содой, г;  – количество Al2O3 в навеске боксита, г.
– количество Al2O3 в навеске боксита, г.
Если  окажется меньше 1,5, то при выщелачивании необходимо добавить некоторое количество свободной каустической щелочи (mк), определяемое из соотношения
окажется меньше 1,5, то при выщелачивании необходимо добавить некоторое количество свободной каустической щелочи (mк), определяемое из соотношения
 , (35)
, (35)
где  – количество Na2О, поступающее на выщелачивание с каустической щелочью в составе промывной воды.
– количество Na2О, поступающее на выщелачивание с каустической щелочью в составе промывной воды.
Из (35) можно определить
 . (36)
. (36)
Тогда потребное количество каустика в граммах
 , (37)
, (37)
где [NaOH]к – содержание NaOH в техническом каустике, %.
При концентрации [Na2Oк] в растворе около 70-80 г/л, объем промывной воды в граммах на литр определяется из соотношения
 , (38)
, (38)
где Vp – искомый объем раствора, примерно равный объему оборотной промывной воды, л.
В стакане на 300-500 мл, при обязательном перемешивании, приготовить синтетическую промывную воду для выщелачивания спека, добавив mк граммов каустика в рассчитанный объем воды Vp. Раствор нагреть до температуры выщелачивания (75-85 °С), внести в него пробу спека и обеспечить изотермическую выдержку пульпы, при перемешивании, в течение 15-20 мин.
7. По окончании выщелачивания пульпу отфильтровать под вакуумом с соблюдением необходимых предосторожностей. Шлам промыть на фильтре 50-70 мл горячей воды, перенести в фарфоровую чашку и просушить. Массу сухого шлама mшл занести в отчет.
8. Алюминатный раствор из колбы Бунзена перенести в коническую колбу на 500 мл, установить ее в водяном термостате и довести температуру раствора до 75-80 °С (температура карбонизации).
9. Подать в объем раствора углекислый газ или газовоздушную смесь известного состава, установив скорость подачи по интенсивности барботажа или показателям расходомеров (задается преподавателем). При использовании в схеме установки газового счетчика перед подачей газа записать его начальные показания (Vн). Состав газа определяется под руководством преподавателя газохроматографическим методом. Контроль завершения карбонизации ведется по величине рН раствора. Для этого каждые 10 мин отбирают пробу раствора (пульпы) объемом около 20 мл, помещают ее в стеклянный стаканчик, охлаждают до комнатной температуры и проводят измерения. По окончании измерений проба возвращается в объем карбонизатора. В конце процесса рН-определяющей реакцией в растворе становится реакция гидролиза Na2CO3 и рН падает до 10,0-10,5. Окончательный контроль завершения карбонизации ведут по исчезновению в растворе каустической щелочи. Для этого к небольшому объему отфильтрованного в пробирку раствора (3-5 мл) добавляют фенолфталеин и избыток 10-процентного раствора BaCl2. Исчезновение малиновой окраски с одновременным выпадением белого осадка говорит о наличии в растворе только углекислого натрия и протекании реакции
Na2CO3 + BaCl2 = BaCO3 + 2NaCl. (39)
По окончании процесса прекратить подачу газа. Записать конечные показания газового счетчика Vк. Отфильтровать под вакуумом гидратную пульпу и промыть на фильтре осадок гидроксида алюминия.
10. Взвесить тигель для кальцинирующего обжига, перенести в него осадок и взвесить повторно. По разнице определить массу влажного гидрата mвл.г.
11. Установить тигель с гидратом в печь и провести кальцинирующий обжиг при температуре 800-900 °С в течение 20-30 мин. По окончании определить массу полученного глинозема mглин.
12. Рассчитать сквозное извлечение Al2O3 в глинозем из боксита в процентах
 , (40)
, (40)
влажность гидрата в процентах
 (41)
(41)
и степень использования СО2 при карбонизации с учетом стехиометрии (23) и (6) в процентах
 , (42)
, (42)
где [CO2] – объемное содержание СО2 в газовоздушной смеси, %; Vк – Vн – объем газовоздушной смеси, пошедшей на карбонизацию, л; Т – температура воздуха в лаборатории, К.
Определить удельные материальные потоки технологии на 1 т глинозема в тоннах или кубических метрах: боксита mб/mглин; известняка mизв/mглин; соды mс/mглин; шихты mш/mглин; спека mсп/mглин; раствора на выщелачивание Vр×103/mглин; шлама mшл/mглин; газа на карбонизацию [(Vк – Vн) 103]/mглин.
13. По указанию преподавателя выполнить фракционный анализ глинозема методом весовой седиментации.
14. Проанализировать полученные результаты.
Работа 3. ПЕРЕРАБОТКА НЕФЕЛИНОВОГО КОНЦЕНТРАТА НА ГЛИНОЗЕМ И ПОПУТНУЮ ПРОДУКЦИЮ
СПОСОБОМ СПЕКАНИЯ
Цель работы – знакомство с теоретическими основами и контурами технологии комплексной переработки нефелинового концентрата. Экспериментальное выполнение основных технологических операций и расчет важнейших технологических показателей.
Основные определения, теория и технология
Нефелинсодержащее сырье – это щелочные алюмосиликаты (фельдшпатоиды), основными из которых являются нефелин и полевые шпаты. В общем виде нефелин выражают формулой Na2K[AlSiO4]4 или R2O×Al2O3×2SiO2, а в технологии глинозема упрощенно – Na2O×Al2O3×2SiO2. В своей основе кристаллическая решетка нефелина имеет структуру тридимита. В ней тетраэдры кремнезема замещены тетраэдром алюминия, а большинство пустот заполнено атомами щелочных металлов. Нефелин имеет четыре модификации: кубическую (a-Na2O×Al2O3×2SiO2), устойчивую выше 1248 °С; низкотемпературную гексагональной формы (b-Na2O×Al2O3×2SiO2); триклинную, получаемую при быстром охлаждении расплава нефелина, иногда называемую b-карнегиитом, и (четвертую) ниже 227 °С – с изменением двупреломления. Природный нефелин обычно имеет кристаллическую решетку гексагональной сингонии. По внешнему виду это бесцветный минерал, но часто имеет серовато-белый или серый цвет с желтоватым, буроватым, красноватым или зеленоватым оттенком. Температура плавления нефелина 1526 °С; твердость 5,5-6,0; плотность 2620 кг/м3.
Ценность нефелинового сырья для технологии производства глинозема и других продуктов в основном определяется его вещественным составом и избыточным содержанием оксида кремния (IV).
Большое влияние на технологические показатели переработки нефелинового сырья оказывает также соотношение в нем щелочных минералов, характеризуемых щелочным модулем n(Na, K)2O/n(Al2O3). Чем меньше щелочной модуль, тем ниже качество сырья, так как оборот щелочи в глиноземном цикле выше. Руды, где это отношение меньше единицы, называют ненасыщенными по щелочи. К этому типу сырья относится кия-шалтырская руда, в кольском нефелиновом концентрате щелочной модуль близок к единице.
В России имеются крупные месторождения нефелиновых пород, представляющих собой практически неограниченную сырьевую базу для алюминиевой и химической промышленности. В настоящее время эксплуатируются месторождения апатито-нефелиновых руд, расположенные в центральной части Кольского полуострова, входящие в состав крупнейшего в мире Хибинского щелочного массива, и месторождения нефелинового сырья в Кия-Шалтырском щелочном массиве, расположенные в северо-восточной части Кузнецкого Алатау. Кольские апатито-нефелиновые руды при переработке на апатитовый концентрат позволяют попутно получать обогащенный нефелиновый концентрат следующего среднего состава, %: Al2O3 – 28,6; SiO2 – 44,0, R2O – 17,8 (в пересчете на Na2O); Na2O – 12,8; K2O – 7,6; Fe2O3 – 3,5; CaO – 1,3. Переработка этого концентрата организована на Пикалевском глиноземном комбинате и Волховском алюминиевом заводе. Кия-шалтырские руды, поступающие в переработку на Ачинский глиноземный комбинат, имеют следующий средний состав, %: Al2O3 – 26,7; SiO2 – 40,2; Fe2O3 – 4,5; CaO – 7,9; R2O – 12,9.
Производство глинозема из нефелинового сырья способом спекания осуществляется по схеме, приведенной на рис.9.
Приготовление известняково-нефелиновой шихты выполняется в несколько этапов. Сначала производится размол известняка на оборотном растворе (различные промывные воды), подаваемом в мельницу вместе со шламом после I и II стадий обескремнивания. Количество вводимой промывной воды определяется влажностью шихты. Известковая пульпа в заданном соотношении смешивается с нефелиновым концентратом и подвергается повторному измельчению в мельнице. После мельниц известняково-нефелиновая шихта поступает в бассейны для усреднения и хранения. Качество шихты определяется такими параметрами, как влажность, известковый и щелочной модули (соответственно 28-29 %; 1,9-2,0 и 1,0-1,05), остаток на сите 0,08 мм не более 8 %.
|
Процесс спекания глиноземсодержащих шихт осуществляется во вращающихся печах. Современные печные агрегаты включают: собственно печь, холодильник, пылегазоочистные сооружения, водовоздушное и газовое хозяйство. В промышленности применяют вращающиеся печи следующих размеров: длина 150 м и диаметр 3,6 м (150 ´ 3,6); длина 185 м и диаметр 5 м (185 ´ 5). Нефелиновая шихта подается в холодный конец печи наливом. Влажная шихта, перемещаясь вдоль печи, сначала подсушивается теплом идущих навстречу ей горячих газов. Для улучшения теплообмена между газами и материалом в холодной части печи подвешены цепи.
Цепи, кроме того, разрыхляют шихту, обеспечивая ее грануляцию при сушке и перемещении. Материал, продвигаясь в печи, нагревается до 1250-1300 °С и затем, пройдя зону спекания, охлаждается до 900-1000 °С. В результате нагрева образуется спек. В общем виде суммарную реакцию спекообразования можно выразить следующим уравнением:
(Na,K)2O×Al2O3×SiO2 + 4CaCO3 =
|
Газы для нагрева материала в печи образуются при сжигании топлива в горячей головке печи. В качестве топлива может быть использован природный газ, мазут или тонкоизмельченный каменный уголь (угольная пыль). Топливо вводится в печь через форсунку. Для сжигания топлива часть воздуха подводится непосредственно к форсунке, часть подается вместе с оборотной пылью, остальная часть – из холодильника.
Газовый поток, двигаясь по печи, поднимает с поверхности слоя материала отдельные частицы (пыль). Крупные частицы оседают в печи, мелкие уносятся за ее пределы. Из общего количества пыли 55-65 % образуется в цепной зоне на участке сушки материала, 10 % – в зоне подогрева и 25-35 % – в зоне кальцинации. Около 50 % от общего количества образовавшейся пыли задерживается в мокрой части цепной зоны. Остальная пыль выносится из печи, улавливается в системе газоочистки (пылевая камера, циклоны, электрофильтр) и с помощью пневмотранспорта подается в бункер на горячей головке печи. Здесь эта пыль используется для «тонкого» регулирования температуры факела.
Окончательное охлаждение спека осуществляется в барабанном или колосниковом холодильнике. Отходящие газы после очистки выбрасываются в атмосферу, а часть их используется для карбонизации алюминатного раствора в содовой и содощелочной ветви.
Качество спека, получаемого на переделе спекания, определяется извлечением Al2O3 и Na2O при стандартном выщелачивании, показатели которого зависят от пористости, фазового и гранулометрического состава. Обычно извлечение Al2O3 и Na2O из нефелинового спека при стандартном выщелачивании составляет 87-89 % при пористости спека 20-40 % и содержании фракции менее 1 мм 20-40 %.
Спек после дробления (до –50 мм) поступает на выщелачивание. Наиболее распространена агитационная схема выщелачивания спека. По этой схеме спек размалывается и выщелачивается в шаровой мельнице оборотным раствором – смесью крепкой промывной воды от промывки шлама и содощелочного раствора. Назначение содощелочного раствора – поддержание заданного каустического модуля алюминатного раствора. В процессе выщелачивания протекают первичные реакции (19)-(22). Одновременно получают развитие вторичные взаимодействия с образованием ГАСН и гидрогранатов кальция:
2Na2SiO3(OH)2 + 2NaAl(OH)4 =
= Na2O×Al2O3×2SiO2×2H2O + 4NaOH; (44)
2Ca(OH)2 + 2NaAl(OH)4 = 3CaO×Al2O3×6H2O + 2NaOH, (45)
3CaO×Al2O3×6H2O + mNa2O×SiO2(OH)2 =
= 3CaO×Al2O3×mSiO2(6 – 2m)H2O + 2mNaOH при m = 0,1¸0,5. (46)
Шлам отделяется от алюминатного раствора сгущением с применением флокулянтов, а сгущенный шлам направляется на 5-7-кратную репульпационную промывку. Обычно в результате выщелачивания получают алюминатный раствор с [Al2O3] = 85¸95 дм3 и aк = 1,5; нефелиновый шлам с содержанием 1,4-1,8 % Na2O и 2,2-2,9 % Al2O3, количество отмываемой щелочи при влажности 40 % составляет 0,15-0,40 % по Na2O.
В алюминатном растворе после выщелачивания содержится 2,5-3,5 г/дм3 SiO2, поэтому он направляется на двухстадийное обескремнивание. Первая стадия осуществляется в автоклавной батарее при 150-170 °С с введением затравки. После отделения шлама, отвечающего по составу гидроалюмосиликату натрия, раствор направляется на вторую стадию обескремнивания. В связи с тем, что в дальнейшем часть раствора (около 50 %) подвергается декомпозиции, при которой раствор не пересыщается кремнием, отпадает необходимость в его глубоком обескремнивании. Вторая стадия обескремнивания проводится в мешалках с добавкой Са(ОН)2 или ГКАК (гидрокарбоалюмината кальция) – 4CaO×Al2O3×xCO2(13 – – 2x)H2O. В результате образуется гидрогранат кальция, имеющий низкую растворимость. Ввиду небольшого количества шлама, образующегося на второй стадии обескремнивания (около 100 кг на 1 т Al2O3), он не подвергается регенерации Al2O3, а направляется в качестве затравки на автоклавное обескремнивание.
Химизм первой стадии обескремнивания соответствует реакции (44), а второй, при использовании известкового молока, – реакциям (45) и (46) при m = 0,1-0,2 (рис.10). Более эффективным представляется использование на второй стадии обескремнивания технологии, разработанной профессором СПГГИ В.М.Сизяковым, с использованием синтетической обескремнивающей добавки – твердого раствора СО2 в 4CaO×Al2O3×13H2О. Ее введение обеспечивает гомогенный механизм взаимодействия с алюминатным раствором, высокую скорость и полноту осаждения кремния с расходом СаО, близким к стехиометрии реакций: при x = 1
4CaO×Al2O3×CO2×11H2O + 2OH– =
= 4Ca2+ + 2Al(OH)–4 + CO32– + 3OH– + 5H2О. (47)
Затем из раствора кристаллизуется гидрогранат кальция:
3Ca2+ + 2Al(OH)–4 + mH2SiO42– + (4 – 2m)OH– =
= 3CaO×Al2O3×mSiO2(6 – 2m)H2O + 2mH2O. (48)
|
В результате реакции (44) кремневый модуль алюминатного раствора повышается с 30 до 400, а в результате реакций (45), (48) – с 400 до 1000-10000.
Гидроксид алюминия выделяется в двух ветвях: содощелочной и содовой. В содовой ветви алюминатный раствор карбонизируется до остаточного содержания Al2O3 1-3 г/дм3; после отделения гидроксида алюминия от раствора он направляется в качестве затравки в карбонизаторы содощелочной ветви, а раствор – на выделение из него соды и поташа.
В содощелочной ветви раствор сначала продувается очищенным газом печей спекания, содержащим 12-15 % СО2, до [Na2Oy] = 40 г/дм3. Затем, после введения дополнительной затравки, разлагается в декомпозерах до aк = 2,8¸3,0. Пульпа разделяется в сгустителе; раствор направляется на выщелачивание, а гидроксид алюминия – на промывку. Остаточная влажность гидроксида алюминия после окончательной фильтрации 15-18 %.
Промытый гидроксид алюминия подвергается кальцинации (см. лабораторную работу 2).
Подготовка к работе
Лабораторное оборудование аналогично используемому в работах 1 и 2. Отличие заключается в использовании высокотемпературной печи с силитовыми нагревателями, на стадии спекания обеспечивающей нагрев шихты до 1250 °С.
Автоклавное обескремнивание выполняется с применением соответствующей лабораторной установки (см. лабораторную работу 1).
Задание на выполнение экспериментальной части включает исчерпывающие данные по составам используемого сырья и материалов, технологические режимы всех моделируемых операций (см. лабораторную работу 2).
Ход работы
1. Выполнить расчет сухой шихты, состоящей из нефелинового концентрата, известняка и соды, удовлетворяющей следующим соотношениям:
 ; (49)
; (49)
 ; (50)
; (50)
mнеф + mизв + mс = mш, (51)
где  ,
,  ,
,  ,
,  – число молей компонентов в пробе нефелинового концентрата (R – Na, K);
– число молей компонентов в пробе нефелинового концентрата (R – Na, K);  ,
,  – число молей СаО и SiO2 в навеске известняка;
– число молей СаО и SiO2 в навеске известняка;  – число молей Na2О в навеске соды; mнеф, mизв, mс и mш – соответственно количество нефелинового концентрата, известняка, соды и шихты.
– число молей Na2О в навеске соды; mнеф, mизв, mс и mш – соответственно количество нефелинового концентрата, известняка, соды и шихты.
При заданном количестве шихты mш необходимо совместное решение уравнений (49)-(51), а при шихтовке на известное количество концентрата возможно последовательное определение количества соды, известняка и в конечном итоге – шихты.
При определении числа молей R2O удобно воспользоваться средневзвешенной молекулярной массой суммы Na2O и K2O в нефелиновом концентрате MR2O в граммах на моль, вычисленной по формуле
 , (52)
, (52)
где Nн и Kн – содержание Na2O и K2O в нефелиновом концентрате, %; 62 и 94 – молекулярные массы Na2O и K2O, г/моль.
2. Взвесить расчетные количества концентрата (рекомендуется 20-30 г), известняка и соды. Компоненты смешать в фарфоровой ступке и усреднить состав. При необходимости шихту дополнительно измельчить и засыпать в алундовый тигель, установить в печь, предварительно разогретую до 1000-1050 °С, при которой исключается получение расплава первично образующихся силикатов (Na2O×3CaO×6SiO2, 2NaO×CaO×3SiO2, Na2O×2CaO×3SiO2), но обеспечивается образование алюминатов натрия и ортосиликата кальция.
3. Произвести изотермическую выдержку в течение 30 мин при температуре 1000 °С, а затем для завершения реакций разогреть печь до 1250 °С и выдержать шихту при этой температуре 15-20 мин. Затем снизить нагрузку на нагреватели до допустимого значения. С соблюдением правил высокотемпературных работ достать тигель из печи и обеспечить его безопасное охлаждение.
4. Спек взвесить (mсп), результат записать в отчет. Описать физические изменения, произошедшие с шихтой. Измельчить спек до крупности менее 1 мм по ситовому анализу. Выполнить стандартное выщелачивание спека при Ж:Т = 4:1. Для этого приготовить раствор следующего состава: [Na2Oк] = 25 г/дм3 и [Na2Oу] = 5 г/дм3. Необходимый объем в кубических дециметрах
 , (53)
, (53)
где r – плотность раствора, равная 1,05 кг/дм3.
Раствор разогреть при перемешивании до 75 °С, внести спек и выщелачивать 15 мин. Затем пульпу отфильтровать, крепкий алюминатный раствор слить из колбы Бунзена и замерить его объем Vал. Оставшийся на фильтре шлам промыть четырехкратным объемом горячей воды (т.е. 4Vал). Промытый шлам перенести в фарфоровую чашку, просушить и взвесить, полученный результат (mшл) занести в отчет. Объем промывной воды измерить (Vпв).
5. Оценить ожидаемые концентрации Na2Oк и A2O3 в алюминатном растворе и промывной воде (см. лабораторную работу 1). В соответствии с полученными результатами отобрать пробы растворов и выполнить их разбавление, обеспечивающее в последующем отбор аликвотной части для анализа объемом 10-20 мл. Разбавление рассчитать по уравнениям (11) и (12). Тогда объем пробы Vп = Vк/n (где Vк = 100¸250 мл), с округлением до стандартных объемов пипеток.
Ожидаемая концентрация SiO2 в алюминатном растворе в граммах на литр или миллиграммах на миллилитр может быть вычислена с учетом известных на практике кремневых модулей
 , (54)
, (54)
где mSi = 30.
При фотоколориметрическом анализе рекомендуется отбирать примерно 0,25 мг SiO2, что обеспечивает максимальную точность определения. В соответствии с этим объем аликвоты в миллилитрах
 , (55)
, (55)
где n¢ – реальное разбавление с учетом выбранного объема пипетки.
6. По указанию преподавателя подготовить необходимое число лабораторных автоклавов для моделирования (снятия кинетики) первой стадии обескремнивания. Для этого залить в автоклав 30-40 мл алюминатного раствора и репульпировать в этом объеме механоактивированный на виброистирателе нефелиновый концентрат до Ж:Т = 3:1. Концентрат выполняет в данном случае роль затравки. Плотность алюминатного раствора в граммах на литр можно приближенно определить по уравнению
 , (56)
, (56)
где rп – плотность раствора NaOH с концентрацией Na2O, равной концентрации Na2Oобщ в алюминатном растворе; А и Ny – концентрации Al2O3 и Na2Oy, г/л.
Масса активированной затравки в граммах с учетом (56)
 . (57)
. (57)
7. Автоклавы собрать и установить в воздушный термостат, предварительно разогретый до 150-170 °С. Включить перемешивание и произвести необходимую изотермическую выдержку каждого автоклава. При снятии кинетики обескремнивания рекомендуемое время выдержки 30, 60, 90 мин, а последовательность работы с ними – по п.6 лабораторной работы 1.
8. Охлажденный до комнатной температуры автоклав разобрать под наблюдением преподавателя и отфильтровать пульпу на вакуум-установке. От полученного фильтрата обескремненного алюминатного раствора отобрать пробу для разбавления и последующего определения SiO2, предполагая изменение  при автоклавной выдержке от 30 до 400 (см. п.5).
при автоклавной выдержке от 30 до 400 (см. п.5).
9. Выполнить химические анализы на содержание Na2Oк и Al2O3 в алюминатном растворе и промывной воде, на содержание SiO2 в алюминатном растворе до и после автоклавного обескремнивания.
10. Рассчитать извлечение Al2O3 в процентах из нефелинового концентрата в раствор
 ,
,
где [Al2O3]ал и [Al2O3]пв – концентрация Al2O3 в алюминатном растворе и промывной воде, г/л; Анеф – содержание Al2O3 в нефелиновом концентрате, %.
Каустический модуль алюминатного раствора и промывной воды вычислить по формуле (1), кремневый модуль алюминатного раствора до и после обескремнивания – по уравнению
mSi = [Al2O3]/[SiO2]. (58)
При снятии кинетики обескремнивания построить зависимость mSi = f(t).
Определить удельные материальные потоки технологии на 1 т нефелинового концентрата для известняка, соды, шихты, спека, алюминатного раствора по аналогии с уравнениями (15).
11. Проанализировать и объяснить полученные результаты.
Работа 4. ВСКРЫТИЕ АЛУНИТОВОЙ ПОРОДЫ
ПРИ КОМПЛЕКСНОЙ ПЕРЕРАБОТКЕ ОБЖИГОВО-ВОССТАНОВИТЕЛЬНЫМ СПОСОБОМ
Цель работы – знакомство с теоретическими основами и контурами технологии комплексной переработки алунитов на основе экспериментального исследования их вскрываемости.
Основные определения, теория и технология
Алунитовые руды представляют собой горные породы с содержанием минерала алунита 25-70 %, остальное – в основном кварц, в меньшей степени каолинит, оксиды железа и др. Алунит – это двойной основной сульфат алюминия и калия с теоретической формулой K2SO4×Al2(SO4)3×2Al2O3×6H2O. Небольшое количество калия в природных алунитах изоморфно замещено натрием. Химический состав калиевого алунита следующий, %: Al2O3 – 37; SO3 – 38,6; K2О – 11,4; Н2О – 13,0. Алунитовую руду долгое время использовали только как сырье для производства квасцов. С 70-х годов XX столетия ее стали применять в качестве комплексного сырья для производства глинозема, серной кислоты, сульфата калия, серно-кислого алюминия, квасцов, пятиокиси ванадия и некоторых других продуктов.
|
K2SO4×Al2(SO4)3×2Al2O3×6H2O ® K2SO4×Al2(SO4)3 + 2Al2O3 +
|
При температуре обжига алунита выше 650 °С активная, легко растворимая в щелочах и кислотах модификация g-Al2O3 постепенно переходит в пассивную малорастворимую форму a-Al2O3. Если обжиг проводить в восстановительной атмосфере, то температура начала диссоциации сульфата алюминия снижается до 500-600 °С, т.е. до такой температуры, при которой глинозем от термического разложения алунита будет находиться в активной g-форме. При использовании в качестве восстановителя твердого углерода или водорода процесс восстановительного обжига предварительно дегидратированного при 480-520 °С алунита может быть описан следующим общим уравнением:
K2SO4×Al2(SO4)3 + 2Al2O3 + 1,5С(3Н2) =
= K2SO4 + 3Al2O3 + 3SO2 + 1,5СО2(3Н2О). (60)
Для снижения температуры этого процесса необходимо пользоваться газообразным или парообразующим восстановителем: нефтепродуктами, соляровым маслом, конверсированным природным газом, парообразной серой и др.
Восстановительный способ комплексной переработки алунитов разработан в ВАМИ под руководством Г.В.Лабутина. Он освоен в промышленности применительно к заглинским алунитовым рудам на Кировобадском алюминиевом заводе (Азербайджан).
По этому способу (рис.11) исходную алунитовую руду дробят и подвергают сухому размолу. Затем измельченная руда пневмотранспортом подается в печь кипящего слоя для окислительного обжига, целью которого является максимальная степень дегидратации алунита при 490-520 °С по схеме (59). Потери SO2 в этом процессе составляют 5-10 %.
Дегидратированная руда поступает во второй аппарат кипящего слоя, где подвергается восстановительному обжигу до достижения максимальной степени разложения сульфата алюминия и отгонки SO2 (на 85-90 %) при сохранении высокой активности g-Al2O3 по уравнению (60). Газ из восстановительного аппарата поступает на получение серной кислоты обычным контактным способом, а восстановленный алунит (глиноземистый концентрат) – на переработку по способу Байера.
|
Операцию предварительного нагрева и дегидратации порошкового алунита отделяют от операции восстановления с целью получения отходящих газов восстановительных печей с высокой концентрацией SO2. В этом случае дымовые газы и водяные пары от дегидратации не разбавляют продукты восстановления и передел получения серной кислоты значительно упрощается. Для эффективного обжига и восстановления алунитовой руды наиболее приемлемы печи кипящего слоя, так как в результате реакций дегидратации алунита и разложения сульфата алюминия происходит значительное паро- и газообразование, что обеспечивает самокипение порошка руды и облегчает осуществление этих процессов в большом масштабе.
Восстановленную алунитовую руду выщелачивают оборотным алюминатным раствором с [Na2Oк] = 100¸120 г/л при температуре 80-90 °С в течение 30-60 мин. В этих условиях в раствор извлекается 83-90 % Al2O3 от содержания в восстановленном продукте. Шлам отделяют и промывают в сгустителях (аналогично красному шламу); алюминатный раствор обескремнивают при 102-105 °С в течение 3-4 ч в присутствии затравки белого шлама и подвергают декомпозиции. При выпарке маточного раствора выделяется основная масса сульфатов калия и натрия.
В восстановительном способе теряется много едкой щелочи из-за образования сульфатов, алюмосиликата натрия и неполноты отмывки шламов. Для возмещения ее потерь предусмотрена ветвь восстановительного спекания смеси Al(OH)3 с углем и сульфатами:
R2SO4 + 2Al(OH)3 + C = R2O×Al2O3 + 3H2O + CO + SO2, (61)
где R – Na, K.
При выщелачивании спека значительная часть Al2O3 остается в нерастворимом остатке и после фильтрации возвращается в процесс. Алюминатный раствор от выщелачивания спека смешивают с основным потоком и направляют на обескремнивание. Образующийся при спекании разбавленный сернистый газ выбрасывают в атмосферу или смешивают с богатым газом от восстановительного обжига алунита.
Подготовка к работе
Лабораторное оборудование должно обеспечивать возможность моделирования всех шихтоподготовительных операций с твердыми материалами, двухстадийный обжиг, выщелачивание глиноземсодержащего огарка щелочными растворами, фильтрацию и промывку шламов, а также химический анализ растворов. В целом применяемое оборудование идентично используемому в лабораторных работах 1 и 2. Исключение составляют обжиговые печи, которые могут быть рассчитаны на более низкую температуру. Обязательным условием их работы является удаление образующихся газов, содержащих SO2, в вентиляционную систему.
Задание на выполнение экспериментальной части включает исчерпывающие сведения о составах используемых материалов, технологические режимы пиро- и гидрометаллургических операций, требования к текущему контролю процессов и выполнению химических анализов.
Ход работы
1. Измельчить исходные материалы: алунит, древесный или активированный уголь, серу.
2. Подготовить навеску алунитовой руды (mал), содержащую около 10 г Al2O3. Массу навески занести в отчет. Пробу загрузить в алундовый или шамотный тигель и установить в печь с температурой 500-520 °С для дегитратирующего обжига на 20-30 мин. По окончании выдержки пробу охладить и взвесить (mог).
3. Полученный огарок mог разделить на две примерно одинаковые по массе пробы (  и
и  ) и зашихтовать их с восстановителем (уголь и элементарная сера).
) и зашихтовать их с восстановителем (уголь и элементарная сера).
Количество угля в граммах может быть рассчитано по уравнению (60). С учетом избытка от стехиометрии 25 %
 , (62)
, (62)
где Аал – содержание Al2O3 в пробе алунита, %.
Количество серы в граммах для восстановления второй пробы может быть рассчитано при условии восстановления S6+ до S4+ и окисления элементарной серы до S4+. С учетом избытка от стехиометрии 25 %
 . (63)
. (63)
Смешать восстановители с соответствующими навесками дегидратированного алунита. Тщательно усреднить шихту при дополнительном истирании в фарфоровой ступке, загрузить в тигли и установить их в печь, предварительно разогретую до 580-600 °С. Провести восстановительный обжиг в течение 20-30 мин. По окончании пробы восстановленного материала охладить и взвесить ( 
 ).
).
4. Рассчитать количество каустика для выщелачивания полученных проб. Без учета затрат щелочи на образование ГАСН и гидролиз невосстановленного сульфата алюминия количество щелочи будет определяться только значением каустического модуля в граммах, необходимого для получения устойчивых алюминатных растворов по реакции (2):
 , (64)
, (64)
где  – масса Na2O, необходимая для выщелачивания первой и второй пробы;
– масса Na2O, необходимая для выщелачивания первой и второй пробы; 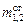 – навески первой и второй пробы дегидратированного алунита; aк принимаем, как в способе Байера, 1,7.
– навески первой и второй пробы дегидратированного алунита; aк принимаем, как в способе Байера, 1,7.
Тогда количество каустика в граммах для первой и второй пробы
 . (65)
. (65)
Объем щелочного раствора и объем воды для его приготовления рассчитать по уравнениям (8) и (8а) для [Na2Oк] = 100¸120 г/л.
5. Провести выщелачивание проб восстановленного алунита в автоклавных или атмосферных условиях по указанию преподавателя (см. методики лабораторных работ 1 и 2). Продолжительность выщелачивания 30-60 мин. Температура автоклавного выщелачивания 150-170 °С, атмосферного – 95-100 °С.
6. По окончании выщелачивания выполнить необходимые действия по п.7, 8 лабораторной работы 1. Пульпу перед фильтрацией разбавить горячей водой в 3-4 раза.
7. Приготовить разбавленные пробы и провести их анализ на содержание Na2Ообщ, Na2Ок и Al2O3 по п. 9-11 лабораторной работы 1.
8. Рассчитать практическое извлечение Al2O3 в раствор в процентах из первой и второй пробы восстановленного алунита
 ; (66)
; (66)
каустические модули полученных алюминатных растворов – по формуле (1). Степень десульфуризации алунита (  ) в процентах по данным о количестве общей щелочи, связанной в сульфат, в граммах
) в процентах по данным о количестве общей щелочи, связанной в сульфат, в граммах
 ; (67)
; (67)
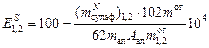 . (68)
. (68)
9. Проанализировать и объяснить результаты экспериментов.
Работа 5. ОСАЖДЕНИЕ ЛИТИЯ В ЩЕЛОЧНЫХ
АЛЮМИНАТНЫХ РАСТВОРАХ
Цель работы – исследование возможности осаждения алюминатов лития в производстве глинозема на основе математического планирования экспериментов.
Основные определения, теория и технология
Литий – типичный литофильный элемент, широко распространенный в земной коре (его содержание по массе 6,5×10–3 %). Элемент преимущественно концентрируется в кислых изверженных (граниты, липариты) и осадочных (глины и сланцы) породах. Кроме того, литий содержится в почвах, соляных рассолах, морской воде, углях, растительных и животных организмах. Известно около 150 минералов, содержащих литий. Большей частью это силикаты или фосфаты.
Один из наиболее распространенных способов переработки литиевых концентратов (сподумена и лепидолита) заключается в их спекании с известью или мелом. При этом в интервале температур 1150-1200 °С со сподуменом, например, протекает следующая реакция:
Li2O×Al2O3×4SiO2 + 8CaO = Li2O×Al2O3 + 4(2CaO×SiO2).
При выщелачивании спека водой в присутствии избытка извести литий переходит в раствор:
Li2O×Al2O3 + Ca(OH)2 = 2LiOH + CaO×Al2O3,
с последующей вакуум-кристаллизацией LiOH×H2O.
Сульфатные методы основаны на обработке минералов сульфатсодержащими реагентами (серной кислотой, сульфатами щелочных металлов), сопровождающейся протеканием следующих процессов (например, для сподумена):
|
|
Li2O×Al2O3×4SiO2 + K2SO4(Na2SO4) ® K2O(Na2O)×Al2O3×4SiO2 + Li2SO4.
Сульфат лития хорошо растворим в воде, поэтому, выщелачивая продукты спекания водой, можно отделить литий от основной массы алюминия и кремния.
Применение лития в металлургии основано, прежде всего, на легком сплавлении почти со всеми металлами. Наиболее перспективны сплавы с магнием и сверхлегкие сплавы с бериллием, обладающие плотностью 1-1,5 кг/дм3. Обычно добавка 1-2 % лития улучшает свойства основы, сообщая сплаву твердость или вязкость. Литий как легирующий компонент многочисленных алюминиевых сплавов снижает их плотность, повышает удельную (объемную) прочность как при обычной, так и при повышенной температуре.
Гидриды лития используют в качестве портативных источников водорода. Растворы гидроксида добавляют к электролиту щелочных аккумуляторов для увеличения их емкости. Гидроксид лития также является основой при производстве морозо- и термостойких смазок.
Керамическая и стекольная промышленность широко использует природные и синтетические литийсодержащие материалы для создания сверхтермостойких керамических покрытий, эмалей с низкой температурой плавления, специальных сортов стекол с повышенной прочностью и проницаемостью ультрафиолетовых лучей, высоким сопротивлением к действию атмосферы и расстекловыванию.
Металлоорганические соединения лития используются в качестве катализаторов при производстве пластических масс и каучуков.
Металлический литий в жидком состоянии (область температур 180-1336 °С) применяется в качестве теплоносителя в урановых реакторах. В атомной технике литий используют для получения тяжелого изотопа водорода – трития, являющегося необходимым компонентов в высокоэнергетических реакциях термоядерного синтеза.
Чрезвычайно перспективно применение соединений лития при электролизе глинозема в расплаве криолита. Введение в электролит 5 % LiF снижает его электрическое сопротивление при 960 °С с 0,42 до 0,38 Ом×см, плотность – с 2,15 до 2,11 т/м3 и вязкость. В результате этого рабочая температура процесса может быть снижена с 965-970 до 930-935 °С, что приводит к уменьшению расхода фторсолей на 50 %, анодной массы – на 5-10 %, повышению выхода по току на 3-5 % и снижению себестоимости на 15 %. В настоящее время перевод алюминиевых электролизеров на работу с литийсодержащим электролитом – практически единственный способ интенсификации действующего производства.
При корректировке состава электролита алюминиевых электролизеров по литию применяют Li2CO3, LiF, Li2O×2Al2O3, 3LiF×AlF3. Для лучшего распределения лития по объему электролизной ванны рекомендуется вводить эти соединения в смеси с глиноземом. Более эффективно использование литийсодержащего глинозема, получаемого совместным осаждением лития и алюминия из щелочных алюминатных растворов на основе низкой растворимости алюминатов лития:
Li2СO3 + 2Na2O×Al2O3 + H2O ® Li2O×2Al2O3 + Na2CO3 + 2NaOH.
Для осаждения алюминатов лития из щелочных растворов могут быть использованы также гидроксид, сульфат или хлорид лития. Диалюминат лития кристаллизуется в форме многоводных кристаллогидратов Li2O×2Al2O3×nH2O, растворимость которых в алюминатных щелочных растворах значительно зависит от температуры, каустического модуля, концентрации и состава. Эта зависимость позволяет совместно перерабатывать алюминийсодержащее и литиевое сырье, направляя последнее на передел вскрытия в способе Байера или спекания с осаждением литийсодержащего глинозема при декомпозиции или карбонизации растворов. При этом содержание лития в глиноземе определяется количеством подаваемого литийсодержащего сырья.
Растворимость диалюмината лития в щелочных растворах является функцией многих переменных, поэтому ее удобно представлять в аналитическом виде. Рациональное построение математической модели проводится на основе планирования экспериментов, позволяющего минимизировать число опытов за счет потери части малозначащей информации. При линейных связях такой информацией может быть зависимость параметра y от совместного влияния факторов х1, х2, …, хi, когда влияние одного из факторов зависит от уровня, на котором находится другой.
Например, для полного факторного эксперимента (ПФЭ) с участием факторов х1 и х2, осуществляемого при двух значениях (уровнях) каждого из них (уровни обозначены +1 и –1), можно составить матрицу планирования, приведенную в табл.5. Символическое обозначение такой матрицы 22, где основание степени – это число уровней факторов, а показатель степени – число факторов.
Таблица 5
Матрица планирования полного факторного эксперимента 22
| Номер опыта | хо | х1 | х2 | х1х2 | уi |
| + | - | - | + | у1 | |
| + | + | - | - | у2 | |
| + | - | + | - | у3 | |
| + | + | + | + | у4 |
Пользуясь такой матрицей, можно вычислить четыре коэффициента и представить результаты эксперимента в виде неполного квадратного уравнения
у = b0 + b1x1 + b2x2 + b12x1x2. (69)
Если имеются основания считать, что в выбранных интервалах варьирования процесс может быть описан линейной моделью, то достаточно определить три коэффициента: b0, b1 и b2. Остается одна степень свободы, которую можно употребить для минимизации числа опытов. При линейном приближении b12 ® 0 и вектор-столбец х1х2 можно использовать для нового фактора х3. В этом случае коэффициенты линейного уравнения будут являться смешанной оценкой влияния отдельного фактора и эффекта его взаимодействия:
b1 ® b1 + b23; b2 ® b2 + b13; b3 ® b3 + b12,
где b1 » b1; b2 » b; b3 » b3.
Если эффекты парного взаимодействия незначимы, то имеется возможность создать линейную модель на основании меньшего числа опытов. Для обозначения дробных реплик полного факторного эксперимента, в которых р линейных эффектов приравнены в эффектам взаимодействия, удобно пользоваться условным обозначением 2k – р, где k – общее число факторов. Матрица планирования табл.5 при замене х1х2 на х3 получит обозначение 23 – 1 и будет являться полурепликой от полного факторного эксперимента для трех факторов с числом опытов 8.
При построении полуреплики 23 – 1 существует всего две возможности: приравнять х3 к +х1х2 или к –х1х2, поэтому есть только две полуреплики 23 – 1 (табл.6).
Таблица 6
Две полуреплики 23-1от ПФЭ 23
| х3 = +х1х2 | х3 = –х1х2 | ||||||||
| Номер опыта | х1 | х2 | х3 | х1х2х3 | Номер опыта | х1 | х2 | х3 | х1х2х3 |
| + | + | + | + | + | + | - | - | ||
| - | - | + | + | - | - | - | - | ||
| + | - | - | + | + | - | + | - | ||
| - | + | - | + | - | + | + | - |
Создание линейной математической модели исследуемого процесса заключается в расчете коэффициентов уравнения регрессии типа
y = b0 + b1x1 + b2x2 + b3x3 + … + bkxk , (70)
установлении значимости полученных коэффициентов и проверке адекватности модели реальному процессу с определенным уровнем точности. Для любого числа факторов коэффициенты линейных членов уравнения регрессии будут вычисляться по полученной с использованием метода наименьших квадратов (МНК) формуле
 (71)
(71)
где Yi – значение параметра для i-го опыта (в i-й строке матрицы планирования); Xji – значение j-го фактора в i-м опыте (в i-й строке матрицы планирования); j = 0, 1, 2, …, k – номер фактора; N – число опытов в матрице планирования.
Тогда расчет отдельных коэффициентов будет выполняться по формулам
 ;
;  и т.д. (72)
и т.д. (72)
Поскольку каждый фактор, кроме х0, варьируется на двух уровнях +1 и –1, вычисления сводятся к приписыванию столбцу y знаков, соответствующих фактору столбца, и алгебраическому сложению полученных значений.
Проверка значимости коэффициентов проводится построением доверительного интервала
Dbj = ±tS{bj} , (73)
где t – табличное значение критерия Стьюдента при выбранном уровне значимости f1 и числе степеней свободы f2 = n – 1, с которым определялась дисперсия функции S2{y}; S{bj} – квадратичная ошибка коэффициента регрессии, S{bj} =  .
.
Дисперсия коэффициента регрессии
 , (74)
, (74)
где S2(y) – дисперсия параметра (дисперсия воспроизводимости), определяемая проведением параллельных опытов на нулевом уровне факторов, а затем рассчитываемая по формуле
 , (75)
, (75)
где n – число параллельных опытов;  – среднее значение функции в этих опытах; уq – текущее значение функции.
– среднее значение функции в этих опытах; уq – текущее значение функции.
Допустим, в нашем эксперименте ошибка трех параллельных опытов, выполненных на нулевом уровне, равна 2 % от  , тогда
, тогда
 .
.
Для трех параллельных опытов значение критерия Стьюдента при 5-процентном уровне значимости t = 4,303, тогда при N = 4
 ,
,
т.е. доверительный интервал составляет примерно 5 % от среднего значения найденной функции. Если абсолютное значение коэффициента больше, чем доверительный интервал, то коэффициент значим; в противном случае его надо исключить из уравнения регрессии, а оставшиеся коэффициенты рассчитать заново.
Проверка адекватности проводится с целью оценки пригодности полученной модели для описания реального процесса и заключается в расчете F-критерия Фишера и его сравнении с табличным значением при заданном числе степеней свободы и уровне значимости. Расчет F-критерия Фишера выполняется по формуле
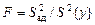 , (76)
, (76)
где  – дисперсия адекватности, равная остаточной сумме квадратов, деленной на число степеней свободы.
– дисперсия адекватности, равная остаточной сумме квадратов, деленной на число степеней свободы.
Дисперсия
 , (77)
, (77)
где f1 – число степеней свободы, вычисляемое как разность между числом опытов в матрице планирования и числом независимых коэффициентов, вычисленных по результатам этих опытов;  – экспериментальное значение параметра (функции) в i-й строке матрицы;
– экспериментальное значение параметра (функции) в i-й строке матрицы;  – значение функции, предсказанное по уравнению.
– значение функции, предсказанное по уравнению.
Модель адекватна, если значение F-критерия, вычисленное по формуле (76), меньше табличного значения.
Значения критерия Фишера при 5-процентном уровне значимости отыскиваются по табл.7 на пересечении столбцов, связанных с числом степеней свободы дисперсии адекватности f1, и строк, связанных с числом степеней свободы дисперсии функции f2 при вычислении воспроизводимости  .
.
При отсутствии степеней свободы, необходимых для проверки адекватности по F-критерию, оценка точности модели может быть выполнена путем расчета средней квадратичной ошибки по формуле
 . (78)
. (78)
Таблица 7
Распределение F-критерия Фишера при 5-процентном уровне значимости
| f2 | f1 | ||||
| 164,4 | 199,5 | 215,7 | 224,6 | 230,2 | |
| 18,5 | 19,2 | 19,2 | 19,3 | 19,3 | |
| 10,1 | 9,6 | 9,3 | 9,1 | 9,0 | |
| 7,7 | 6,9 | 6,6 | 6,4 | 6,3 | |
| 6,6 | 5,8 | 5,4 | 5,2 | 5,1 |
Подготовка к работе
Лабораторное оборудование включает фарфоровые или стеклянные реакторы (стаканы), снабженные механическим перемешивающим устройством и оборудованные системой электрообогрева и автоматического поддержания температуры.
Для фильтрации и промывки диалюмината лития удобно использовать вакуум-фильтровальные установки. Удаление кристаллогидратной влаги проводится прокаливанием в электропечах при температуре до 800 °С. Все операции по приготовлению растворов, связанные с измерением объемов и взвешиванием, проводятся на соответствующем лабораторном оборудовании, обеспечивающем необходимую точность работ.
Задание на выполнение экспериментальной части включает характеристику исследуемых факторов:
· каустический модуль растворов;
· концентрация;
· температура процесса;
· продолжительность осаждения;
· дозировка Li2O.
При этом задается нулевой уровень фактора и интервал варьирования. Необходимо обратить внимание на методики анализов и обработки экспериментальных данных.
Ход работы
1. Синтезировать исходный алюминатный раствор с aк = 1,6, устойчивый при комнатной температуре. При приготовление этого раствора прямым растворением гидроксида алюминия каустиком образуется пересыщенный по алюминату натрия раствор, в котором происходит кристаллизация. В связи с этим сначала готовят более разбавленные растворы с заданным значением aк, а затем упаркой переводят его в область необходимых концентраций.
Согласно диаграмме растворимости в системе Na2O-Al2O3-H2O устойчивыми при комнатной температуре будут растворы с aк = 1,6 при [Na2Oк] = 22 %. Для приготовления заданного количества алюминатного раствора (mр) потребуется в граммах: чистого оксида натрия
0,22mр;
чистого оксида алюминия
 .
.
При внесении Al2O3 с техническим гидратом
 ,
,
где Wгидр – влажность технического гидрата в долях единицы.
Для растворения гидрата 30-процентным раствором Na2Oк потребуется в граммах гидроксида натрия заданной марки (каустика) и воды

и
 ,
,
где [NaOH]к – содержание чистого гидроксида в используемой марке реактива, доли ед.
С учетом H2O, вносимой каустиком (свободной и связанной), для приготовления 30-процентного раствора потребуется воды
 ,
,
где Wк – влажность используемой марки каустика, доли ед.
Тогда масса раствора, образующегося при растворении технического гидрата алюминия 30-процентным щелочным раствором,
m¢p = mт.гидр + mк + mв
и для получения раствора заданной концентрации подлежит упарке следующее количество воды: m¢p – mр.
Расчетное количество каустика осторожно (порциями) при перемешивании вносить в отмеренный объем воды, не допуская закипания.
Приготовленный щелочной раствор разогреть до 90-95 °С и при интенсивном перемешивании (порциями) вносить в него гидрат алюминия по мере растворения. Контр


