 |
|
Теоретическое введение
Для объяснения зависимости теплоемкости твердых тел от температуры (модели Эйнштейна, Дебая) используется модель кристалла, в которой принимается, что отклонения атомов, ионов (частиц, из которых состоит кристалл) из положения равновесия малы по сравнению с расстояниями между ними. Предполагается, что можно точно определить свойства твердого тела, сохраняя в разложении потенциальной энергии кристалла лишь первый неисчезающий член, квадратичный по смещениям атомов. Это – так называемое гармоническое приближение. Предположение о малости колебаний кажется разумным для большинства твердых тел при температурах, лежащих гораздо ниже температуры плавления. Может показаться, что в том случае, когда выполняется предположение о малых колебаниях атомов кристалла, поправки к гармоническому приближению важны лишь в очень точных вычислениях.
Тем не менее ряд свойств твердых тел, проявляющихся при любой температуре, не удается объяснить в чисто гармоническом приближении, поскольку они полностью обусловлены высшими (ангармоническими) членами в разложении энергии взаимодействия атомов вблизи ее равновесного значения. Важнейшее из этих физических свойств – эффект теплового расширения. У строго гармонического кристалла равновесные размеры не зависели бы от температуры.
Для кристаллов с кубической симметрией коэффициент теплового расширения определяется так:

 . (14.1)
. (14.1)
Здесь l – линейные размеры тела, V – его объем. Индекс «P» означает, что производная берется при постоянном давлении.
При свободном тепловом расширении твердого тела тепловая деформация ε (относительное изменение линейных размеров) будет пропорциональна изменению температуры DT:
 . (14.2)
. (14.2)
Как правило, с повышением температуры размеры твердых тел увеличиваются, т.е. α>0. Явление теплового расширения в твердых телах обусловлено некоторым изменением характера межатомного взаимодействия при изменении температуры. С усилением теплового движения, с увеличением температуры, с ростом амплитуды колебаний атомов твердого тела силы притяжения и отталкивания между ними, определяющие их энергию взаимодействия, различным образом меняются. И это приводит к тому, что среднее расстояние между атомами в твердом теле изменяется при изменении температуры.
Поясним на простой модели линейной цепочки атомов причины теплового расширения. Для этого рассмотрим влияние ангармонического вклада в выражении для потенциальной энергии взаимодействия пар атомов при температуре T. Потенциальную энергию взаимодействия атомов при смещении на расстояние x от положения равновесия x0 представим в виде:
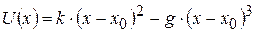 . (14.3)
. (14.3)
Здесь k – квазиупругая постоянная, g – ангармоническая постоянная; первое слагаемое – потенциальная энергия в гармоническом приближении, второе слагаемое – ангармонический вклад в потенциальную энергию. Он определяет асимметрию взаимного отталкивания атомов. В отсутствие ангармонизма (g=0) на атомы действует только квазиупругая сила – зависимость U(x) описывается параболой. Из (14.3) находим по определению (  ) возвращающую силу, действующую на атом:
) возвращающую силу, действующую на атом:
 . (14.4)
. (14.4)
Среднее по времени значение силы 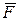 (это сила, действующая на атом в состоянии равновесия) должно быть равно нулю, иначе атомы в среднем обладали бы ускорением и сместились из положения равновесия. Так что:
(это сила, действующая на атом в состоянии равновесия) должно быть равно нулю, иначе атомы в среднем обладали бы ускорением и сместились из положения равновесия. Так что:
 . (14.5)
. (14.5)
Укажем, что, во-первых, по определению (14.2)  , и что в гармоническом приближении (g=0) из (14.5) следует
, и что в гармоническом приближении (g=0) из (14.5) следует  , и теплового расширения нет. Этот результат не зависит от амплитуды колебаний атомов. Атомы колеблются гармонически, и в среднем их позиции в кристаллической решётке не зависят от температуры.
, и теплового расширения нет. Этот результат не зависит от амплитуды колебаний атомов. Атомы колеблются гармонически, и в среднем их позиции в кристаллической решётке не зависят от температуры.
Из соотношения (14.5) следует также, что с учётом ангармонизма:
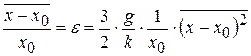 . (14.6)
. (14.6)
Для нахождения величины 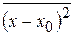 можно при высоких температурах воспользоваться классическим законом распределения энергии по степеням свободы:
можно при высоких температурах воспользоваться классическим законом распределения энергии по степеням свободы:
 , (14.7)
, (14.7)
где kБ – постоянная Больцмана.
Сравнивая (14.6) и (14.2) с учётом (14.7) находим, что для линейной цепочки атомов  , так что отклонения атомов от положения равновесия
, так что отклонения атомов от положения равновесия  становятся зависящими от температуры, а тепловая деформация
становятся зависящими от температуры, а тепловая деформация
 , (14.8)
, (14.8)
Тогда
 . (14.9)
. (14.9)