 |
|
Средняя длина свободного пробега молекул
Взаимодействие молекул в газе, молекулы которого находятся на относительно большом расстоянии друг от друга, носит характер столкновений. От частоты столкновений зависит время протекания процессов, ведущих к установлению состояния термодинамического равновесия: диффузии, теплопроводности, электропроводности. Кроме того, от частоты соударений зависит протекание фазовых переходов в таких системах.
В действительности молекулы газа, непрерывно соударяясь друг с другом, имеют конечные размеры. Между двумя последовательными соударениями молекулы, двигаясь прямолинейно и равномерно, проходят некоторые расстояния, называемы длинами свободных пробегов. Эти расстояния могут быть самыми различными. Поэтому вводится понятие о средней длине свободного пробега.
Средняя длина свободного пробега – путь, который в среднем проходят молекулы между двумя последовательными соударениями:
< l > =  =
=  , (м),
, (м),
где <  - средняя скорость молекул; < Z > =
- средняя скорость молекул; < Z > = 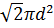
 <
<  - среднее число столкновений, испытываемых одной молекулой за секунду; d – эффективный диаметр молекулы, т.е. минимальное расстояние, на которое сближаются при столкновении центры двух молекул (задаётся в таблицах) (см. рис. 116).
- среднее число столкновений, испытываемых одной молекулой за секунду; d – эффективный диаметр молекулы, т.е. минимальное расстояние, на которое сближаются при столкновении центры двух молекул (задаётся в таблицах) (см. рис. 116).

Рис. 116.
Так как P=  kT, то есть
kT, то есть  =
=  ,то < l > =
,то < l > =  .
.
Таким образом, при заданной температуре средняя длина свободного пробега обратно пропорциональна давлению Р:
< l > 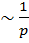 .
.
Пример. При эффективном диаметре молекулы d = 3×10-10 м, давлении Р = 105 Па и температуре Т = 300 К, и средней длине свободного пробега < l > = 10-7 м а, т.к. <  > = 103 м/с, то число столкновений молекулы в секунду: Z =
> = 103 м/с, то число столкновений молекулы в секунду: Z =  = 1010 .
= 1010 .
Упрощённое доказательство
Для определения частоты столкновений Z считаем, что молекула имеет форму шара, и движется среди других неподвижных молекул. Эта молекула сталкивается только с теми молекулами, центры которых находятся на расстояниях  d, то есть лежат внутри “ломаного” цилиндра радиусом d (рис. 117).
d, то есть лежат внутри “ломаного” цилиндра радиусом d (рис. 117).

Рис. 117.
Среднее число столкновений за 1 секунду равно числу молекул в объёме “ломаного” цилиндра:
<  = n0 Z,
= n0 Z,
где n0 - концентрация молекул, а V =  d2 <
d2 < 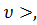 где <
где <  - средняя скорость молекулы, или путь, пройдённый ею за 1 секунду; < Z > =
- средняя скорость молекулы, или путь, пройдённый ею за 1 секунду; < Z > =  d2 n0 <
d2 n0 <  - среднее число столкновений.
- среднее число столкновений.
С учетом движения других молекул: < Z > = 
 d2 n0 <
d2 n0 <  .
.
Тогда: < l > =  =
=  , то есть < l >
, то есть < l >  ; n0
; n0  P => < l >
P => < l >  , т.е.
, т.е.  =
=  =
=  .
.
II. Термодинамика
Термодинамика – часть физики, в которой изучаются наиболее общие закономерности преобразования энергии.
2 .1. Термодинамический метод
Термодинамика изучает макроскопические процессы в телах, не рассматривая внутреннее строение тел. Её выводы основаны на общих принципах (началах), являющихся обобщением опытных фактов. В этом смысле – термодинамика – феноменологическая теория.
Классическая термодинамика изучает равновесные состояния и квазистатические процессы. Такие состояния и процессы в реальности не существуют.
2.2. Внутренняя энергия
Внутренняя энергия U(Дж) – энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т.п.) и энергия взаимодействия этих частиц.
В общем случае внутренняя энергия термодинамической системы включает следующие компоненты:
1) Кинетическая энергия теплового поступательного и вращательного движения молекул;
2) Кинетическая и потенциальная энергия колебаний атомов в молекулах;
3) Потенциальная энергия, обусловленная межмолекулярными взаимодействиями;
4) Энергия электронных оболочек атомов и ионов;
5) Кинетическая и потенциальная энергия взаимодействия нуклонов в ядрах атомов.
В нашем курсе рассматриваем первый и третий компоненты.
Внутренняя энергия – однозначная функция состояния термодинамической системы, т.е. в каждом состоянии система обладает определённой внутренней энергией (она не зависит от того, как система пришла в данное состояние). При переходе системы из одного состояния в другое изменение внутренней энергии определяется только разностью значений внутренней энергии этих состояний и не зависит от пути перехода: ∆U = U2 – U1.
Внутренняя энергия идеального газа
Так как в идеальном газе потенциальная энергия связи между молекулами пренебрежительно мала по сравнению с кинетической энергией их движения, то, исходя из закона равномерного распределения молекул, получим: U = N < 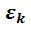 >,N =
>,N =  Na – число молекул газа; <
Na – число молекул газа; < 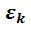 > =
> =  kT – кинетическая энергия теплового хаотического поступательного и вращательного движения молекул. С учётом этого получаем: U =
kT – кинетическая энергия теплового хаотического поступательного и вращательного движения молекул. С учётом этого получаем: U =  kT
kT  Na . Так как Na k = R – универсальная газовая постоянная.
Na . Так как Na k = R – универсальная газовая постоянная.
Окончательно получим выражение для внутренней энергии идеального газа: U=  RT.
RT.
В случае одного моля идеального газа (  = 1 моль):
= 1 моль):  =
= 
Внутренняя энергия моля идеального газа зависит только от его абсолютной температуры.