 |
|
реагують з ферум (ІІІ) хлоридом
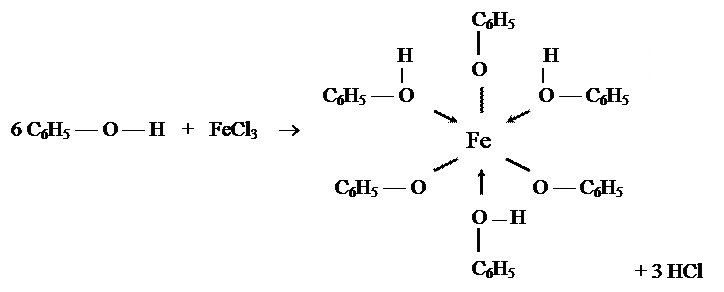 .
.
mmm Якісна реакція на фенол: в результаті взаємодії з ферум (ІІІ) хлоридом утворюється розчин синіх, синьо-зелених, фіалкових відтінків
‚ Реакції заміщення гідроксогупи галогеном
C6H5 ¾ OH + HCl ¹
ƒ Реакції дегідратації
~ реакції внутрішньомолекулярної дегідратації
üяк іметанол, фенолв реакцію не вступає
~ реакції міжмолекулярної дегідратації® реакції утворенняетерів
 [NaOH, t0]
[NaOH, t0]
С6Н5 — О — Na + Cl — CH3 ® С6Н5 — О — CH3 + NaCl
Метилфеніловий етер
„ Реакції естерифікації
Фенол не утворює естерів при безпосередній дії на нього карбонових кислот.
Отримати естер фенолу та карбонової кислоти можна при взаємодії натрій феноляту з хлорангідридом карбонової кислоти:

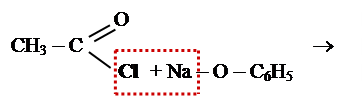 |
Фенілетаноат
Властивості, за бензольним ядром
Гідроксогрупа – орієнтант І роду (ē-донорний замісник) Þ активізує перебіг реакцій заміщення в бензеновому ядрі Þ реакції SE перебігають легко.
… Реакція нітрування фенолу
 [HNO3 (к)]
[HNO3 (к)]
Тринітрофенол
пікринова кислота (пік ратна)
† Реакція бромування фенолу
[бромна вода, звичайні умови]
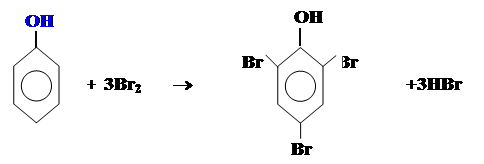 |
Трибромофенол
 |
При дії бромної води на фенол утворюється білий осад.
mmm Це - якісна реакція на фенол
1Нагадай! Бензен реагує тільки з парами брому при t0, kat – FeBr3, при цьому утворюються монобромопохідні.
† Реакція окиснення фенолу
Окиснення фенолу відбувається дуже легко, фенол окиснюється киснем повітря, при цьому фенол змінює забарвлення – відтінки рожевого.
mmm Через легку здатність фенолів до окиснення їх застосовують як антиоксиданти -речовини, які окиснюються самі, перешкоджаючи окисненню інших речовин.
‡ Реакція поліконденсації фенолу та формальдегіду
 |

Продукт реакції поліконденсації фенолу та формальдегіду – фенол-формальдегідні смоли. Це термореактивнийполімер.
Його особливість, полягає в тому, що при нагріванні втрачає здатність плавитись та розчинятись в органічних розчинниках, тобто необернено змінює свою будову при нагріванні.
Фенол-формальдегідні полімери виготовляють у вигляді порошків, які змішують з наповнювачем (деревною мукою, каоліном, волокнистими матеріалами, скляним волокном тощо). В гарячій формі з цієї суміші формують найрізноманітніші вироби – теплоізолізаційні плити, пенопласти.
ÚЯкісна реакція на фенол
~ взаємодія з ферум (ІІІ) хлоридом – утворюється розчин синіх, синьо-зелених, фіалкових відтінків.
~ взаємодія з бромною водою - випадає білий осад 2,4,6-трибромофенолу
ÚДобування фенолу
Метод лужного плаву [натрієві солі сульфобензенової кислоти сплавляють з лугом, t0 – 3000C]:
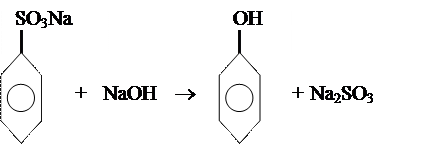 |
‚ Лужний гідроліз моногалогенпохідних аренів
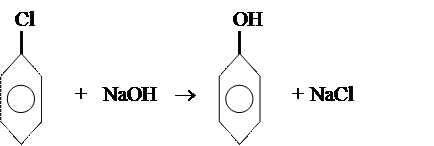 [t0 – 5000C, kat – Cu2+ на алюмосилікатах]
[t0 – 5000C, kat – Cu2+ на алюмосилікатах]
ƒ Кумольний метод
[з пропенової фракції крекінгу нафти, окисник – О2,t0 – 110-1300С]:

 |
1Нагадай! Кумол утворюється при ______________________________
___________________________________________________________________
 |
† Коксування кам’яного вугілля:продукт сухої перегонки кам’яного вугілля – кам’яновугільна смола містить > 400 ароматичних та гетероциклічних сполук, серед яких - фенол.
1Нагадай! Основні компоненти коксування вугілля:
1.________________________
2.________________________
3.________________________
4.________________________
ÚЗастосування фенолу
~ Фенол – сировина для виробництва:
¶ пластмас (фенол-формальдегідні смоли)
¶ ліків (саліцилова кислота та її похідні)
¶ барвників, індикаторів (фенолфталеїн)
¶ вибухових речовин (пікринова кислота)
~ Фенол володіє антисептичними властивостями (5% розчин – карболова кислота) Þ дезинфікуюча речовина:
¶ знезаражування приміщень, хірургічних інструментів
¶ обробка деревини
~ Фенол легко окиснюється Þ антиоксидант.
ÚШкідливий вплив фенолу на живі організми
Фенол є одним з найбільш поширених забруднювачів, який потрапляє в поверхневі води. Він міститься:
Ê в сечі людини і тварин, так як білкові амінокислоти, які містять бензольне ядро, при розщепленні в живих організмах утворюють фенол.
Ê в стічних водах нафтопереробного, коксохімічного, сланцепереробного, лісохімічного, анілінофарбових виробництв.
Фенол згубно впливає на флору та фауну. Шкідлива дія фенольних вод полягає в:
Ê їх токсичності ($дивись фізіологічну дію фенолу)
Ê сильній відновній здатності - на окиснення фенолу витрачається багато кисню Þ порушується кисневий режим водойм
ÚОчищення стічних вод від фенолу
Ê адсорбційний метод:адсорбентом є активоване вугілля
Ê озонування стічних вод:озон легко окислює феноли
Ê метод лужного випарювання:упарювання відбувається з додаванням лугів або вапна. Леткі одноатомні феноли переходять у парову фазу, яку зрошують розчином лугу і виводять з пари у вигляді фенолятів активних металів. Цей метод застосовують для очищення стічних вод, утворених після переробки бурого вугілля.
?Тренувальні вправи
1.Серед наведених нижче формул вказати формули
1.насичених одноатомних спиртів
2.ароматичних спиртів
3.фенолів
а.С6Н13ОН
б.С6Н4(ОН)2
в.С6Н5СН2ОН
г.С6Н5СН2СН2ОН
д.С3Н7ОН
2.Написати рівняння реакцій:
1.фенол + Na
2.фенол + NaOH
3.натрій фенолят + Н2О
4.натрій фенолят (стояння на повітрі)
5.фенол + ферум (ІІІ) хлорид
6.натрій фенолят + хлороетан
7.натрій фенолят + хлороангідрид оцтової кислоти
8.фенол + нітратна кислота
9.фенол + бромна вода
10.фенол + хлороетан (t0, AlCl3)
11.фенол + формальдегід
12.бензен ® Х ® фенол
13.бензен ® Х ® фенол
3.Написати рівняння реакції, за допомогою якого можна довести, що карбонатна кислота сильніша, ніж фенол.
4.Написати рівняння реакцій, за допомогою яких можна отримати фенол, використовуючи ацетилен, безводний бром та воду.
5.Написати рівняння реакцій, за допомогою яких можна виявити наявність кожної з речовин:
1.гліцерин
2.етанол
3.розчин фенолу
4.1-гексен
6.Написати рівняння реакцій за допомогою яких можна здійснити ланцюжки перетворень: ═
| |||
 | |||
|
?Тренувальні задачі
1.Бромна вода, яка містить 43,2 г брому повністю прореагувала з 15 г водного розчину фенолу. Визначити масову частку фенолу у водному розчині.[56,4%]
2.Для нейтралізації суміші етанолу і фенолу витратили 65,31 мл розчину натрій гідроксиду з масовою часткою лугу 20%, густина розчину 1,225 г/см3. При взаємодії такої самої кількості вихідної суміші з надлишком натрію виділилося 6,72 л газу (н.у.) Визначити масові частки компонентів у вихідній суміші. .[19,66%, 80,34%]
3.При дії на суміш метанолу та фенолу бромною водою утворився осад масою 33,1 г. А при дії на цю суміш натрієм виділився газ у кількості, достатній для повного гідрування пропену об’ємом 4,48 л (н.у.) Визначити масову частку фенолу у суміші. [49,5%]