 |
|
МИКРОМИР. ИДЕЯ АТОМИЗМА
От атомизма и симметрии к термоядерным реакциям Солнца
· Белоусова Галина Павловна, учитель физики
Разделы: Преподавание физики

| «Если бы я мог упомнить названия всех элементарных частиц, я бы стал биологом» Энрико Ферми |
МИКРОМИР. ИДЕЯ АТОМИЗМА

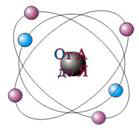
Рис.1. Структура атома: протон и нейтрон – частицы, состоящие из трех кварков.
Замечательный английский поэт и художник Уильям Блейк (1757–1827) в своем стихотворении «Изречение невинности» призывал:
 В одно мгновенье видеть вечность,
В одно мгновенье видеть вечность,
Огромный мир – в зерне песка,
В единой горсти – бесконечность
И небо – в чашечке цветка.
Оказывается, любая песчинка, – действительно, целая Вселенная, т.к. включает в себя почти столько же мельчайших частиц, сколько звезд содержится во всей Мегагалактике!
Из этих частиц состоит и камень, одиноко лежащий на обочине, и цветок, радующий нас своей естественной красотой, и пушистые облака, неторопливо плывущие по голубому небу.
Еще в глубокой древности, 2500 лет назад, некоторые ученые высказывали предположение о строении вещества. Греческий ученый Демокрит (460–370 до н.э.) (рис.2) считал, что все вещества состоят из мельчайших частичек. Была выдвинута атомистическая гипотеза.

Рис.2. Демокрит
В соответствии с ней все в мире состоит из атомов, различающихся своей формой, порядком и ориентацией в теле, а между атомами находится пустота. Что же лежит в основе всех вещей? Если в природе нет ничего, кроме атомов и пустоты, как считал Демокрит, то каким образом из них можно «сконструировать» эти вещи, причем так, что одни из них оказываются твердыми, другие – жидкими, а иные – газообразными?
По легенде идея о существовании атомов возникла у ее автора, когда он разрезал яблоко. До каких пор можно рассекать яблоко на части? Мысль о том, что существует предел такого деления, побудила назвать мельчайшие (далее уже неделимые) частицы материи атомами. В буквальном
переводе с языка древних греков слово «atomos» означает неразрезаемый, нерассекаемый, неделимый.

Рис.3. Аристотель
Атомистическая гипотеза впервые в научном познании предполагала существование объектов, недоступных восприятию органов чувств человека.
Другие философы придерживались других точек зрения, и в IV веке до н.э. Аристотель(рис.3) высказался в поддержку мнения, согласно которому материя состоит из различных сочетаний так называемых четырех стихий – земли, воздуха, огня и воды. Эта идея получила широкое распространение и легла в основу алхимии – примитивной формы химии, господствовавшей до XVII века.
Некоторые ученые продолжали придерживаться мнения, что материя состоит из атомов. И только в начале XIX века, через два тысячелетия, эта гениальная идея человеческого разума нашла свое экспериментальное подтверждение.

Рис.4. Менделеев Д.И. (1834–1907)
Вторым рождением атома человечество обязано английскому ученому Джону Дальтону (1766–1844), который впервые предпринял попытку количественного описания их свойств. Именно им было введено понятие атомного веса и составлена первая таблица атомных весов различных химических элементов. Джон Дальтон проводил опыты с газами и изучал пути их соединения. Так, он обнаружил, что кислород и водород, образуя воду, всегда соединяются в одних и тех же пропорциях по массе. Другие ученые также сталкивались с подобными данными, но именно Дальтон впервые осознал их значение. Он сделал вывод, что вещества состоят из атомов, и что все атомы простого вещества имеют одинаковую массу. При соединении простых веществ количества соединяющихся атомов находятся в определенной неизменной пропорции.
Атомистика Дальтона объясняла, почему вещества соединяются в неизменной массовой пропорции, а также явилась основой для детального изучения материи. Так, объясняя химические превращения и реакции, он пришел к выводу, что каждому химическому элементу соответствует свой тип мельчайших невидимых атомов, а все вещества состоят из химических соединений атомов. Обнаружение этой структуры ознаменовало третье рождение атома. Так, из умозрительной гипотезы он превратился в реальную и осязаемую единицу материи, а это означает, что многообразный окружающий мир сконструирован примерно из сотни типовых блоков – атомов. Последующая классификация атомов в периодической таблице элементов Д.И.Менделеева (рис.4) в порядке возрастания массы показала, что всего в природе насчитывается около 110 химических элементов.
МОДЕЛИ В МИКРОМИРЕ
Хотя уже никто не сомневался в наличии атомов, реально существующие атомы оказались совсем не такими, какими их представлял Демокрит. Уже Больцман по этому поводу писал: «В неделимость атома не верит в настоящее время ни один физик».
Исследования структуры вещества в пространственных масштабах, меньших атомарных, привели к открытию новых простейших кирпичиков мироздания.
Вещества состоят из атомов, а из чего состоят атомы? Первые ключи к разгадке этой тайны появились в конце XIX века, когда исследователи изучали прохождение электричества через разрядные трубки, содержащие разреженный воздух. Иногда стенки трубки излучали зеленый свет при подаче высокого напряжения на две металлические пластинки-электроды. Свечение возникало при попадании невидимых лучей от отрицательного электрода, или катода, на стенки трубки.
В 1887 году английский физик Томсон доказал, что эти катодные лучи (как их тогда называли) – не что иное, как потоки заряженных частиц. Предполагалось, что эти частицы исходят из атомов, хотя их расположение внутри атомов оставалось неясным. Томсон высказал предположение, что атом может быть похож на рождественский пудинг, в котором большая, но легкая по массе положительно заряженная сфера усеяна многочисленными отрицательно заряженными частицами (электронами). Но различные опыты по изучению строения атома доказали, что это, безусловно, ошибочная теория. Установить истинную структуру атома все-таки удалось благодаря продолжительным и кропотливым экспериментам.

Рис.5. Резерфорд(1871–1935)
В 1911 году Эрнест Резерфорд (Рис.5), британский физик, уроженец Новой Зеландии, работавший вместе с Томсоном, предложил строение атома, реально объясняющее его поведение во время экспериментов. Резерфорд предположил, что центр (или ядро) атома имеет положительный заряд и относительно большую массу, а вокруг ядра вращаются крайне легкие и отрицательно заряженные электроны, составляющие электронную оболочку. Это открытие привело к созданию планетарной модели атома (рис.6).

Рис.6. Планетарная модель атома
Согласно этой модели атом состоит из ядра, вокруг которого вращаются электроны. Это похоже на планеты, вращающиеся вокруг Солнца. Поэтому эта модель получила название планетарно-ядерной (табл.1).
Таблица 1