 |
|
ВТОРОЕ И ТРЕТЬЕ НАЧАЛА ТЕРМОДИНАМИКИ
Ø Приведённая теплота – это отношение теплоты Q в изотермическом процессе к температуре Т, при которой происходит передача теплоты:
 .
.
Ø ЭнтропияS – это отношение полученной или отданной теплоты к температуре, при которой происходит этот процесс:
 .
.
Ø Равенство Клаузиуса – для обратимых процессов изменения энтропии равно нулю:
 или
или  или
или  .
.
Ø Неравенство Клаузиуса – при любом необратимом процессе в замкнутой системе энтропия возрастает:
 , или
, или  или
или  .
.
Ø Для произвольного процесса энтропия замкнутой системы, при любых происходящих в ней процессах, не может убывать (или увеличивается или остается неизменной):
 ,
,
где знак “=” – для обратимого процесса; знак “>” – для необратимого.
Ø Математическое выражение второго начала термодинамики:
 .
.
Ø Первое и второе начала термодинамики в объединенной форме:
 ,
,
где dU – изменение внутренней энергии;  приращение работы.
приращение работы.
Ø Изменение энтропии в изопроцессах:
· изохорический процесс:
 , т.к V1 = V2;
, т.к V1 = V2;
· изобарический процесс:
 т.к.
т.к. 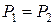 ;
;
· изотермический процесс:
 , т.к.
, т.к.  ;
;
· адиабатический процесс:
 , т.к.
, т.к.  (изоэнтропийный процесс, т.к.
(изоэнтропийный процесс, т.к.  ).
).
Ø Количество теплоты, необходимой для нагревания тела массой т от температуры Т1 до температуры Т2
 .
.
Ø Процессы изменения агрегатного состояния вещества:

· Закон плавления и кристаллизации:
 ,
,
где λ – коэффициент пропорциональности.
· Изменение энтропии при плавлении и кристаллизации:
 .
.
· Закон испарения и конденсации:
 .
.
· Изменение энтропии при испарении и конденсации:
 .
.
Ø Внутренняя энергия системы:
 ,
,
где F – свободная энергия; TS – связанная энергия.
Ø Энергетическая потеря в изолированной системе:
 ,
,
где Тмин – температура окружающей среды.
Ø Статистический смысл энтропии – мера беспорядочности, хаотичности состояния:
 ,
,
где k – коэффициент Больцмана; W – термодинамическая вероятность.
Ø Эквивалентные формулировки второго начала термодинамики:
· невозможен процесс, единственным результатом которого является превращение всей теплоты, полученной от нагревателя в эквивалентную ей работу (формулировка Кельвина);
· невозможен вечный двигатель второго рода (Томсон – Планк);
· невозможен процесс, единственным результатом которого является передача энергии в форме теплоты от холодного тела к горячему (формулировка Клаузиуса);
· энтропия замкнутой системы не может убывать:
 .
.
Ø Третье начало термодинамики – энтропия всякой системы, при температуре, равной абсолютному нулю, равна нулю:
 .
.
Ø Принцип недостижимости абсолютного нуля температуры: невозможно охладить тело до абсолютного ноля.