 |
|
Атмосферный воздух и его особенности.
По своему составу атмосферный воздух является механической смесью разнообразных газов, количество которых в сухом воздухе остаётся неизменным. Масса одного литра воздуха составляет 1,293 г. при давлении 101 кПа (760 мм. рт. ст.) и температуре  С. Состав атмосферного воздуха приведен в таблице 1.2.
С. Состав атмосферного воздуха приведен в таблице 1.2.
Поскольку воздух имеет массу, то он осуществляет давление на поверхность земли. Атмосферное давление не всегда и не везде бывает одинаковым и зависит от географической широты, температуры воздуха и высоты над уровнем моря. На широте 45 градусов на уровне моря при температуре  С атмосферное давление уравновешивается в труппки с перетином 1 см2 барометра столбом ртути высотой 760 мм. или столбом воды 10,33 метра при 40 С, что соответствует давлению на 1 см2 поверхности силой 10 Н (1,033 кгс). Эта величина называется «нормальной» или физической атмосферы. В технике используют техническую атмосферу (кгс/см2), что соответствует давлению 10 м вод. ст. 735,6 мм рт. ст. при значительно повышенных условиях. В системе единиц СИ давление измеряется в Паскалях:
С атмосферное давление уравновешивается в труппки с перетином 1 см2 барометра столбом ртути высотой 760 мм. или столбом воды 10,33 метра при 40 С, что соответствует давлению на 1 см2 поверхности силой 10 Н (1,033 кгс). Эта величина называется «нормальной» или физической атмосферы. В технике используют техническую атмосферу (кгс/см2), что соответствует давлению 10 м вод. ст. 735,6 мм рт. ст. при значительно повышенных условиях. В системе единиц СИ давление измеряется в Паскалях:
1Па = 1  = 0,102 мм. вод ст. = 1,02 *10-4 м. вод. ст. =
= 0,102 мм. вод ст. = 1,02 *10-4 м. вод. ст. =
=1,02 * 10-5 кгс/см2 = 7,5 * 10-3 мм. рт. ст.
Воздух при повышении давления очень легко сжимается, значительно уменьшается в объёме. Давление воздуха измеряют с помощью манометров, показывающих избыточное давление, т.е. давление над атмосферным. Сумма избыточного и атмосферного давлений называется «абсолютным давлением ».
В обычных земных условиях на человека воздух давит равномерно со всех сторон, если поверхность тела человека составляет 1.7-1.8 м2, то сила давления на него составляет 1.7-1.8 тыс. МПа. Притом человек этого не ощущает, потому что тело его на 70% состоит из жидкости, практически несжимаемой, а во внутренних органах давление уравновешивается противодавлением воздуха, которым человек дышит. При земном давлении возникают болезненные ощущения, присущи водолазам, лётчикам, альпинистам.
Воздух, как и другие реальные газы и газовые смеси подсчитываются по известным законам, выведенным для реальных газов. Какое-либо количество газа или газовой смеси характеризуется четырьмя величинами: объёмом(V), давлением(P), температурой(T) и массой(M). Все эти величины находятся в постоянной связи, которая обозначена газовыми законами.
Зависимость давления воздуха от его объёма установлена известным в физике законом Бойля-Мариота:
Р*V=Const, (1,2)
где Р- абсолютное давление; V- объём газа.
Пользуясь этой формулой, вычисляют запас воздуха (кислорода) в баллонах воздушных или кислородных противогазов.
Пример. Избыточное давление воздуха в воздушных баллонах объёмом по 5 л. каждый составляет 20 МПа. Вычислить объём, который будет занимать этот воздух при нормальном давлении.
Р1=20 МПа;
Р2= 0.1МПа;
Vб=5 л.; к=2
На практике проходится считать изменения объёма, давления при разнообразных температурах. Эта зависимость объёма и давления воздуха от его температуры исчисляется законами Гей-Люссака и Шарля. Законы могут быть выражены двумя формулами:
V1/ T1=V2/T2 когда Р=Соnst (1.3)
и
P1/P2=P2/T2 когда V=Const. (1.4)
При расчёте абсолютной температуры газа необходимо к величине 273 градуса прибавить температуру в градусах Цельсия. Например, при температуре воздуха 20 градусов Цельсия его абсолютная температура будет равна 293 градуса Кельвина.
Разнообразные газы, входящие в состав воздуха, по разному действуют при повышении давления на организм человека. Поэтому для того, чтобы рассмотреть действие на человека какого-то газа под давлением, необходимо знать парциальное давление этого газа, то есть часть общего давления, который перепадает на этот газ.
Следовательно, по закону Дальтона, общее атмосферное давление составляет:
Pатм. =  +
+ 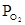 +
+  +
+  , (1.5)
, (1.5)
где Pатм – атмосферное давление, МПа;
 ,
, 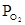 ,
,  ,
,  - парциальное давление азота, кислорода, углекислого газа и других газов, которые входят в состав воздуха, МПа.
- парциальное давление азота, кислорода, углекислого газа и других газов, которые входят в состав воздуха, МПа.
Из формулы (1.5) видно, что атмосферное давление равно сумме парциальных давлений газов, входящих в состав воздуха.
Величина парциального давления газа, входящего в состав воздуха, высчитывается по формуле:
 , (1.6)
, (1.6)
где 
 - процентный состав
- процентный состав  i-го газа, входящего в атмосферный воздух,%.
i-го газа, входящего в атмосферный воздух,%.
В сжатом воздухе процентный состав газов, входящих в состав воздуха, остается неизменным, но парциальное давление каждого газа (кислорода, азота, углекислого газа, и др.) увеличивается ровно во столько раз, во сколько повышено общее давление.
Например, на поверхности парциальное давление кислорода составляет

При избыточном давлении 0.2 МПа (2 кгс/см2)парциальное давление уже будет составлять, учитывая:  ;
;
 .
.
Физиология для того или иного газа обозначается не относительным процентным составом газа в смеси, а (как это было показано в табл. 1.1) величиной его парциального давления. Это подтверждается таким примером. Если человек будет дышать на поверхности земли воздухом, в котором содержится 7.0 % кислорода, он быстро устанет и погибнет от недостачи кислорода, потому что парциальное давление в данном случае будет составлять только 7 кПа(0.07кгс/см2). Если человек будет вдыхать этот же воздух при абсолютном давлении 0,3 МПа (3кгс/см2) при глубине погружения 20 м, он будет ощущать себя хорошо, потому что в этом случае парциальное давление кислорода увеличиться в три раза и станет равным 7*3=21кПа(0.21 кгс/см2). То есть таким же, как и на поверхности земли.
Известно, что граничная величина парциального давления кислорода, вызывающего отравление организма, составляет 0.28 МПа (2.8 кгс/см2). Это приводит к тому, что при погружении в кислородных изолирующих противогазах под воду с содержанием в смеси около 90%кислорода, подобное давление наступает уже на глубине около 20 м, поскольку
0.9*0.3= 0.27 МПа (2.7 кгс/см2).
Поэтому, чтобы избежать кислородного отравления, погружение в кислородных изолирующих противогазах под воду не допускается.
Наибольшую часть земной атмосферы составляет азот. В обычных условиях он является нейтральным газом, не принимающим участия в обмене веществ. По сравнению с другими газами, входящими в состав воздуха, азот имеет повышенную растворимость в крови и тканях человеческого организма. Азот – газ без цвета, запаха и вкуса, он не горит и не поддерживает горение, немного легче воздуха, его масса составляет 1,25 кг/м3.
При нормальном давлении это безвредный газ, но при парциальном давлении около 0,55 МПа (5,5 кгс/см2) он вызывает наркотическое действие. Кстати при повышении давления возрастает парциальное давление и других опасных примесей в воздухе (углекислого газа и т.д.), в последствии чего увеличивается их токсическое действие. Кроме наркотического действия азота и отравляющего действия кислорода и углекислого газа, пребывание под повышенным давлением причиняет организму насыщение газами, растворяющимися в тканях и крови.
Необходимо отметить, что растворение каждого газа осуществляется не зависимо от растворение от других газов. При нормальном давлении в организме человека массой 70 кг. растворено около одного литра азота. При вдыхании газовой смеси, обогащенной кислородом, осуществляется «вымывание» этого азота из организма человека. При повышении давления способность тканей организма растворять газы увеличивается пропорционально давлению. Количество газа, которое может раствориться в жидкости, зависит от величины парциального давления, времени пребывания под давлением и объёма легочной вентиляции. При физической нагрузке частота и глубина дыхания, а также скорость кровотока увеличивается, поэтому насыщение организма газами находится в прямой зависимости от интенсивности физической нагрузки.
При быстром снижении давления, растворенный в тканях газ начинает образовываться в пузырьки. Током крови они могут разноситься по всему телу, вызывая закупорку кровеносных сосудов, что приводит к кессонной болезни.
Состав азота в выдыхаемом воздухе при проделывании работы средней тяжести увеличивается приблизительно на 0,4 %, что соответствует 0,12 л/мин. Этот азот выделяется из организма во время окисления и вида изменения белков. То есть происходит процесс «вымывания» азота из организма человека. Во время использования изолирующего противогаза, азот накапливается в системе противогаза, вследствие чего процентный состав кислорода опасно уменьшается. То есть необходимо использовать средство выделения азота из системы аппарата для исключения заазотирования противогаза.
Существенно действуют на организм человека пары, содержащиеся в воздухе, количество которых может колебаться до 4 %. Чем выше температура воздуха, тем больше в нем водяного пара. Нормальным для дыхания человека считается воздух, в котором состав водяного пара не превышает 1,5-2,5 %.
Кислород – основной газ, принимающий участие, в процессе, который осуществляется в живом организме. Без кислорода жизнь человека не возможна. Внезапный перерыв в обеспечении организма кислородом или даже уменьшение его поступления к тканям вызывает кислородное голодание. Такое заболевание может наступить, если состав кислорода во вдыхаемом воздухе будет менее 16 % при нормальном атмосферном давлении. Влияние кислорода на организм человека приведено в таблице 1.3.
Таблица 1.3 – Влияние кислорода на организм человека.
| Количество кислорода в воздухе, % | Состояние организма |
| 16-17 | Слабость, отдышка, учащение сердцебиение |
| 11-13 | Явная сердечная недостаточность, повышение частоты пульса и дыхания |
| 10,0 | Потеря сознания |
| 7-8 | Может наступить смерть |
Граничное значение парциального давления кислорода во вдыхаемом воздухе, ниже которого в организме человека происходят функциональные расстройства, составляет 13 кПа (97,5 мм. рт. ст.), что соответствует его составу во вдыхаемом воздухе около 13 % при нормальном атмосферном давлении.
Первая помощь при кислородном голодании – вынести пострадавшего на свежий воздух. Если его дыхание остановилось, необходимо сделать искусственное дыхание и вызвать доктора. После оказания помощи пострадавший быстро приходит в нормальное состояние.
Концентрация кислорода в воздухе понижается по нескольким причинам. При пожарах в помещениях с плохим притоком воздуха кислород используется на горение (см. табл. 1.4). в этом случае его концентрация может снизиться до опасного значения. Кроме того, возможны случаи вытеснения воздуха дымом, например, при пожарах в метро, туннелях, подвалах и т. д..
Таблица 1.4 – Изменения состава воздуха на пожаре.
| Местовзятиепроб | Состав в % (при объёме) | ||
| СО | СО2 | О2 | |
| Пожары в подвалах | 0,04-0,65 | 0,1-3,4 | 17,0-20,0 |
| Пожары чердаков | 0,01-0,2 | 0,1-2,7 | 17,7-20,7 |
| Пожары на этажах | 0,01-0,4 | 0,3-10,1 | 9,9-20,8 |
| Исследование _____ дымами | 0,20-1,1 | 0,5-8,4 | 10,8-20,0 |
Кислород – газ без цвета и запаха, тяжелее, чем воздух (_____ 1,43 кг/м3). Кислород не горит но поддерживает горение. Для дыхания в кислородных изолирующих противогазах используется чистый медицинский кислород с анализом, подтверждающим, что его состав не менее 99,5 %.
В системе регенеративного дыхательного аппарата состав кислорода, как правило, более 60%. Научные исследования и многолетняя практика показали, что вдыхание воздуха, имеющее в своем составе повышенное содержание кислорода, при атмосферном давлении в основном безопасно для человека и не отражается на его здоровье. В этом случае парциальное давление менее граничного уровня 0,28 МПа (2,8 кгс/см2). При этом дыхание чистым кислородом в атмосферных условиях на протяжении 3 суток приводит к развитию воспалительных процессов в легких человека.
У здоровых людей в возрасте 20-45 лет, если они дышат чистым кислородом более 7 часов, появляется отдышка и другие признаки ухудшения состояния. Поэтому количество включений в регенеративный дыхательный аппарат без крайней необходимости должно быть ограниченно. Пребывание в аппарате более 4 часов недопустимо и может быть разрешено только в случае крайней необходимости (спасение пострадавших и т.д.) особы, отработавшие в регенеративных дыхательных аппаратах одну смену, могут привлекаться к работе в противогазе не ранее чем через 8 часов.
К поступкам, ведущим к возникновению кислородного отравления относятся: повышенное содержание во вдыхаемом воздухе углекислого газа, тяжелой физической работы, переохлаждения и перегрев организма.
В состав атмосферного воздуха входит (см табл. 1.2) и углекислый газ ( СО2) – газ без цвета, запаха, со слабым кислым вкусом, легче кислорода. Причиной повышения количества углекислого газа на пожаре могут быть процессы взрыва, результаты окисления древесины и угля. Кроме этого, углекислый газ при тушении подают на изолированные пожарные участки. Если в воздухе содержится до 3 процентов углекислого газа, то он стимулирует дыхание. Так в спокойном состоянии повышение содержания СО2 в альвеолярном воздухе на 0,01 % вызывает повышение альвеолярной вентиляции на 5%. При дыхании воздухом содержащим 6% СО2 , появляется отдышка и слабость при 10% возможно полусознательное состояние, при 20-25 % - смертельное отравление.
Источником углекислого газа в газовоздушной смеси, которую вдыхает газодымозащитник из изолирующего противогаза, является опасный простор самого аппарата (на протяжении всего времени работы в нем) и неполное поглощение выдыхаемого углекислого газа в регенеративном патроне кислородного изолирующего противогаза.
Установлено, что во время много часовой работы в регенеративных дыхательных аппаратах среднее содержание СО2 во вдыхаемой смеси не должен превышать 0,25%, а максимальный - 1%.