 |
|
Сильные электролиты. Изотонический коэффициент
Диссоциация электролита приводит к тому, что общее число частиц растворенного вещества в растворе увеличивается по сравнению с раствором неэлектролита той же концентрации. Поэтому коллигативные свойства проявляются в растворах электролитов в большей степени, чем в растворах неэлектролитов. Эта разница учитывается изотоническим коэффициентом i, который показывает, во сколько раз, экспериментально найденные величины 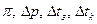 раствора электролита, превышают ту же величину, вычисленную для раствора неэлектролита такой же концентрации:
раствора электролита, превышают ту же величину, вычисленную для раствора неэлектролита такой же концентрации:

Величина  зависит от степени диссоциации
зависит от степени диссоциации  :
:
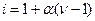 или
или 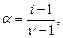
где  - число ионов, образующихся при диссоциации электролита.
- число ионов, образующихся при диссоциации электролита.
Например, для 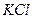
 = 2; для
= 2; для 
 = 3 и т.д.
= 3 и т.д.
Пример 25. Раствор, содержащий 0,85 г  в 125 г воды, закипает при 100,06 °С. Определите кажущуюся степень диссоциации
в 125 г воды, закипает при 100,06 °С. Определите кажущуюся степень диссоциации  , температуру замерзания раствора, давление пара растворителя над раствором при температуре 34 °С, если давление водяного пара при данной температуре равно 5,318 кПа.
, температуру замерзания раствора, давление пара растворителя над раствором при температуре 34 °С, если давление водяного пара при данной температуре равно 5,318 кПа.
Решение: Экспериментально найденное значение повышения температуры кипения раствора составляет:

Найдем теоретическое повышение температуры кипения раствора:

Вычислим изотонический коэффициент:

Определим кажущуюся степень диссоциации:

Найдем понижение температуры замерзания раствора:
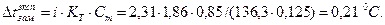
Температура замерзания раствора составит:

Определим понижение давления пара над раствором:


Давление пара над раствором составит:

КОНТРОЛЬНЫЕ Задания для самостоятельноЙ РАБОТЫ
Задача 13
Раствор, содержащий ... г вещества  (...) в ... г воды замерзает при температуре
(...) в ... г воды замерзает при температуре  = ... 0С. Определите:
= ... 0С. Определите:
а) кажущуюся степень диссоциации данного соединения в растворе;
б) температуру кипения раствора;
в) давление пара растворителя над раствором при температуре  =...°С, если давление пара чистой воды
=...°С, если давление пара чистой воды  при данной температуре равно ....
при данной температуре равно ....
| Вариант | Растворено | Температура | Давление водяного пара  , кПа , кПа
| ||||
| Масса, г | Вещество | Масса воды, г |  , 0С , 0С
|  , 0С , 0С
| |||
| 4,9 | MgCl2 | -2,5 | 12,34 | ||||
| 12,0 | NaCl | -3,5 | 70,10 | ||||
| 2,1 | KOH | -0,519 | 3,17 | ||||
| 17,4 | K2SO4 | -1,52 | 90,92 | ||||
| 17,1 | Al2(SO4)3 | -4,19 | 7,37 | ||||
| 0,834 | Na2SO4 | ||||||
| 3,0 | NaCl | -0,028 | 12,34 | ||||
| 1,06 | Na2CO3 | -1,8 | 2,34 | ||||
| 10,4 | CaCl2 | -0,22 | 4,24 | ||||
| 10,0 | H2SO4 | -2,6 | 19,92 | ||||
| 0,44 | AlCl3 | -5,5 | 31,16 | ||||
| 0,64 | Na2CO3 | -0,14 | 3,17 | ||||
| 0,67 | CaCl2 | -0,25 | 70,10 | ||||
| 1,0 | AgNO3 | -0,22 | 101,32 | ||||
| 272,0 | ZnCl2 | -0,348 | 57,80 | ||||
| 9,0 | NaCl | -5,49 | 97,74 | ||||
| 5,0 | CaCl2 | -5,4 | 84,50 | ||||
| 10,4 | MgCl2 | -2,4 | 57,80 | ||||
| 3,9 | CuSO4 | -3,1 | 38,54 | ||||
| 4,5 | KCl | -0,13 | 43,36 | ||||
| 0,0855 | H2SO4 | -0,684 | 15,73 | ||||
| 3,29 | K3[Fe(CN)6] | -0,0054 | 17,30 | ||||
| 14,92 | KCl | -0,062 | 27,33 | ||||
| 2,67 | NH4Cl | -6,8 | 41,87 | ||||
| 1,7 | ZnCl2 | -0,344 | 62,48 | ||||