 |
|
Действие ионизирующего излучения на воду.
Радиолиз воды и водные растворы
Впервые разложение воды под действием ионизирующего излучения подробно исследовали в 1913 году Дуан и Шойер, который обнаружили, что облучение воды  -частицами приводит к образованию водорода, кислорода и небольших количеств перекиси водорода. Однако механизм радиационного разложения воды был неясен вплоть до 1927 года, пока Г. Фрике не начал свои исследования радиационно-химических реакций.
-частицами приводит к образованию водорода, кислорода и небольших количеств перекиси водорода. Однако механизм радиационного разложения воды был неясен вплоть до 1927 года, пока Г. Фрике не начал свои исследования радиационно-химических реакций.
Фрике и его сотрудники обнаружили, что рентгеновское излучение в отличие от  -частиц, не вызывает заметного разложения воды, особенно если перед облучением ее тщательно очищали. В присутствии растворенных веществ заметно значительное разложение воды. При этом количество разложившейся воды не зависит от количества растворенного вещества в широком диапазоне концентраций.[1]
-частиц, не вызывает заметного разложения воды, особенно если перед облучением ее тщательно очищали. В присутствии растворенных веществ заметно значительное разложение воды. При этом количество разложившейся воды не зависит от количества растворенного вещества в широком диапазоне концентраций.[1]
Для объяснения механизма химических реакций в разбавленных растворах Фрике постулировал, что под действием излучения вода переходит в некую «активированную» форму, которая затем инициирует химические реакции. В результате проведенных опытов удалось провести целый ряд параллелей между действием ионизирующей радиации и ультрафиолетового излучения. В частности, Фрике показал, что облучение водных растворов радиацией с длиной волны короче 1900  вызывает многие реакции, сходные с теми, которые наблюдаются под действием рентгеновского излучения. Возбужденные молекулы воды при этом могли диссоциировать.
вызывает многие реакции, сходные с теми, которые наблюдаются под действием рентгеновского излучения. Возбужденные молекулы воды при этом могли диссоциировать.
 (1)
(1)
Дальнейшие исследования, однако, показали, что разложение воды и водных растворов гораздо более сложный процесс, и его нельзя объяснить простым образованием радикалов. Для выяснения сложных механизмов радиолиза воды требуется разобраться в пространственном распределении активных частиц, способах их образования, радиационно-химическом выходе различных процессов, а также реакциях других промежуточных продуктов, участвующих в наблюдаемых химических явлениях.[2]
Возможные реакции распада воды при воздействии ионизирующей радиации:
 , (2)
, (2)
 , (3)
, (3)
 , (4)
, (4)
 , (5)
, (5)
 , (6)
, (6)
 , (7)
, (7)
 , (8)
, (8)
где КЭ – кинетическая энергия. Время образования первичных активных частиц, примерно равно периоду молекулярных колебаний, 10-14 – 10-15 секунд. Масс-спектр воды дал данные о наличии продуктов распада воды при воздействии ионизирующего излучения в относительных единицах:
| Ион | Относительные единицы |

| |

| |

| |

| |

| |

| 1,5 |

| 0,6 |
Через 10-14 – 10-12 секунд после возникновения частицы, указанные в таблице, исчезают.
Наиболее вероятные реакции этих частиц:
 (9)
(9)
 (10)
(10)
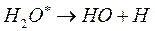 (11)
(11)
 (12)
(12)
 (13)
(13)
 (14)
(14)
 (15)
(15)
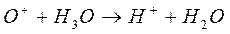 (16)
(16)
 (17)
(17)
 (18)
(18)
Суммарный результат реакций состоит в том, что появляются частицы Н, ОН,  и небольшие количества Н2 и Н2О2. Реакция (12) относится к числу ион-молекулярных реакций и происходит за время около 10-14 секунд. Эта реакция может успешно конкурировать с прямыми реакциями диссоциации, и, вероятно, поэтому ионы Н+, О+ и НО+ почти не образуются, а если и образуются, то в очень небольших количествах. В пользу этого говорят и высокие энергии образования ионов Н+, О+ и НО+. Вторичные электроны, возникающие в процессе ионизации термализуются и сольватируются в течении 10-11 секунд. Сольватированный электрон может реагировать с молекулами воды при отсутствии растворенных веществ с образованием Н и НО – и с другим сольватированным электроном, давая Н2, или с Н+, образуя Н. Стационарная концентрация любых активных частиц оказывается весьма низкой.[7];[2]
и небольшие количества Н2 и Н2О2. Реакция (12) относится к числу ион-молекулярных реакций и происходит за время около 10-14 секунд. Эта реакция может успешно конкурировать с прямыми реакциями диссоциации, и, вероятно, поэтому ионы Н+, О+ и НО+ почти не образуются, а если и образуются, то в очень небольших количествах. В пользу этого говорят и высокие энергии образования ионов Н+, О+ и НО+. Вторичные электроны, возникающие в процессе ионизации термализуются и сольватируются в течении 10-11 секунд. Сольватированный электрон может реагировать с молекулами воды при отсутствии растворенных веществ с образованием Н и НО – и с другим сольватированным электроном, давая Н2, или с Н+, образуя Н. Стационарная концентрация любых активных частиц оказывается весьма низкой.[7];[2]
Прямые доказательства существования атомов Н получены при анализе парамагнитных свойств этих систем. Радикалы ОН, возникающие при электрическом разряде в водяных парах, обнаруживаются по абсорбционным и эмиссионным спектрам около 3064  , а также с помощью масс-спектрометра. Существование радикалов Н2О удалось доказать масс-спектрометрически при анализе продуктов реакции атомов Н, возникающих в газовом разряде с молекулами О2 в присутствии инертных газов.[1]
, а также с помощью масс-спектрометра. Существование радикалов Н2О удалось доказать масс-спектрометрически при анализе продуктов реакции атомов Н, возникающих в газовом разряде с молекулами О2 в присутствии инертных газов.[1]