 |
|
Приклади розв’язування задач
В особливу групу можна виокремити задачі на визначення вологості. Їх розв’язування у більшості випадків можна звести до розв’язування задач про ідеальний газ. Треба пам’ятати, що відносну вологість φ можна визначати як через густину пари, так і через тиски. 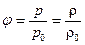 , де ρ і
, де ρ і 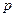 – відповідно густина і тиск водяної пари при заданій температурі, а
– відповідно густина і тиск водяної пари при заданій температурі, а  і
і 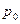 – густина і тиск насиченої пари при тій же температурі.
– густина і тиск насиченої пари при тій же температурі.
Якщо, за умовою задачі, пов’язані температура, тиск і густина насиченої пари, то використовують рівняння Клапейрона – Менделєєва, яке, з урахуванням вологості φ, набуває вигляду:
 або
або 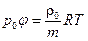 .
.
Задача 1. У закритій посудині об’ємом  знаходиться повітря за температури
знаходиться повітря за температури  з відносною вологістю
з відносною вологістю  . Яка маса водяної пари сконденсується під час охолодження посудини до температури
. Яка маса водяної пари сконденсується під час охолодження посудини до температури  ? Тиск насиченої пари при 25 °С
? Тиск насиченої пари при 25 °С  , при 10 °С
, при 10 °С  .
.
Дано:
 , ,
 К, К,
 , ,
 К, К,
 , ,

| Розв’язування
Тиск водяної пари в посудині:
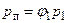 ; ;  .
Отже, точка роси відповідає температурі вище .
Отже, точка роси відповідає температурі вище  . Із рівняння Клапейрона – Менделєєва випливає, що . Із рівняння Клапейрона – Менделєєва випливає, що  і і  . Аналогічно, . Аналогічно,  . Маса сконденсованої води . Маса сконденсованої води
 , ,
|

|
де газова стала  , молярна маса води
, молярна маса води  ;
;
 .
.
Відповідь:  = 1 г.
= 1 г.
Задача 2. Під час пропускання через піпетку 4 см3 рідкої оливи здобуто 304 краплі. Діаметр отвору кінця піпетки 1,2 мм, густина оливи 0,9·103 кг/м3. Знайти коефіцієнт поверхневого натягу оливи.
Дано:
 , ,
 , ,
 , ,
 . .
| Розв’язування
Під час витікання рідини з піпетки перед відривом краплі утворюється «шийка», по якій і відбувається розрив поверхневої плівки (мал. 5.44). Вважаючи, що діаметр кінця піпетки дорівнює діаметру шийки  , а на краплю діють сила тяжіння , а на краплю діють сила тяжіння  і сила поверхневого натягу і сила поверхневого натягу 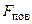 , знаходимо:
. , знаходимо:
.
|

|
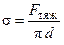 .
.
Силу тяжіння  можна визначити, знаючи об’єм рідини, що витікає,
можна визначити, знаючи об’єм рідини, що витікає, 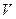 і кількість крапель
і кількість крапель 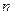 :
:
 ,
,
де  – маса рідини, що витікає;
– маса рідини, що витікає;  – її густина. Отже,
– її густина. Отже,
 ;
;
 .
.
Відповідь: 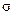 = 0,03 Н/м.
= 0,03 Н/м.
Задача 3. Посудину, в якій була суміш води і льоду, винесли взимку з кімнати на вулицю і почали вимірювати температуру суміші. Маса суміші 8 кг. Отримали графік залежності температури  від часу
від часу  (мал. 5.58). Визначити, яка маса
(мал. 5.58). Визначити, яка маса  води була в посудині спочатку.
води була в посудині спочатку.
Дано:
 , ,
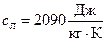 , ,
 , ,
 , ,
 хв, хв,
 хв. хв.
| Розв’язування
З графіка (мал. 5.58) видно, що за перші 40 хв температура суміші в посудині не змінювалась і дорівнювала 0 ºС. Це означає, що протягом цього часу відбувався процес кристалізації й перетворення води в лід. Теплота, яка виділялася під час кристалізації, поглиналася навколишнім середовищем:  . Через 40 хв уся вода перетворилася в лід, і температура льоду в посудині почала знижуватися. Ще через 20 хв температура льоду знизилася на . Через 40 хв уся вода перетворилася в лід, і температура льоду в посудині почала знижуватися. Ще через 20 хв температура льоду знизилася на  . .
|

|
Кількість теплоти, що виділилася льодом під час його охолодження на  :
:
 .
.
Відповідно за одиницю часу виділилося:
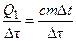 .
.
Якщо вважати, що швидкість відведення теплоти від системи була однаковою, то за 40 хв від системи відведено:  ,
,
де  – кількість теплоти, яка виділилася під час кристалізації води. Отже
– кількість теплоти, яка виділилася під час кристалізації води. Отже  . Звідки:
. Звідки:  ;
; 
Відповідь:  = 0,8 кг.
= 0,8 кг.
Вправа 11
1(п).50 г води повністю випарувалося із склянки за 5 діб. Скільки в середньому молекул вилітало з поверхні води за 1 с?
2 (д). У повітрі насичена водяна пара знаходиться при 30 °С. Визначте масу води, що випала у вигляді роси із 1 м3 повітря під час його охолодження до 15 °С.
3 (д). У кімнаті, об’єм якої 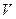 = 150 м3, підтримується денна температура
= 150 м3, підтримується денна температура  = 293 К і відносна вологість φ = 60%. Скільки води виділиться на вікнах, якщо вночі температура знизиться до
= 293 К і відносна вологість φ = 60%. Скільки води виділиться на вікнах, якщо вночі температура знизиться до  = 281 К?
= 281 К?
4 (д). Тонке алюмінієве кільце радіусом 7,8 см і вагою 7·10-2 Н дотикається до розчину мила (σ = 40·10-3 Н/м). Яке зусилля потрібне для відривання кільця від розчину?
5 (с). З якою швидкістю мають летіти назустріч одна одній дві однакові льодинки при температурі – 10 °С, щоб під час удару вони перетворилися в пару?
6 (с). Автомобіль витрачає масу  = 5,67 кг бензину на шлях
= 5,67 кг бензину на шлях  = 50 км. Знайти потужність
= 50 км. Знайти потужність  , що розвивається двигуном автомобіля, якщо швидкість руху
, що розвивається двигуном автомобіля, якщо швидкість руху 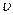 = 72 км/год і ККД двигуна η = 22%. Питома теплота згоряння бензину
= 72 км/год і ККД двигуна η = 22%. Питома теплота згоряння бензину 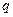 = 45 МДж/кг.
= 45 МДж/кг.
7 (с). На електроплитці потужністю P = 500 Вт, що має ККД η = 40%, нагрівся до кипіння об’єм V = 0,8 л води, що взята при температурі t = 15 °С, і 10% її перетворилось у пару. Як довго тривало нагрівання?
8 (с). Крапля води витікає з кінця скляної трубки d = 1·10-3 м. Знайти кінетичну енергію краплі через 1 с після початку її вільного падіння.
9 (в). По скляному капіляру зі сторонами його перерізу  = 1 мм,
= 1 мм,  = 1,5 мм піднімається на висоту
= 1,5 мм піднімається на висоту 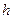 = 5 см рідина, коефіцієнт поверхневого натягу якої 0,040 Н/м. Знайти густину рідини.
= 5 см рідина, коефіцієнт поверхневого натягу якої 0,040 Н/м. Знайти густину рідини.
10 (в). Під час витікання із бюреток однакових об’ємів рідини, густина якої ρ1 = 1030 кг/м3 і  = 0,073 Н/м, та рідини, густина якої ρ2 = 800 кг/м3 утворилось
= 0,073 Н/м, та рідини, густина якої ρ2 = 800 кг/м3 утворилось  = 25 крапель першої рідини і
= 25 крапель першої рідини і  = 80 крапель другої. Визначити коефіцієнт поверхневого натягу цієї рідини.
= 80 крапель другої. Визначити коефіцієнт поверхневого натягу цієї рідини.
11 (в). З якою швидкістю свинцева куля має вдаритися об перешкоду, щоб розплавитись, якщо до удару температура кулі була 100 °С? Під час удару в тепло перетворюється 60% енергії кулі.
12 (в). Сірник довжиною 4 см плаває на поверхні води, температура якої 18 °С. Якщо з одного боку від сірника обережно налити розчину мила, то сірник почне рухатись. У який бік він рухатиметься? Яке значення сили, яка рухає сірник?
! Найголовніше у розділі 5
Для глибокого розуміння навчального матеріалу цього розділу слід збагнути його логічну структуру. У цьому розділі ви продовжували вивчати властивості матерії (мал. 5.45).
Три основні положення молекулярно-кінетичної теорії (МКТ) речовини сформульовано на підставі результатів спостережень і дослідів. Для кожного із трьох положень слід навести приклади експериментальних підтверджень.
Потрібно розуміти, що між атомами і молекулами одночасно діють сили притягання і сили відштовхування електромагнітної природи.
Для усвідомлення усіх перетворень, що призводять до одержання рівнянь, законів, величин цього розділу важливо розуміти такі абстрактні поняття, як відносна молекулярна маса М r, молярна маса  , кількість речовини ν. Ви їх вивчали у шкільному курсі хімії. Для їх свідомого засвоєння зробимо декілька зауважень. Потреба у введенні цих понять зумовлена складністю математичних викладок, якими користувались учені, теоретично обґрунтовуючи дослідні дані з вивчення газів та інших речовин, що складаються з величезної кількості частинок дуже малих розмірів. Установлюючи відносну молекулярну масу сполук, учені користувались кратною подільністю маси їх молекули на якийсь еталон маси. Із цих міркувань за еталон було взято 1/12 маси ізотопу карбону
, кількість речовини ν. Ви їх вивчали у шкільному курсі хімії. Для їх свідомого засвоєння зробимо декілька зауважень. Потреба у введенні цих понять зумовлена складністю математичних викладок, якими користувались учені, теоретично обґрунтовуючи дослідні дані з вивчення газів та інших речовин, що складаються з величезної кількості частинок дуже малих розмірів. Установлюючи відносну молекулярну масу сполук, учені користувались кратною подільністю маси їх молекули на якийсь еталон маси. Із цих міркувань за еталон було взято 1/12 маси ізотопу карбону  . Було введено також поняття кількості речовини і молярної маси. Особливо зазначимо, що певну кількість речовини, відносну молекулярну і молярну масу мають всі речовини, а не тільки ідеальний газ.
. Було введено також поняття кількості речовини і молярної маси. Особливо зазначимо, що певну кількість речовини, відносну молекулярну і молярну масу мають всі речовини, а не тільки ідеальний газ.
На основі прийнятих положень МКТ речовини та експериментальних результатів досліджень газів створено МКТ газів. Для побудови цієї теорії використано модель ідеального газу. На основі цієї моделі і законів класичної механіки виведено основне рівняння МКТ газів (  ). Його називають основним, бо з нього виводяться інші газові закони, зокрема рівняння Клапейрона-Менделєєва, результатами якого є газові закони Авогадро, Бойля – Маріотта , Гей-Люссака, Дальтона, Шарля.
). Його називають основним, бо з нього виводяться інші газові закони, зокрема рівняння Клапейрона-Менделєєва, результатами якого є газові закони Авогадро, Бойля – Маріотта , Гей-Люссака, Дальтона, Шарля.
Температура є головним поняттям розділу «Молекулярна фізика і термодинаміка» найбільш пов’язаним з іншими поняттями (мал. 5.46).
Головним поняттям температури залишається і під час вивчення властивостей рідин і твердих тіл (мал. 5.47) від температури залежить стан речовини, її властивості в різних агрегатних станах.
За будь-якої температури рідини відбувається випаровування. За певної визначеної для кожної рідини температури пароутворення відбувається в усьому об’ємі рідини і називається кипінням. Зі зниженням температури до точки роси відбувається конденсація, наприклад, водяної пари.
Унаслідок випаровування води утворюється ненасичена і насичена пара, вміст якої у повітрі визначає абсолютна і відносна вологість. Слід пам’ятати, що насиченою може стати і ненасичена пара, відділена від рідини, якщо її ізотермічно стискати або ізохорно охолоджувати. Температуру, за якої ненасичена пара перетворюється в насичену в результаті охолодження, називають точкою роси. Це спостерігається і під час випадання роси поблизу поверхні Землі.
На межі рідини, твердого тіла і газу (пари) спостерігаються явища поверхневого натягу і змочування, які сприяють виявленню капілярних явищ.
Тверді тіла поділяють на кристалічні та аморфні. Вони мають здатність до деформацій, за якими вивчають механічні властивості, а регулювати ці властивості можна за діаграмою розтягу матеріалу.
Тверді тіла внаслідок плавлення перетворюються в рідини, а внаслідок тверднення рідини стають твердими тілами. Кристалічні тіла плавляться і тверднуть за певної температури, аморфні ж, поступово розм’якшуючись під час нагрівання, перетворюються в рідини. Аморфні тіла не мають і цілком визначеної температури тверднення.
Запропонована логічна структура поелементно конкретизована у змісті навчального матеріалу і стає зрозумілою лише в результаті самостійної наполегливої праці.
Розділ 6