 |
|
Взаємні перетворення рідин і газів
Взаємодія атомів і молекул у газах, рідинах і твердих тілах. Випаровування та конденсація. Насичена і ненасичена пара. Кипіння.
Питома теплота пароутворення. Вологість повітря та її вимірювання.
Взаємодія атомів і молекул у газах, рідинах і твердих тілах.Молекули різних речовин взаємодіють силами притягання і відштовхування, що мають електромагнітну природу. Модулі цих сил залежать від відстані між молекулами. Тому потенціальна енергія  , що характеризує інтенсивність таких взаємодій, також залежить від відстані між молекулами (мал. 5.30).
, що характеризує інтенсивність таких взаємодій, також залежить від відстані між молекулами (мал. 5.30).
У газоподібному станісередня відстань між молекулами є набагато більшою від  , тому сили міжмолекулярних взаємодій істотно не впливають на рух молекул. Кінетична енергія руху молекул газу значно більша від потенціальної енергії їх взаємодії, тому гази вільно розширюються і легко стискуються. Молекули газу рухаються хаотично (в довільних напрямах і з довільною швидкістю). Молекула, що складається з декількох атомів, під час свого поступального руху ще й обертатиметься.
, тому сили міжмолекулярних взаємодій істотно не впливають на рух молекул. Кінетична енергія руху молекул газу значно більша від потенціальної енергії їх взаємодії, тому гази вільно розширюються і легко стискуються. Молекули газу рухаються хаотично (в довільних напрямах і з довільною швидкістю). Молекула, що складається з декількох атомів, під час свого поступального руху ще й обертатиметься.
У твердому станівідстані між молекулами (атомами) майже дорівнюють  . Через значні міжатомні взаємодії атоми у твердих тілах здійснюють лише коливальний рух відносно положень рівноваги (у кристалах відносно вузлів кристалічної ґратки). Тому потенціальна енергія взаємодії молекул значно більша від їх кінетичної енергії. Щоб змінити об’єм твердого тіла або рідини лише на 1%, необхідні величезні тиски, які перевищують атмосферний тиск у 200 (вода, спирт) – 10 000 разів (метали).
. Через значні міжатомні взаємодії атоми у твердих тілах здійснюють лише коливальний рух відносно положень рівноваги (у кристалах відносно вузлів кристалічної ґратки). Тому потенціальна енергія взаємодії молекул значно більша від їх кінетичної енергії. Щоб змінити об’єм твердого тіла або рідини лише на 1%, необхідні величезні тиски, які перевищують атмосферний тиск у 200 (вода, спирт) – 10 000 разів (метали).
У рідинах сили взаємодії між молекулами слабкіші, ніж у твердих тілах, і значно сильніші, ніж у газах. Молекула рідини, коливаючись у межах певного положення рівноваги, змінює з часом це положення, перескакуючи до інших молекул. Молекули рідини здійснюють коливальний, поступальний і обертальний рухи. У рідинах відстані між молекулами сумірні з їх ефективним діаметром, тому сили взаємодії молекул є значними. У цілому кінетична енергія молекул рідин приблизно дорівнює їх потенціальній енергії.
Випаровування та конденсація.Отже, молекули рідини знаходяться у безперервному хаотичному русі. Якщо молекула випадково з’являється біля поверхні в результаті підштовхування знизу іншою, то вона може набути швидкості, достатньої для подолання притягання з боку інших молекул і вийти у простір над рідиною.
Сукупність молекул, що знаходяться у просторі над рідиною, називають парою, а процес переходу рідини у стан пари – пароутворенням.Пароутворення відбувається двома способами – випаровуванням і кипінням.
Розглянемо спочаткувипаровування – пароутворення, що відбувається за будь-якої температури з вільної поверхні рідини.Оскільки з рідини під час випаровування вилітають найшвидші молекули, то середня швидкість тих молекул, що залишилися, зменшується, ось чому під час випаровування рідина охолоджується. Для підтримання температури такої рідини сталою необхідно підводити тепло. Інтенсивність випаровування залежить від: площі відкритої поверхні рідини (чим поверхня більша, тим більша кількість молекул вилітає з неї), температури, зовнішніх умов (вітер, тиск, концентрація молекул поблизу поверхні рідини). Швидкість випаровування залежить також від природи речовини, яка випаровується. Зокрема, вода випаровується швидше за олію, але ефір швидше випаровується за воду. Це пояснюється різними силами взаємодії між молекулами цих речовин. Пароутворення спостерігається також у твердих тіл. Процес переходу твердого тіла (нафталін, сухий лід, кристалики йоду) одразу в стан пари, називається сублімацією.
Явище охолодження рідини в результаті її випаровування є корисним у природі і на практиці. Завдяки тому, що 2/3 поверхні Землі вкрито водоймами, підтримується тепловий баланс нашої планети. Після купання в них шкіра людини охолоджується через випаровування з поверхні тіла крапель води, при цьому повітря здається холоднішим, ніж вода. Під час перевезення продуктів різними транспортними засобами у спеціальних пристроях випаровують рідкий аміак або рідкий двоокис вуглецю. У місцевостях із жарким кліматом воду намагаються зберігати у пористих глиняних посудинах. Вода, просочуючись крізь пори такої посудини, випаровується, і в результаті цього залишається холодною. Через властивість швидко випаровуватися і охолоджуватися деякі рідини (ефір) використовуються як знеболювальний засіб.
Молекули пари, рухаючись хаотично, можуть набути швидкості, напрямленої, наприклад, у бік рідини, і до неї повернутись. Одночасно з випаровуванням відбувається обернений процес – процес переходу молекул пари в рідину, який називаютьконденсацією. Унаслідок конденсації затрачене для випаровування тепло повертається. Однак, якщо посудина відкрита, то молекули, які залишили рідину, можуть і не повернутися назад. У цих випадках випаровування не компенсується конденсацією і кількість рідини зменшується. Коли потік повітря над посудиною відносить пару, що утворюється, рідина випаровується швидше, оскільки в молекул пари зменшується можливість знову повернутися в рідину.
Втрати енергії поверхнею Землі внаслідок випаровування води з водойм компенсується у результаті конденсації пари під час утворення хмар, туману, роси, виникнення опадів. Під час конденсації пари молекули зближуються, сили молекулярного зчеплення прискорюють їх рух, кінетична енергія молекул зростає, температура рідини, що утворюється при цьому, підвищується. За рахунок внутрішньої енергії пари нагріваються навколишні тіла. Виділення тепла під час конденсації враховують в інженерній справі, використовують у сільському господарстві. Одним із важливих прикладів застосування передачі теплової енергії під час випаровування і конденсації є домашній холодильник.
Конденсація великого об’єму пари вимагає наявності центрів конденсації – мікрокрапель, пилу, оточуючих об’єм пари твердих тіл, які становлять опору для прикріплення молекул газу й поглинають енергію конденсації.
Ненасичена та насичена пара.Накриємо посудину, що містить рідину і пару. Через деякий час між рідиною і парою настане стан теплової рівноваги. При цьому кількість молекул, що утворюють пару за час  , стане дорівнювати кількості молекул, які утворюють конденсат за такий самий час. Встановлюється динамічна рівновага між процесами випаровування і конденсації речовини.
, стане дорівнювати кількості молекул, які утворюють конденсат за такий самий час. Встановлюється динамічна рівновага між процесами випаровування і конденсації речовини.
Пару, що знаходиться в тепловій динамічній рівновазі зі своєю рідиною, називають насиченою.
Ця назва передає ту думку, що у певному об’ємі за певної температури не може бути вміщено більшу кількість пари. Зрідка вдається одержати насичену пару і у відчинених посудинах.
Тиск насиченої пари наближено можна розрахувати за виразом основного рівняння МКТ:
 .
.
Оскільки концентрація  молекул насиченої пари не залежить від об’єму за сталої температури, то і тиск насиченої пари не залежить від об’єму, проте залежить від температури. Ці закономірності встановлено експериментально.
молекул насиченої пари не залежить від об’єму за сталої температури, то і тиск насиченої пари не залежить від об’єму, проте залежить від температури. Ці закономірності встановлено експериментально.
З підвищенням температури тиск насиченої пари зростає швидше, ніж тиск ідеального газу (мал. 5.31, ділянка АВ), адже під час нагрівання тиск насиченої пари збільшується не тільки через підвищення температури, але й у результаті збільшення концентрації молекул (густини) пари. Коли вся рідина випарується, пара за подальшого нагрівання стане вже ненасиченою і її тиск за сталого об’єму зростатиме прямо пропорційно абсолютній температурі (мал. 5.31, ділянка ВС).
Якщо у великому об’ємі знаходиться невелика кількість рідини, то процес пароутворення переважає над процесом конденсації. Динамічна рівновага між парою і рідиною не встановлюється і рідина з плином часу повністю перетворюється у пару. Пара, що не перебуває у стані динамічної рівноваги зі своєю рідиною, називається ненасиченою. Спостереження показують, що тиск і густина ненасиченої пари залежать від речовини, з якої складається пара, від температури, а також від об’єму, в якому пара знаходиться. Вона утворюється за умови, що у просторі, де є пара якоїсь рідини, може ще відбуватися випаровування цієї рідини.
За певної температури тиск ненасиченої пари завжди менший від тиску насиченої пари. Отже, найбільший тиск за певної температури пара чинить, знаходячись у стані насичення.
Описати стан ненасиченої пари можна, використовуючи закони ідеального газу, а стан насиченої пари – за рівнянням Клапейрона-Менделєєва за низьких температур і малих концентрацій:
 , (5.14)
, (5.14)
де 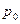 і
і  – відповідно тиск і густина насиченої пари.
– відповідно тиск і густина насиченої пари.
Густина і тиск насиченої пари за незмінної температури є сталими величинами. Для різних рідин – різні величини, бо існує відмінність сил міжмолекулярного зчеплення. Так, при 20 ºС тиск насиченої пари води, молекули якої сильно притягуються одна до одної, дорівнює 2,3 кПа, а тиск леткого хлороформу – 21, 3 кПа.
Перехід ненасиченої пари у насичену, а потім – у рідину, як і зворотний перехід рідини в насичену і ненасичену пару, може відбуватися двома способами – під час зміни об’єму пари і за зміни її температури. Перший спосіб графічно можна зобразити так (мал. 5.32). При зменшенні об’єму ненасиченої пари за сталої температури її тиск зростає доти, поки пара не стане насиченою. Спочатку тиск ненасиченої пари змінюється відповідно до закону Бойля – Маріотта (ділянка АВ ізотерми). Точці В відповідає стан насиченої пари. Починаючи з цієї миті, під час зменшення об’єму насичена пара конденсується в рідину, а її тиск, що не залежить від об’єму, залишається сталим (ділянка ВС ізотерми). Точка С відповідає повному переходу пари в рідину. Оскільки рідини є майже нестисливими, навіть незначне зменшення об’єму рідини пов’язане зі значним збільшенням тиску, то ділянка СД ізотерми, що відповідає рідині, майже паралельна осі ординат.
Збільшення об’єму за незмінної температури веде до того, що описані явища відбуваються у зворотному порядку. Рідина спочатку перетворюється у насичену пару, яка потім стає ненасиченою.
Другим способом переведення пари із ненасиченої у насичену і у зворотному напрямі є зміна її температури. Якщо охолоджувати ненасичену пару за сталого тиску, вона стає насиченою, а потім конденсується в рідину (утворення роси на поверхні Землі). Якщо рідину нагріти, відбувається процес пароутворення. Спочатку пара є насиченою, а потім стає ненасиченою. У закритій посудині процес випаровування рідини триває доти, поки тиск пари не досягне значення тиску насиченої пари.
Кипіння.З підвищенням температури рідини інтенсивність випаровування зростає. Випаровування відбувається не тільки з поверхні рідини, але й й бульбашки повітря, яке розчинене в рідині. Особливим видом випаровування є процес кипіння.
Кипіння – процес утворення пари не тільки на поверхні рідини, а і в її об’ємі.
Необхідною умовою кипіння є наявність в об’ємі рідини під меніском бульбашок розчиненого в ній газу або адсорбованого на стінках посудини, які відіграють таку саму роль, як пилинки або іони у процесі конденсації, тобто роль зародків. Бульбашки газу (повітря) у процесі нагрівання рідини наповнюються насиченою парою під час випаровування рідини всередину бульбашки. За звичайної температури тиск насиченої пари в бульбашках набагато менший від зовнішнього тиску. Під зовнішнім тиском слід розуміти атмосферний і гідростатичний тиски та тиск, зумовлений кривизною поверхні бульбашки.
Бульбашки повітря за невисоких температур сплюснуті і мають мікроскопічні розміри. З підвищенням температури тиск насиченої пари в бульбашці зростає (  ). За деякої граничної температури для кожної рідини, яку називають температурою кипіння, тиск пари всередині бульбашок переважає зовнішній, внаслідок чого бульбашки збільшуються в об’ємі. А коли сила Архімеда перевищує за модулем силу зчеплення бульбашки зі стінкою посудини і силу тяжіння бульбашки спливають у верхні шари рідини (наприклад, води), які ще не встигли нагрітися. Оскільки бульбашки містять пару і небагато повітря, то значна частина водяної пари конденсується у воду і бульбашка зменшується. Це періодичне зменшення і збільшення бульбашок супроводжується звуками: закипаюча вода «шумить». Нарешті вся вода прогрівається і бульбашки у верхніх шарах уже не зменшуються у розмірах і, вийшовши на поверхню, лопаються, викидаючи пару у простір над рідиною (мал. 5.33). На місці цих бульбашок утворюються інші, «шум» припиняється і починається «булькання» – ми говоримо, що вода закипіла. Кипіння починається вже за температури, що відповідає рівності
). За деякої граничної температури для кожної рідини, яку називають температурою кипіння, тиск пари всередині бульбашок переважає зовнішній, внаслідок чого бульбашки збільшуються в об’ємі. А коли сила Архімеда перевищує за модулем силу зчеплення бульбашки зі стінкою посудини і силу тяжіння бульбашки спливають у верхні шари рідини (наприклад, води), які ще не встигли нагрітися. Оскільки бульбашки містять пару і небагато повітря, то значна частина водяної пари конденсується у воду і бульбашка зменшується. Це періодичне зменшення і збільшення бульбашок супроводжується звуками: закипаюча вода «шумить». Нарешті вся вода прогрівається і бульбашки у верхніх шарах уже не зменшуються у розмірах і, вийшовши на поверхню, лопаються, викидаючи пару у простір над рідиною (мал. 5.33). На місці цих бульбашок утворюються інші, «шум» припиняється і починається «булькання» – ми говоримо, що вода закипіла. Кипіння починається вже за температури, що відповідає рівності  . За нормальних умов термометр, вміщений у пару над кип’ячою чистою водою, весь час поки вона кипить показує одну і ту саму температуру, майже 100 0С. У такий спосіб градуюють термометри.
. За нормальних умов термометр, вміщений у пару над кип’ячою чистою водою, весь час поки вона кипить показує одну і ту саму температуру, майже 100 0С. У такий спосіб градуюють термометри.
Усі рідини мають сталу температуру кипіння, яка залежить від роду речовини і зовнішнього тиску. Температура кипіння залежить від тиску насиченої пари. Чим більший тиск насиченої пари, тим менша температура кипіння. Чим менший тиск насиченої пари, тим більша температура кипіння.
Чим більший зовнішній тиск, тим вищою буде температура кипіння рідини і навпаки. Так, на висоті 5 км над рівнем моря, де тиск є у 2 рази нижчий від атмосферного, температура кипіння води 83 ºС. Отже, рідину можна закип’ятити, не нагріваючи її; достатньо знизити тиск над рідиною і вона закипить. Цю властивість рідин широко використовують у різних технологічних процесах: у процесі нафтопереробки для роз’єднання нафтопродуктів, під час цукроваріння сироп кипить завдяки зниженому тиску при незначній температурі і цукор не пригорає тощо.
Для прискорення варіння придумали «швидковарки» – посудини зі щільно припасованою кришкою (мал. 5.34), де при нагріванні за допомогою регульованого запобіжного клапана забезпечується підвищений тиск, температура кипіння води досягає 120 ºС. Оскільки швидкість хімічних реакцій під час приготування їжі подвоюється на кожні 10 ºС, що перевищують 100 ºС, то підвищення температури кипіння на 20 ºС у 4 рази прискорює процес приготування їжі.
У парових котлах, де тиск досягає 15 атм (1,5·106 Па), температура кипіння води майже 200 ºС.
Щоб кипіння відбувалося тривалий час, треба спочатку рідину довести до температури кипіння, а потім продовжувати надавати їй теплоту, необхідну для пароутворення:
Q = cm + rm,
де с – питома теплоємність рідини, m – маса рідини, r – питома теплота пароутворення.
Завдяки якісній обробці поверхонь посудини та очищенню самої рідини можна досягти практичної відсутності в ній центрів пароутворення, що призводить до того, що кипіння не відбувається навіть за температур, вищих від температури кипіння. Таку рідину називають перегрітою.
Питома теплота пароутворення.Під час випаровування рідини, температура якої дещо нижча за температуру навколишнього середовища, робота на подолання міжмолекулярних сил виконується за рахунок енергії, яка надходить з навколишнього середовища (через стінки посудини, з повітря тощо). Залежно від маси і будови речовини, її температури ця кількість теплоти різна. Тому і виникла потреба введення поняття питомої теплоти пароутворення (конденсації).
Питома теплота пароутворення – важлива характеристика процесів випаровування і конденсації. Це фізична скалярна величина  , що чисельно дорівнює кількості теплоти, потрібної для перетворення 1 кг рідини в пару за температури її кипіння. Її в СІ вимірюють у джоулях на кілограм;
, що чисельно дорівнює кількості теплоти, потрібної для перетворення 1 кг рідини в пару за температури її кипіння. Її в СІ вимірюють у джоулях на кілограм;  = Дж/кг.
= Дж/кг.
Для води r = 2,256·10 6 Дж/кг при 100 ºС. Під час пароутворення тепло, що підводиться до рідини, витрачається на руйнування зв’язків між її молекулами.
Питому теплоту пароутворення можна визначити не тільки за температури кипіння, але й під час пароутворення за будь-якої температури. У цьому разі питома теплота пароутворення залежатиме від температури.
Для випаровування рідини масою  їй треба надати кількість теплоти:
їй треба надати кількість теплоти:

Під час конденсації 1 кг пари виділятиметься теплота, що чисельно дорівнює кількості теплоти пароутворення з 1 кг рідини. Питома теплота пароутворення зменшується зі зростання температури і за критичної температури дорівнює нулю. Що ж таке критична температура?
Вологість повітря та її вимірювання.З поверхні водойм, вологого ґрунту, листків рослин, легенів і шкіри тварин та людини в атмосферу Землі випаровується величезна кількість водяної пари (1014 т/рік) і майже ¼ цієї води випадає у вигляді опадів на сушу. Тому атмосферне повітря завжди вологе. Атмосферне повітря є сумішшю різних газів (  ,
,  , інертні гази, водяна пара).
, інертні гази, водяна пара).
Хоча водяної пари в атмосфері мало порівняно з іншими її складовими, їх значення для життєдіяльності всього живого величезне.
Від наявності водяної пари в атмосфері залежить режим випаровування з поверхні суходолу, морів. Перехід водяної пари в рідкий і твердий стан приводить до утворення туманів, хмар, опадів. Виділення теплоти конденсації, замерзання слугують внутрішнім джерелом енергії руху повітряних мас. Здатність водяної пари поглинати сонячне та інфрачервоне випромінювання Землі впливає на тепловий режим земної поверхні й атмосфери.
Процеси випаровування впливають також на організм людини, що складається на 65% з води. За одну добу (в залежності від роду занять) з поверхні шкіри і легенів людини випаровується майже 2 кг води. Це вказує на велике значення вологості оточуючого повітря для її здоров’я й самопочуття. Тривале перебування в теплому й вологому повітрі порушує теплообмін в організмі. Людина стає в’ялою, її працездатність знижується. Тому про вміст водяної пари в атмосфері щоденно повідомляють у зведенні погоди.
Важливе значення має вологість для життєдіяльності тваринного і рослинного світу, для процесів сушіння виробів тощо.
Контроль і підтримання необхідної вологості дуже важливі також для зберігання книг, творів мистецтва, музичних інструментів, харчових продуктів, овочів, фруктів тощо.
Для підтримання необхідної вологості користуються приладами, які зволожують чи осушують повітря – кондиціонерами.
Для вивчення впливу на ці процеси потрібні оперативні дані. Вміст водяної пари в повітрі, тобто його вологість, можна охарактеризувати кількома величинами. Оскільки атмосферний тиск – це сума тиску сухого повітря і водяної пари, що є в ньому, то тиск, який чинила б водяна пара, коли б не було інших газів, називають парціальним тиском водяної пари. Парціальний тиск пари ще називають пружністю. За парціальним тиском водяної пари не можна судити про те, наскільки водяна пара в цих умовах близька до насиченої. Тому ввели величину, яка показує наскільки водяна пара за певної температури близька до насичення – відносну вологість повітря.
Відносна вологість –це відношення парціального тиску водяної пари p, що міститься в повітрі за певної температури, до тиску  насиченої пари (за такої самої температури), виражена у відсотках:
насиченої пари (за такої самої температури), виражена у відсотках:
 % ,
% ,
 % ,
% ,
де  – відповідно густина ненасиченої пари (абсолютна вологість);
– відповідно густина ненасиченої пари (абсолютна вологість);  – густина насиченої водяної пари.
– густина насиченої водяної пари.
Оскільки тиск насиченої пари не залежить від об’єму, але залежить від температури і ця залежність є складною, тому вона досліджена експериментально. На основі здобутих результатів складено таблиці залежності тиску насиченої водяної пари від температури. Якщо знижується температура ненасиченої пари, то її відносна вологість зростатиме без додаткового випаровування води. Знижуючи температуру повітря, можна довести пару, що в ньому перебуває, до стану насичення, що приводить до випадання роси.
Вологість повітря вимірюють спеціальними приладами – психрометром, гігрометром тощо. Психрометр(мал. 5.35) складається з двох термометрів: резервуар одного з них, який показує температуру повітря, залишається сухим, резервуар другого оточений шматком тканини, зануреної у воду. Вода випаровується і завдяки цьому термометр охолоджується. Чим більша відносна вологість φ, тим менш інтенсивне випаровування і тим вищу температуру показує термометр, оточений вологою тканиною. За різницею температур термометрів і спеціальною таблицею можна визначити відносну вологість φ повітря. Найсприятливішою для організму людини є відносна вологість від 40% до 60%.
За деякої температури ненасичена пара перетворюється в насичену (відносна вологість дорівнює 100%). Температура t p, до якої треба ізобарно охолодити повітря певної вологості, щоб водяна пара стала насиченою, називається точкою роси.
Вимірюють вологість також за допомогою волосяного гігрометра, дія якого ґрунтується на властивості волосини людини змінювати свою довжину у вологому повітрі. Унаслідок збільшення вологості довжина волосини зростає, а зі зменшенням вологості волосина коротшає.
? Запитання для самоперевірки
1. Що називають пароутворенням? Конденсацією? Випаровуванням? Парою?
2. Назвіть причини, від яких залежить швидкість випаровування рідини.
3. Як пояснити зниження температури рідини у результаті її випаровування?
4. Чи можуть випаровуватися тверді тіла?
5. Що таке сублімація? Наведіть приклади речовин, здатних до сублімації.
6. За якою формулою визначають кількість теплоти, витрачену на перетворення в пару довільної маси рідини і виділену під час конденсації пари в рідину?
7. Що називають питомою теплотою пароутворення?
8. Опишіть процес пароутворення в закритій посудині. Що таке динамічна рівновага?
9. Яку пару називають насиченою?
10. Чому тиск насиченої пари не залежить від об’єму, у якому вона знаходиться?
11. Зобразіть графічно і поясніть залежність тиску насиченої пари від температури за постійного об’єму.
12. Запишіть формулу залежності тиску насиченої пари від температури і поясніть її.
13. Що називають кипінням? Виконавши рисунок, поясніть фізичний процес кипіння.
14. Запишіть і поясніть умови кипіння рідини.
15. Від чого залежить температура кипіння рідини?
16. Чому під час кипіння температура рідини не змінюється?
17. Поясніть принцип дії швидковарки.
18. Що розуміють під вологістю повітря?
19. Що називають відносною вологістю повітря? Які формули виражають зміст цього поняття у фізиці і метеорології? У яких одиницях її виражають?
20. Відносна вологість повітря 70%. Що це означає?
21. Що називають точкою роси?
22. За допомогою яких приладів визначають вологість повітря?
23. Які суб’єктивні відчуття вологості повітря людиною?
24. Виконавши рисунок, поясніть будову і принцип дії психрометра.