 |
|
Реакция Мейера (1872)
Взаимодействие галоидных алкилов с нитритом серебра приводит к получению нитроалканов:
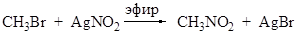
Способ получения нитроалканов из галоидных алкилов и нитрита натрия в среде ДМФА (диметилформамида) предложен Корнблюмом. Реакция протекает по механизму SN2.

Наряду с нитросоединениями в реакции образуются нитриты, это связано с амбидентностью нитрит-аниона:
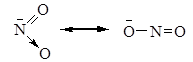
Строение нитроалканов
Нитроалканы могут быть изображены октетной формулой Льюиса или резонансными структурами:

Одна из связей атома азота с кислородом называется донорно-акцепторной или семиполярной.
Физические свойства
Нитросоединения жирного ряда – жидкости, обладающие приятным запахом, они мало растворимы в воде, ядовиты, не вызывают коррозии металлов. В табл. 24.1 приведены температуры кипения, плотность и показатель преломления наиболее распространенных нитропарафинов. Нитросоединения – полярные вещества; их дипольные моменты 3,5-4,0 D.
Таблица 24.1
Физические свойства нитроалканов
| № | Вещество | Т. кип., °С | d, г/см3 | nD20 |
| Нитрометан | 101,2 | 1,132 | 1,3935 | |
| Нитроэтан | 114,0 | 1,047 | 1,3901 (24°С) | |
| 1-Нитропропан | 131,6 | 1,008 | 1,4003 (24°С) | |
| 2-Нитропропан | 120,8 | 1,024 | - | |
| Тетранитрометан | 125,7 | 1,631 | 1,4384 | |
| Тринитрометан (нитроформ) | 45* | 1,615 | - | |
| Гексанитроэтан | 142* | - |
* т. пл.
Химические свойства
Химическиепревращения нитроалканов связаны с реакциями по a-водородному атому углерода и нитрогруппе.
К реакциям по a-водородному атому следует отнести реакции со щелочами, с азотистой кислотой, альдегидами и кетонами.
1. Образование солей
Нитросоединения относятся к псевдокислотам – они нейтральны и не проводят электрический ток, однако взаимодействуют с водными растворами щелочей с образованием солей, при подкислении которых образуется аци-форма нитросоединения, самопроизвольно изомеризующаяся затем в истинно нитросоединение:

Способность соединения существовать в двух формах называется таутомерией. Анионы нитроалканов – амбидентные анионы, обладающие двойственной реакционной способностью. Строение их может быть представлено следующими формами:

2. Реакции с азотистой кислотой
Первичные нитросоединения взаимодействуют с азотистой кислотой (HONO) с образованием нитроловых кислот:

Нитроловые кислоты при обработке щелочами образуют соль кроваво-красного цвета:

Вторичные нитроалканы образуют псевдонитролы (гем-нитронитрозо-алканы) синего или зеленоватого цвета:

Третичные нитросоединения с азотистой кислотой не реагируют. Эти реакции используют для качественного определения первичных, вторичных и третичных нитросоединений.
3. Синтез нитроспиртов
Первичные и вторичные нитросоединения взаимодействуют с альдегидами и кетонами в присутствии щелочей с образованием нитроспиртов:
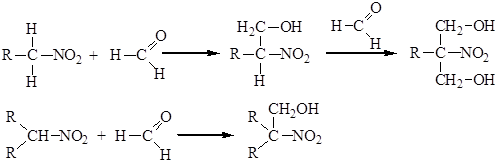
Нитрометан с формальдегидом дает триоксиметилнитрометан NO2С(СН2ОН)3. При восстановлении последнего образуется аминоспирт NH2С(СН2ОН)3 – исходное вещество для получения моющих средств и эмульгаторов. Тринитрат три(оксиметил)нитрометана, NО2С(СН2ОNО2)3, является ценным взрывчатым веществом.
Нитроформ (тринитрометан) при взаимодействии с формальдегидом образует тринитроэтиловый спирт:

4. Восстановление нитросоединений
Полное восстановление нитросоединений в соответствующие амины можно осуществить многими методами, например, действием сероводорода, железа в соляной кислоте, цинком и щелочью, литийалюмогидридом:




Известны также методы неполного восстановления, в результате которого образуются оксимы соответствующих альдегидов или кетонов:
