 |
|
Реакции электрофильного замещениия
Карбонильная группа является электроноакцепторным заместителем, дезактивирует ароматическое кольцо в реакциях электрофильного замещения и направляет электрофильный агент в м-положение:

Ароматические альдегиды при хранении легко окисляются до кислот. Окисление ускоряется светом и катализаторами – солями металлов, например, железа.
Окисление можно предотвратить добавлением ничтожных количеств ингибиторов – фенолов или аминов.
Ароматические кетоны менее реакционноспособны, чем кетоны жирного ряда. Для них не характерна реакция с бисульфитом натрия. С гидроксиламином и производными гидразина, а также магнийорганическими соединениями ароматические кетоны реагируют по обычной схеме.
Жирноароматические кетоны (например, ацетофенон) благодаря подвижности водородных атомов у атома углерода в α-положении легко галогенируются и способны к различным реакциям конденсации (альдольная конденсация, конденсация Кляйзена).
Отдельные представители
Бензальдегид – бесцветная жидкость с запахом горького миндаля, т. кип. 179,5°С. На воздухе он быстро окисляется в бензойную кислоту. Бензальдегид встречается в природе в виде гликозида амигдалина в масле горьких миндалей, в косточках вишни, абрикоса, персика и т.д. Амигдалин под действием ферментов дает бензальдегид, синильную кислоту и дисахарид генцибиозу. Бензальдегид в промышленности получают каталитическим окислением толуола. Широко применяется в синтезе красителей, лекарств и душистых веществ.
Коричный альдегид С6Н5-СН=СН-СНО применяется в парфюмерной промышленности.
Ацетофенон – имеет запах цветов черемухи. Встречается в каменноугольной смоле. В промышленности его получают каталитическим окислением этилбензола кислородом воздуха. Применяется в парфюмерии.
Бензофенон – также применяется в парфюмерной промышленности, галлогенпроизводные о-аминобензофенона используются в синтезе успокаивающих лекарственных препаратов (транквилизаторов).
КАРБОНОВЫЕ КИСЛОТЫ
Лекция 20. ОДНООСНОВНЫЕ НАСЫЩЕННЫЕ
КАРБОНОВЫЕ КИСЛОТЫ
Гомологический ряд насыщенных карбоновых кислот. Общая формула. Изомерия. Номенклатура. Способы получения: из алканов, алкенов, алкинов, спиртов, альдегидов и кетонов, галогеналканов (через нитрилы и по реакции Гриньяра) и сложных эфиров (гидролиз жиров). Физические свойства. Строение карбоксильной группы,
p,p – сопряжение.
Органические карбоновые кислоты характеризуются наличием функциональной карбоксильной группы СООН. По числу этих групп в молекуле различают одно-, двух– и многоосновные кислоты. Органические кислоты могут быть предельными (насыщенными) – карбоксил связан с алкилом, непредельными (ненасыщенными) – карбоксил связан с радикалом непредельного углеводорода и ароматическими – карбоксил связан с бензольным кольцом.
Одноосновные предельные карбоновые кислоты имеют общую формулу СnН2nО2 или CnH2n+1COOH. Изомерия связана с изомерией углеродного скелета.
Кислоты С1-С3 не имеют изомеров, по мере возрастания углеродной цепи число изомеров увеличивается.
По системе IUРАС карбоновые кислоты называют, выбирая за основу наиболее длинную цепь, содержащую карбоксильную группу, и добавляя окончание -овая кислота; углеродному атому карбоксильной группы приписывается номер 1. Для многих карбоновых кислот сохранились их тривиальные названия (муравьиная, уксусная, масляная); положение заместителей можно обозначать буквами греческого алфавита или цифрами:


Остатки карбоновых кислот имеют следующие названия:

Кислотные остатки RCO– (ацилы) имеют следующие названия:
| метаноил | формил | НСО- |
| этаноил | ацетил | СН3СО- |
| пропаноил | пропионил | СН3СН2СО- |
| бутаноил | бутирил | СН3СН2СН2СО- |
| пентаноил | валероил | СН3СН2СН2СН2СО- |
Карбоксилат-анионы имеют следующие названия:
НСОО– – формиат (метаноат);
СН3СОО– – ацетат (этаноат);
СН3СН2СОО– – пропионат (пропаноат).
Промышленные способы получения
карбоновых кислот
1. Окисление углеводородов. Существует два способа: окисление низших алканов C4-C8 преимущественно в уксусную кислоту и окисление твердого парафина в так называемые синтетические жирные кислоты (СЖК) с прямой цепью углеродных атомов С10-С20, являющихся сырьем для синтеза ПАВ (поверхностно-активных веществ).
Процесс протекает в жидкой фазе при нагревании или в присутствии катализаторов. При окислении алканов происходит деструкция по связям между вторичными углеродными атомами, поэтому из н-бутана образуется главным образом уксусная кислота, а в качестве побочных продуктов – метилэтилкетон и этилацетат.
2.Синтезы на основе оксида углерода (II). Карбоновые кислоты получают на основе оксида углерода по реакции карбонилирования:

Присоединение по двойной связи при кислотном катализе всегда протекает по правилу Марковникова, вследствие этого только из этилена получается неразветвленная кислота, а из его гомологов – α-метилзамещенные кислоты. Особый интерес данный метод представляет для синтеза кислот с третичным радикалом (неокислот) из изоолефинов (реакция Коха):

Механизм реакции состоит в предварительном протонировании алкена кислотой с образованием иона карбения, его взаимодействия с СО с получением ацилий – катиона и реакции последнего с водой с образованием карбоновой кислоты:

Неокислоты и их соли обладают очень высокой растворимостью и вязкостью, а их сложные эфиры – стабильностью к гидролизу, что обеспечивает им широкое применение в ряде отраслей.
Карбонилирование спиртов катализируется комплексами металлов (Ni, Со, Fe, Pd). Процесс реализован в промышленности для синтеза уксусной кислоты из метанола и характеризуется высокими экономическими показателями.
Кислоты также получают окислением альдегидов (продукт оксосинтеза).
Лабораторные способы получения
карбоновых кислот
1. Окисление первичных спиртов (см. лекцию 14).
2. Окисление альдегидов и кетонов. Альдегиды окисляются значительно легче, чем кетоны. Кроме того, окисление альдегидов приводит к образованию кислот с тем же числом углеродных атомов, в то время как окисление кетонов протекает с разрывом углерод-углеродных связей (образуются две кислоты или кислота и кетон):

Окислителями служат перманганат калия или бихромат. Окисление кетонов требует более жестких условий, чем окисление альдегидов.
3. Гидролиз нитрилов. Нитрилы получают взаимодействием галогеналканов с цианистым калием, а затем их подвергают гидролизу водными растворами кислот или щелочей. В кислой среде азот выделяется в виде соли аммония:
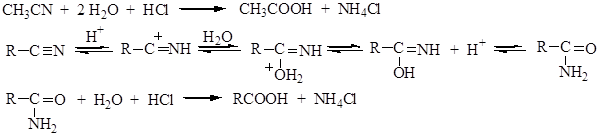
в щелочной – в виде гидроксида аммония, который разлагается с выделением аммиака, кислота же получается в виде соли:

4. Синтез Гриньяра. При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:

Под действием сильной кислоты (обычно НСl) соль превращается в кислоту:

5. Гидролиз жиров. Жиры – сложные эфиры карбоновых кислот и глицерина (триглицериды). Карбоновые кислоты, входящие в состав жиров, имеют углеродную цепь от 3 до 18 углеродных атомов.
Кипячение жиров или масел с водными растворами щелочей (NaOH, КОН) приводит к получению солей карбоновых кислот и глицерина.