 |
|
Отклонение от закона Бойля-Мариотта
Качественное отличие изотерм реального и идеального газов показано на рисунке.
При V>V2 газ ведет себя как идеальный.
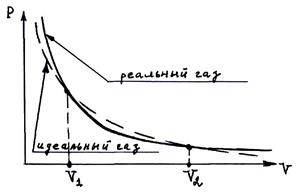 При средних плотностях V1>V>V2 давление реального газа меньше, чем в случае, когда газ ведет себя как идеальный. Это объясняется тем, что при этом проявляется молекулярные силы притяжения, которые делают газ более сжимаемым под действием внешних сил по сравнению с идеальным газом.
При средних плотностях V1>V>V2 давление реального газа меньше, чем в случае, когда газ ведет себя как идеальный. Это объясняется тем, что при этом проявляется молекулярные силы притяжения, которые делают газ более сжимаемым под действием внешних сил по сравнению с идеальным газом.
При бо’льших плотностях (V<V1) давление реального газа больше идеального. Это объясняется только тем, что при больших сжатиях проявляются силы отталкивания, вследствие чего среда делается менее сжимаемой.
Потенциальная энергия парного взаимодействия молекул зависит только от расстояния между молекулами:
 ,
,
где r – расстояние между центрами масс частиц,  – положительная составляющая, связанная с проявлением сил отталкивания,
– положительная составляющая, связанная с проявлением сил отталкивания,  – отрицательная составляющая, связанная с проявлением сил притяжения.
– отрицательная составляющая, связанная с проявлением сил притяжения.
Обе составляющие являются электрического происхождения. Потенциальная энергия, отнесенная к единице массы определяет потенциал парного взаимодействия:

Экспериментальные изотермы реального газа
 Простейший изотермический процесс осуществляют путем медленного сжатия реального газа в сосуде под поршнем.
Простейший изотермический процесс осуществляют путем медленного сжатия реального газа в сосуде под поршнем.
Результаты экспериментов представлены на графике. При этом температура газа должна быть ниже некоторого значения, называемого критической температурой.
Состояния: 1 – состояние ненасыщенного пара.
2 – состояние насыщенного пара
2-3 – сжатие происходит при постоянном давлении: газ конденсируется в жидкость
3-4 – сжатие жидкости; поскольку жидкость обладает малой сжимаемостью, то наблюдается значительное возрастание давления при малых уменьшениях объема.