 |
|
Реакции присоединения
1. Присоединение воды. Вода присоединяется к альдегидам и кетонам, образуя неустойчивые гем-диолы:

Реакция обратима, гем-диолы легко образуются и снова распадаются с отщеплением воды, выделить их удается очень редко. Устойчивость гем-диолов существенно повышается при наличии электроноакцепторных заместителей, связанных с карбонильным атомом углерода. Например, трихлорацетальдегид (хлораль) легко присоединяет воду с образованием устойчивого продукта:
Cl3CCHO + H2O ® Cl3CCH(OH)2
Образующийся хлоральгидрат – кристаллическое вещество с т. пл. 57°С. Устойчивость этого соединения связана с наличием электроноакцепторной трихлорметильной группы. Хлораль применяется в медицине как успокаивающее и снотворное средство.
Другие альдегиды и кетоны также существуют в водных растворах в гидратированной форме с различным содержанием гем-диола (табл. 17.2).
Таблица 17.2
Содержание карбонильной формы и гем-диола
в водных растворах альдегидов и кетонов
| Соединение | Карбонильная форма, % | Гем-диол, % |
| Н2С=О | 0.05 | 99.95 |
| СН3СН=О | ||
| СН3С(О)СН3 | 99.8 | 0.2 |
| СlСН2СН=О |
Водный раствор, содержащий 40% формальдегида, называется формалином.
2. Присоединение спиртов. Спирты, как и вода, реагируют с альдегидами и кетонами:

При этом образуются соединения, содержащие один алкоксильный остаток – OR’ (полуацетали, полукетали) или два – ацетали, кетали. Образование полуацеталей катализируется и кислотами, и основаниями.
Кислотный катализ


На первой стадии происходит протонирование атома кислорода карбонильной группы, на второй стадии образовавшийся карбокатион присоединяет молекулу спирта, реакция завершается депротонированием аддукта.
Активация карбонильной группы в реакциях присоединения воды и спиртов может происходить двумя способами:

Первый путь – специфический кислотный катализ, когда реакция ускоряется Н+. В этом случае скорость реакции изменяется с изменением рН среды (образование оксониевого катиона) и не зависит от природы кислоты.
Во втором случае реакция катализируется не протонами (т.е. диссоциированной кислотой), а недиссоциированной кислотой в целом. В этом случае говорят об общем кислотном катализе. Положительный заряд на карбонильном атоме углерода увеличивается за счет образования водородной связи. Протон в этом случае переносится на карбонильный атом кислорода только при атаке нуклеофила. В этом случае природа кислоты оказывает существенное влияние: чем сильнее кислота, тем выше скорость реакции.
Необходимость активирования карбонильной группы кислотным катализатором будет тем больше, чем менее нуклеофильно основание.
По этой причине сильноосновные азотистые соединения (аммиак, амины, гидроксиламин, гидразин и др.) легко реагируют с альдегидами и кетонами в нейтральной или даже слабощелочной среде, в то время как спирты, менее нуклеофильные, часто требуют добавления кислот, так же как и очень слабые азотистые основания, например 2,4 – динитрофенилгидразин.
Основной катализ
1 стадия – образование алкоксид-иона:

2 стадия – присоединение нуклеофильного реагента:

3 стадия – присоединение протона к образующемуся на второй стадии алкоксид-иону:

Реакция образования ацеталей (кеталей) катализируется только кислотами. В качестве исходного может быть использован альдегид или полуацеталь:

Реакции присоединения спиртов с образованием ацеталей и кеталей являются обратимыми. Они относятся к кислотно-катализируемым реакциям. Ацетали устойчивы к действию оснований.
3. Присоединение синильной кислоты. Синильная кислота присоединяется к карбонильным соединениям с образованием гем-цианоксидов (циангидринов). Реакция катализируется только основаниями, которые позволяют получить активный нуклеофил CN– из слабой кислоты HCN. Циангидрины встречаются в природе – например, содержатся в косточках сливы, вишни, персика и в миндале. Циангидрины приводят к тяжелому отравлению в результате освобождения синильной кислоты внутри организма.
Стадия 1 – образование цианид-иона:

В качестве оснований в этой реакции используют NaOH, K2CO3, третичные амины, но чаще всего реакцию проводят с использованием водного раствора цианида натрия или калия.
Стадия 2 – медленное присоединение цианид-иона к карбонильной группе:

Стадия 3 – быстрое присоединение протона к алкоксид-иону:
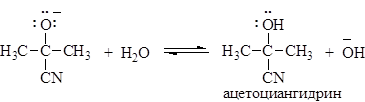
Реакция обратима на всех стадиях, так как в щелочной среде образовавшийся циангидрин расщепляется. Выход продукта реакции зависит от пространственного строения карбонильного соединения: альдегиды образуют циангидрины легко (80-90%), метилкетоны, за исключением ацетона, более трудно.
4. Присоединение бисульфита натрия. Альдегиды и кетоны взаимодействуют с бисульфитом натрия, образуя хорошо растворимые в воде соли α-гидроксиалкансульфоновых кислот:

Этот метод используют для очистки альдегидов и кетонов. Для выделения их из гидросульфитных производных используют разбавленные кислоты и основания.
5. Реакции присоединения – отщепления. Большинство реакций присоединения – отщепления сводится к взаимодействию карбонильной группы с N-нуклеофилами. К N-нуклеофилам относят аммиак и его производные:
R-NH2
где R = H, Alk, Ar, OH, NH2, NHC6H5, NHCONH2, NHCSNH2
Стадия 1 – медленное присоединение N-нуклеофила по карбонильной связи:

Стадия 2 – быстрый перенос протона с атома азота на атом кислорода:
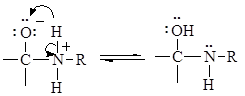
Стадия 3 – отщепление воды (1,2-отщепление):

Продукт этой реакции называется имином или основанием Шиффа. Имины типа >C=NН называются незамещенными иминами, имины типа >C=NR – замещенными иминами.
Многие другие производные аммиака также дают с альдегидами и кетонами аналогичные продукты конденсации. К таким производным относятся гидроксиламин (NH2OH), гидразин (NH2-NH2), фенилгидразин (NH2-NHC6H5) и семикарбазид (NH2-NHC(O)NH2). Продукты их конденсации с карбонильными соединениями называются соответственно оксимами, гидразонами, фенилгидразонами и семикарбазонами:

Конденсацию карбонильных соединений с этими реагентами часто проводят в присутствии электрофильного катализатора, чаще всего – протонных кислот. Реакции с сильными нуклеофилами протекают без катализатора, слабые нуклеофилы реагируют только в присутствии катализатора.
Реакции с участием α-водородного атома
1. Альдольная конденсация. Под действием каталитических количеств водной кислоты или основания альдегиды превращаются в
β-оксиальдегиды. Этот процесс носит название альдольной конденсации:

Альдольная конденсация, катализируемая основаниями. Катализируемая основаниями альдольная конденсация начинается с образования енолят-иона альдегида (стадия 1). Поскольку енолят-ион является нуклеофилом, то он атакует карбонильную группу другой молекулы альдегида. В результате образуется алкоксид-ион (стадия 2). Далее происходит протонирование алкоксид-иона водой, при этом образуется конечный продукт – альдоль и регенерируется катализатор (ОН-) (стадия 3). Это происходит потому, что алкоксид-ион является более сильным основанием, чем гидроксид-ион.

При нагревании в присутствии основания альдоли легко отщепляют воду, образуя a,b-ненасыщенные альдегиды. Дегидратация протекает легко благодаря кислому характеру атома водорода у a-углеродного атома углерода и вследствие того, что образующийся продукт содержит сопряженную систему двойных связей:
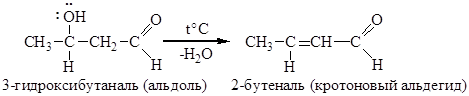
Этот тип конденсации получил название кротоновой.
Альдольная конденсация, катализируемая кислотами. Механизм альдольной конденсации, катализируемой кислотами, включает две основных стадии: превращение кето-формы альдегида в енольную форму (стадия 1) и атака образовавшимся енолом карбонильной группы альдегида (стадия 2):

Альдоль под действием разбавленной кислоты отщепляет воду даже при комнатной температуре, поэтому конденсацию, катализируемую кислотой, практически невозможно остановить на стадии b-оксиальдегида:

Кетоны вступают в альдольную конденсацию значительно труднее, чем альдегиды. Однако при катализе кислотами образующийся в небольших количествах 4-окси-4-метил-2-пентанон (продукт альдольной конденсации) будет быстро дегидратироваться в 4-метил-3-пентен-2-он (мезитилоксид):

2. Галогенирование альдегидов и кетонов. Реакция галогенирования протекает с участием α-углеродного атома. С галогеном реагирует не само карбонильное соединение, а его енольная форма:

При присоединении галогена к енолу образуется неустойчивый галогенгидрин. От него отщепляется галогеноводород, и образуется α-галогензамещенное карбонильное соединение. Реакция катализируется щелочью. Если в молекуле альдегида или кетона с карбонильной группой связана метильная группа (метилкетоны и ацетальдегид), то при избытке галогена в ней замещаются все атомы водорода:

Тригалогенметильная группа является сильнейшим акцептором электронов, поэтому карбонильная активность полученного альдегида или кетона становится высокой, и гидроксид-анион, служивший катализатором в этой реакции, проявляет уже нуклеофильные свойства и атакует карбонильный атом углерода. От полученного аддукта сравнительно легко отщепляется тригалогенметил-анион, который стабилизируется присоединением протона и образует тригалогенметан:
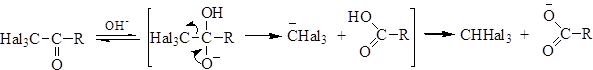
Такая реакция носит название галоформной. При использовании йода в результате галоформной реакции образуется йодоформ – кристаллическое вещество желтого цвета, которое легко идентифицировать. Это позволяет использовать галоформную реакцию для обнаружения метилкарбонильных соединений – в этом случае ее называют йодоформной.
Окислительно–восстановительные реакции
Кетоны в нейтральной среде устойчивы к окислению – например, не реагируют с перманганатом калия. В кислой и щелочной среде кетоны окисляются с расщеплением углерод-углеродной связи, при этом образуется смесь продуктов:

Если R1 и R2 = Н, то в качестве продуктов окисления образуется две (в случае симметричных кетонов R=R3) или четыре различных кислоты (R≠R3 – несимметричный кетон).
В отличие от кетонов альдегиды легко окисляются практически любыми окислителями, даже кислородом воздуха. Легкость окисления альдегидов используют для качественного их обнаружения реакцией «серебряного зеркала» – восстановлением одновалентного серебра в аммиачном растворе:

Восстановление альдегидов и кетонов водородом в момент выделения приводит к образованию первичных и вторичных спиртов:

Отдельные представители
Формальдегид – бесцветный газ с резким специфическим запахом. Он ядовит, действует раздражающе на слизистые оболочки глаз и дыхательных путей. Хорошо растворим в воде, его 40%-ный водный раствор называют формалином и широко используют в качестве дезинфицирующего средства для дезинфекции зерно– и овощехранилищ, парников, теплиц. Формальдегид широко применяется в органическом синтезе – например, в производстве синтетических смол (фенолформальдегидные, карбамидные), глицерина и т.д.
При нагревании с аммиаком формальдегид образует гексаметилентетрамин (уротропин), который в больших количествах применяют в производстве фенолформальдегидных смол, взрывчатых веществ, а также в качестве горючего (сухой спирт).
Уксусный альдегид (ацетальдегид) – жидкость с резким неприятным запахом, вызывает раздражение слизистых оболочек, удушье, головную боль. Из ацетальдегида в промышленных масштабах получают уксусную кислоту, уксусный ангидрид, этиловый спирт, бутиловый спирт, ацетали, этилацетат и ряд других веществ. Подобно формальдегиду он конденсируется с фенолом, аминами и другими веществами, образуя синтетические смолы, используемые в производстве полимерных материалов.
Ацетон – бесцветная жидкость с характерным запахом. Хорошо растворим в воде и органических растворителях. В качестве растворителя в очень больших количествах применяется в лакокрасочной промышленности, в производстве ацетатного шелка, кинопленки, бездымного пороха (пироксилина), для растворения ацетилена (в баллонах) и т.д. Он служит исходным сырьем при производстве небьющегося органического стекла, кетена и т.д.
Лекция 18. НЕНАСЫЩЕННЫЕ АЛЬДЕГИДЫ И КЕТОНЫ
Изомерия. Классификация. Строение: сопряжение связей С=О и С=С. Акролеин и кротоновый альдегид. Способы получения. Химические свойства: особенности реакций электрофильного и нуклеофильного присоединения. Кетены. Дикетен.
Ненасыщенные альдегиды и кетоны, в зависимости от взаимного расположения двойной и карбонильной групп в молекуле, могут быть поделены на три группы: с кумулированными (кетены CH2=C=O), сопряженными (CH=CH2-COCH3 – метилвинилкетон, 1-бутен-3-он; CH2=CHCHO – акролеин, пропеналь) и изолированными (CH2=CHCH2CH2CH2COCH3) кратными связями. Из них наибольший интерес представляют соединения с сопряженными связями (акролеин, кротоновый альдегид, метилвинилкетон) – α,β-ненасыщенные альдегиды и кетоны.
Для некоторых α,β-ненасыщенных альдегидов и кетонов сохранились эмпирические (акролеин) или рациональные (метилвинилкетон) названия. По номенклатуре IUPAC положение двойной связи и карбонильной группы указывают цифрами.
Важнейшими представителями ненасыщенных альдегидов являются акролеин CH2=CH-CHO и кротоновый альдегид CH3-CH=CH-CHO.
Существует несколько способов получения акролеина: