 |
|
Алкадиены с изолированными связями
Для алкадиенов этого типа характерны те же свойства, что и для алкенов, поскольку взаимное влияние двойных связей на расстоянии, более чем две С–С-связи пренебрежимо на фоне влияния ближнего структурного окружения двойной связи.
Лекция №15
АЛКИНЫ
План.
- Изомеризация и номенклатура.
- Методы синтеза.
- Структура и физические свойства.
- Химические свойства.
Алкины – углеводороды ациклического ряда, содержащие в своей структуре два атома углерода, связанные между собой тремя связями, а оставшиеся валентности этих атомов могут быть затрачены на образование связей с другими атомами углерода или атомами водорода.
Алкины образуют гомологический ряд соединений, выраженных общей формулой СnH2n-2. Первый член гомологического ряда – этин или ацетилен.
Изомерияи номенклатура
Согласно IUPAC названия алкинов образуют, заменяя в названиях алканов суффикс “-ан” на “-ин”. В качестве родоначальной структуры выбирают самую длинную цепь, содержащую тройную связь. Нумерацию этой цепи начинают с того конца, к которому ближе находится тройная связь.
Примеры

Названия остатков алкинов образуют, присоединяя суффикс –ил к названию алкина:
HCº C- этинил
СН3-Сº С- пропинил-1
НСº С-СН2- пропинил-2.
В рациональной номенклатуре замещенные алкины рассматриваются как производные ацетилена:

Структурная изомерия начинается с 4-го “С”, изомерия, связанная с изомерией углеродного скелета начиная с 5 “С”. По числу изомеров ацетиленовые углеводороды занимают промежуточное положение между алканами и алкенами.
Методысинтеза алкинов
- Реакции пиролиза метана или этана
2CH4 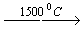 C2H2 + 3H2
C2H2 + 3H2
CH3 - CH3 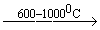 C2H2 + 2H2
C2H2 + 2H2
При пиролизе метана необходимо строго выдерживать время реакции. Для этого используется “закалка” - быстрый ввод на выходе реакционной зоны воды.
- Карбидный метод
CaC2 + 2H2O ® C2H2 + Ca(OH)2
Аналогично реагируют карбиды стронция и бария SrC2, BaC2.
Карбид магния с водой образует пропин
Mg2C3 +4 H2O ® CH3C º CH + 2Mg(OH)2
- Реакции нуклеофильного отщепления дигалогеналканов и моногалогеналкенов.
CH3-CHBr-CH2Br + 2NaOH 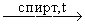 CH3-Cº CH + 2NaBr + 2H2O
CH3-Cº CH + 2NaBr + 2H2O
CH3-BrC=CH2 + NaOH 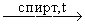 CH3-Cº CH + NaBr + H2O
CH3-Cº CH + NaBr + H2O
- Алкилирование алкинов.
Реакции проводятся через синтез ацетиленидов
а) R-Cº CH + NaNH2® R-Cº C-Na+ + NH3
R-Cº CNa + R'Hal ® RCº CR' + NaHal
б) R-Cº C-H +CH3-MgHal ® R-Cº C-MgHal + CH4
R-Cº C-MgHal + R’Hal ® R-Cº C-R’ + MgHal2
Физическиесвойства алкинов и природа связей
Алкины представляют собой бесцветные газы или жидкости. Начиная с С17 , алкины являются кристаллическими веществами.
Тройная связь представляет собой одну s -связь С-С и две p -связи. При переходе от двойной к тройной связи средняя энергия p -связи снижается. Это означает, что тройная связь менее стабильна, чем двойная. Сам ацетилен неустойчивое соединение и способен к спонтанному взрывному распаду на элементы. Молекула ацетилена имеет линейное строение, что обусловлено sp-состоянием атомов углерода. Тройная связь в алкинах характеризуется более высокой поляризуемостью, чем в алкенах RCº C = 5,96; RC=C=4,17.
По сравнению с алкенами алкины характеризуются большими значениями потенциалов ионизации. Это означает, что электрон на ВЗМО у ацетилена связан прочнее чем у этилена. Это обусловливает более высокую электрофильность алкенов по сравнению с алкинами. Потенциал ионизации алкинов резко снижается при введении в них алкильных групп.
В электронных спектрах поглощения алкины имеют полосу поглощения при 170-180 нм, что соответствует p - p * - переходу. В ИК спектрах характерны валентные колебания связи Сº С при 2100-2260 см-1 и связи º С-Н при 3270-3330 см-1.
В спектрах ПМР химический сдвиг атома водорода º С-Н равен 1,7-2 м.д.
Химическиесвойства алкинов.
Высокая степень ненасыщенности алкинов обусловливает их склонность к реакциям присоединения. В реакциях электрофильного присоединения алкины менее реакционноспособны по сравнению с алкенами, несмотря на то что энергия p -связей у последних выше. Это обусловлено более высокой электрофильностью алкенов. В то же время в реакциях, имеющих гомолитический характер, например, каталитическое гидрирование, большую реакционную способность обнаруживают алкены.
- Реакция гидрирования.
Реакция имеет ступенчатый характер:
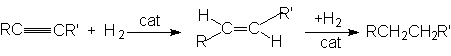
Сat: металлические Ni, Pl, Pd.
На первой стадии количественно образуется алкен, и после практического исчерпывания алкина начинается гидрирование алкена. Это связано с более высоким сродством алкинов к поверхности катализатора. Обычно реакция протекает нестереоселективно и образуется смесь цис- и транс-продуктов присоединения.
Модификация катализаторов приводит к стереоселективному синтезу. Так, промотируя палладий оксидом свинца (II) и CaCO3, получают катализатор Линдлара, на котором осуществляется стереоспецифичный синтез цис-изомера.
| RCºCR' + 2H2 | ® | RCH=CHR' |
| цис-алкен |
К аналогичным результатам приводит катализатор Pd/BaSO4 в пиридине.
Стереоселективное восстановление тройной связи можно осуществлять, используя для этого соответствующие агенты. К этим реакциям относятся:
а) восстановление натрием или литием в жидком аммиаке или этиламине. При этом преимущественно образуется транс-изомер:

б) Гидроборирование. Алкины, подобно алкена, реагируют с гидридами бора, присоединяя их по тройной связи углерод-углерод
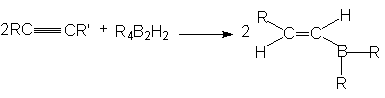
Первоначально образуется моноалкенильное производное бора, причем присоединение идет против правила Марковникова. Дальнейшее присоединение может происходить по двойной связи моноалкенильных производных бора. Однако если R2BH ( или RBH2) содержит объемные группы, то пространственные препятствия затрудняют вторую реакцию присоединения и достигается высокий выход моноалкенильного производного.
Реакции такого типа особенно важны для синтезов, поскольку моноалкенильные производные бора могут быть окислены щелочным раствором Н2О2 в альдегиды (если в исходном алкине тройная связь находиться на конце цепи) или в кетоны ( если тройная связь неконцевая)
2C4H9CºCH + R4B2H2 ® 2C4H9CH=CHB(R)2 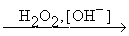 2C4H9CH=CH-OH ®
2C4H9CH=CH-OH ®
® 2C4H9CH2CHO

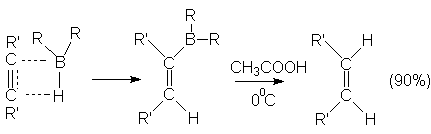
Моноалкенильные производные бора легко реагируют с уксусной кислотой в мягких условиях, образуя алкены. Весь этот процесс полностью стереоспецифичен, поскольку дизамещенные алкины дают только цис-алкены. Очевидно, что гидрид бора присоединяется к тройной связи цис-способом и образующийся моноалкенил бора реагирует далее с кислотой, образуя цис-алкен.
Реакции электрофильного присоединения.
- Присоединение галогенов (Cl2 и Br2)
Алкины, подобно алкенам, участвуют в реакциях присоединительного галогенирования. Отличие состоит лишь в том, что алкин можен присоединить две молекулы галогена, а алкен – только одну:
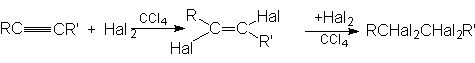
Промежуточный дигалогенид может быть получен присоединением одной молекулы галогена к алкину при низких температурах, причем реакция протекает преимущественно как транс-присоединение.
Реакции присоединения галогенов к алкинам как и другие реакции электрофильного присоединения, происходят медленнее, чем реакции присоединения к алкенам.
HCº C-CH2-CH=CH2 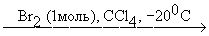 HCº C-CH2-CHBr-CH2Br (90%)
HCº C-CH2-CHBr-CH2Br (90%)
Такое соотношение реакционных способностей связано с различием устойчивости карбкатионов, образующихся при присоединении электрофильного реагента к кратным связям
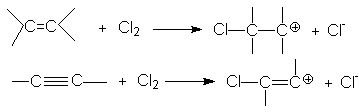
Можно видеть, что винил-катион менее устойчив по сравнению с алкил-катионом, поэтому образование последнего характеризуется более низким энергетическим барьером. В целом механизм галогенирования алкина (на примере бромирования) может быть представлен следующими стадиями:
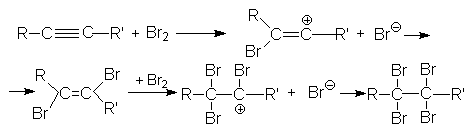
2. Присоединение галогеноводородов к алкинам.
Присоединение хлоро- и бромоводорода к алкинам протекает также, как и к алкенам. Реакция имеет ступенчатый характер.
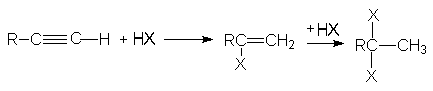
Обе реакции идут по правилу Марковникова. Показано, что присоединение галогеноводородов к алкинам идет как транс-присоединение. Поскольку реакционная способность тройной связи меньше чем у алкенов, используют катализ: например HgCl2.
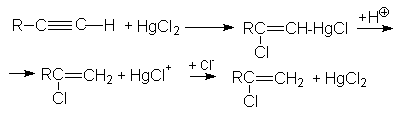
3. Реакция гидратации (Реакция Кучерова)

Механизм этой реакции можно представить последовательностью стадий:
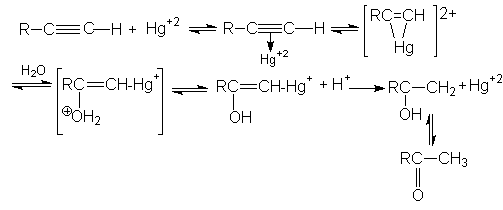
При синтезе ацетальдегида протекают побочные реакции:
а) альдольная конденсация
CH3CHO+CH3CHO 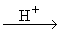 CH3CH(OH)CH2CHO
CH3CH(OH)CH2CHO 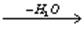 CH3CH=CH-CHO
CH3CH=CH-CHO 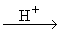 альдегидные смолы
альдегидные смолы
б) окисление
СH3CHO + 2Hg2+ 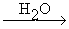 2Hg+ + CH3COOH + 2H+
2Hg+ + CH3COOH + 2H+
CH3CHO + Hg+ 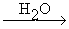 Hg + CH3COOH + 2H+
Hg + CH3COOH + 2H+
Подавление приведенных побочных реакций можно обеспечить путем увеличения скорости подачи ацетилена в реакционную зону. Благодаря этому образующийся альдегид отдувается из реакционной массы и степень его вовлечения в побочные реакции резко снижается.
4. Присоединение HCN.
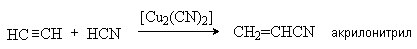
5. Присоединение спиртов.
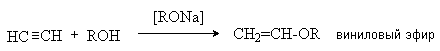
Кислотные свойства ацетилена и алкинов
с терминальной тройной связью.
Соединения этого типа являются С-Н – кислотами. Атом водорода, находящийся при углероде тройной связи обладает большей кислотностью, чем атом водорода алкенов и алканов. Объясняется это тем, что атомы Сº обладают большим s-характером и поэтому сильнее притягивают электроны, поэтому С-Н связи поляризованы и электроположительные атомы водорода в них проявляют большую кислотность. Кислотность ацетилена и a -алкинов проявляется в следующих реакциях:
RCº CH + K+NH2- 
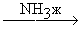 RCº C-K+ + NH3
RCº C-K+ + NH3
Амид-анион обладает высокой основностью, что обусловливает сдвиг равновесия в сторону образования ацетиленида. В то же время, вода, обладая более высокой кислотностью по сравнению с ацетиленом, вытесняет последний из ацетиленидов:
RCº CК + H2O ® RCº CH + КOH
Натриевые, калиевые и другие ацетилениды щелочных металлов являются истинными солями, состоящие из катиона металла и ацетиленид-анионов. Соли ацетиленов с тяжелыми металлами (Ag, Cu, Hg) – не в полном смысле соли. Это ковалентно-построенные соединения, нерастворимые в воде. Они осаждаются из водного раствора.
Осаждением ацетиленида серебра определяют наличие тройной связи или отделяют терминальные ацетилены от дизамещенных:
RCº CH + [Ag(NH3)2]NO3® RCº CAg + NH4NO3 + NH3
RCº CR' + [Ag(NH3)2]NO3 ® реакция не идет
Монозамещенные ацетилены тяжелых металлов легко регенерируют из осадка под действием сильных минеральных кислот.
RCº CAg + HNO3 ® RCº CH + AgNO3
Аналогичное использование находят ацетилениды меди
RCºCH + [Cu(NH3)2]Cl ® RCºC-Cu¯ + NH4Cl + NH3
RCºC-Cu + HCl ® RCºCH + CuCl
Ацетилениды магния (реактив ) имеют важное синтетическое значение. Их получают действием терминального алкина на магний органические соединения с предельными радикалами:
RCºCH + CH3MgI ® CH4 + RCºC-MgI
Благодаря этому реактиву можно получать спирты и карбоновые кислоты, содержащую тройную связь:
а) RCºC-MgI + CH2=O ® RCºC-CH2-OMgI 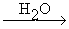 RCºC-CH2OH + Mg(OH)I
RCºC-CH2OH + Mg(OH)I
первичный спирт
б)
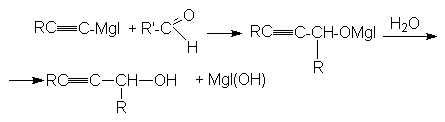
вторичный спирт
в)
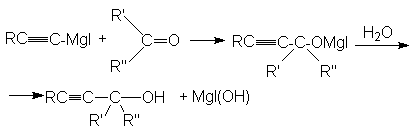
третичный спирт
г)
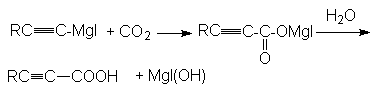
карбоновая кислота
Подобные синтезы можно осуществлять путем конденсации ацетилена или терминальных алкинов с альдегидами и кетонами (Фаворский)
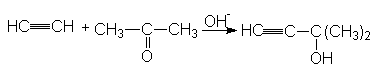
Механизм:
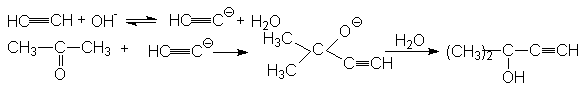
+ OH-
Конденсация ацетилена с альдегидами в присутствии щелочей не дает желаемого результата из-за побочной реакции альдольной конденсации. В.Реппе осуществил ее разработав новый катализатор на основе ацетиленида меди, стабилизированного соединениями висмута:
СHº CH + CH2O ® CHº CH-CH2OH 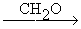 HO-CH2-Cº C-CH2-OH
HO-CH2-Cº C-CH2-OH
(бутиндиол-1,4)
Изомеризация алкинов
Алкины способны к изомеризации с перемещением кратной связи или с превращением в диеновые углеводороды.
Под действие щелочных металлов тройная связь переходит на конец молекулы полученного ацетиленида. Действие спиртовых щелочей способствует переходу тройной связи с конца молекулы в центр. Промежуточными продуктами в этих превращениях являются алленовые углеводороды (Фаворский)
CH3CH2CºCH 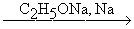 CH3CºCCH3
CH3CºCCH3
Окисление
RCº CR' + KMnO4  RCOOH + R'COOH
RCOOH + R'COOH
RCºCH 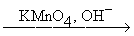 RCOOH + CO2
RCOOH + CO2
RCºCR' 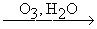 RCOOH + R'COOH
RCOOH + R'COOH
Окислительная конденсация терминальных алкинов.
2RCºCH 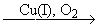 RCºC-CºCR
RCºC-CºCR
Полимеризация
1) Реакция Зелинского:
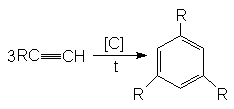
2) Димеризация:
2HCºCH 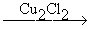 HCºC-CH=CH2
HCºC-CH=CH2 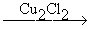 H2C=CH-CºC-CH=CH2
H2C=CH-CºC-CH=CH2
винилацетилен дивинилацетилен
Карбонилирование (Реппе)
CHºCH + CO + H2O ® CH2=CH-COOH акриловая кислота
CHºCH + CO + ROH ® CH2=CH-COOR эфир акриловой кислоты
CHºCH + CO + NH3® CH2=CH-CONH2 амид акриловой кислоты
Катализаторами этих реакций являются карбонилы никеля и кобальта.