 |
|
Б. Обследование детей раннего возраста 3 страница



 Тромбин (IIa) XIII XIIIa
Тромбин (IIa) XIII XIIIa
 | |||||
 |  | ||||
Фибриноген
 Фибрин-мономер + фибринопептиды А и В +
Фибрин-мономер + фибринопептиды А и В +
комплексы
 Фибрин S XIIIa
Фибрин S XIIIa
 Первичный красный тромб
Первичный красный тромб
 (сгусток)
(сгусток)

 | |||||||||
 |   | ||||||||
 |  | ||||||||
Спонтанный Ретракция
фибринолиз
|
|
|
Третья Окончательный Сыворотка
фракция тромб (сгусток)
(форменные
элементы
крови)
Рис. 4. Схема свёртывания крови
(по Е.П.Иванову, 1983, с нашими дополнениями)

 Примечание. Сплошные стрелки активирующее действие; пунктирные стрелки превращение факторов в активную форму.
Примечание. Сплошные стрелки активирующее действие; пунктирные стрелки превращение факторов в активную форму.
1.3.2. Классификация геморрагического синдрома новорождённых
Классификация ГСН.
I. Первичные геморрагические расстройства:
1). Геморрагическая болезнь новорождённых (ГрБН).
2). Наследственные коагулопатии (гемофилия, афибриногенемия и др.).
3). Тромбоцитопенические пурпуры:
- врождённые – аллоиммунная (изоиммунная) и трансиммунная;
- наследственные – синдром Вискотта-Олдрича, гипо- или аплазия мегакариоцитарного ростка и др.;
- гетероиммунные.
4). Тромбоцитопатии:
- врождённые медикаментозные (на фоне лечения матери в последние сроки гестации салицилатами, индометацином, антиконвульсантами и другими тромбоцитарными ингибиторами);
- наследственные тромбоцитопатии.
II. Вторичные геморрагические расстройства:
1). ДВС-синдром.
2). Тромбоцитопенический и коагуляционный геморрагический синдром при инфекциях и гепатитах.
3). Витамин-К-дефицитный геморрагический синдром при механических желтухах.
4). Медикаментозный тромбоцитопатический синдром.
1.3.3. Геморрагическая болезнь новорождённых (ГрБН)
Частота ГрБН составляет от 0,25-0,5 % до 1,1 %, или 1:200 – 1:400 новорождённых. В США с 1960 г. всем новорождённым в первые часы жизни вводят витамин «К1» (филлохинон), благодаря чему снизилась частота ГрБН до 0,01 %.
Этиология. Витамин «К» плохо проникает через плаценту от матери к плоду. Дефицит витамина «К» способствует синтезу в печени новорождённого ребёнка неактивных факторов крови II, VII, IX и X (PIVKA – Protein induced by vitamin K-absence), которые не могут связывать ионы Ca2+ и полноценно включаться в известную каскадную систему свёртывания крови. PIVKA лабораторно обнаруживаются даже у внешне здоровых доношенных новорождённых детей. ГрБН развивается на 2-5 день жизни (реже позднее) и связана с резким снижением (< 10 %) К-витаминзависимых факторов.
Предрасполагающие факторы для развития ГрБН:
1. Гестозы с низкой эстрогенной активностью (выделение эстрогенов с мочой < 10 мг/сут).
2. Приём беременной женщиной в последние сроки гестации антикоагулянтов непрямого действия (из группы неодикумарина), а также нестероидных противовоспалительных препаратов (индометацина, аспирина), антиконвульсантов (фенобарбитал, дифенин и др.), больших доз антибиотиков широкого спектра действия (ампициллина, карбенициллина, цефалоспоринов, рифампицина и др.), изониазида.
3. Патология печени и кишечника у матери.
4. Недоношенность, ЗВУР.
5. Диареи у новорождённых детей.
6. Лечение новорождённых антибиотиками, подавляющими микрофлору в кишечнике, которая синтезирует витамин «К» (цефалоспорины III генерации и др.).
7. Грудное вскармливание (в женском молоке низкое содержание витамина «К» - 2 мкг/л).
8. Внутриутробные инфекции (часто поражается печень).
9. Полное парентеральное питание.
Таблица 6
Международная номенклатура факторов свёртывания крови
| Факторы | Синонимы | Содержание в плазме | Полупериод распада (в часах) |
| I II III IV V VI VII VIII IX X XI XII XIII | Фибриноген* Протромбин* Тканевой тромбопластин Ионы кальция Проакселерин* (лабильный) Исключен из употребления, т.к. является активной формой V ф. Проконвертин* (стабильный) Антигемофильный фактор (AHF) А Кристмас-фактор, плазменный тромбопластиновый компонент (РТС), антигемофильный глобулин В* Фактор Стюарт-Проуэра* Плазменный предшественник тромбопластина, РТА, антигемофильный фактор С Фактор Хагемана, фактор контакта Фибриназа, фибринстабилизирующий фактор, фактор Лаки-Лоранда | 2,0 – 3,5 г/л 0,07 г/л - 0,09 – 0,10 г/л 12 – 17 ед/мл - 0,05 г/л 0,03 – 0,05 г/л - - 0,50 – 1,85 - 0,019 г/л | 72 – 120 48 – 96 - - 15 –18 - 4 – 6 7 - 8 15 – 30 30 – 70 30 – 70 50 – 70 |
| Дополнительные: Виллебранда Флетчера Фитцжераль-да | VIII – ф.В Прекалликреин плазменный Кининоген плазменный | - - - | 18 – 30 - - |
Примечание. * - продуцируются в печени; витамин-К-зависимые факторы II, VII, IX, X.
Клиническая картина ГрБН
Различают три вида ГрБН:
1) ранняя (в первые 24 часа жизни);
2) классическая (на 1-7 сутки жизни);
3) поздняя (на 2-8 нед жизни, иногда до 6-месячного возраста).
1. Ранняя ГрБНпроявляется при рождении геморрагиями на коже, кефалогематомой, внутричерепными кровоизлияниями на фоне тяжёлой асфиксии или родовой травмы (обнаруживаются при УЗИ мозга). Возможны лёгочные кровотечения, геморрагии в надпочечники, селезёнку, печень, мелена.
2. Классическая ГрБН диагностируется в виде:
- мелены и кровавой рвоты (гематемезис);
- экхимозов и петехий на коже;
- кровотечений из пупочной ранки после хирургического иссечения или отпадения пуповинного остатка;
- носовых кровотечений;
- кефалогематомы;
- внутричерепных кровоизлияний;
- внутренних гематом;
- лёгочных кровотечений и др.
Мелена – это кишечное кровотечение, связанное с образованием язвочек на слизистой оболочке желудка и кишечника после родового стресса (избыток глюкокортикоидов в крови новорождённого). Кроме того, в генезе мелены играют роль ишемия желудка и кишечника, повышенная кислотность желудочного сока, пептический рефлюкс-эзофагит. Часто мелена сочетается с кровавой рвотой. Могут быть рецидивы мелены. При дифференциальной диагностике мелены и «синдрома заглоченной крови» проводят тест Апта: при смешивании надосадочной жидкости рвотных масс или мекония с 1 % раствором NaOH в соотношении 4:1 изменение цвета на коричневый укажет на присутствие в жидкости крови матери, содержащей HbA, а сохранение розового цвета означает наличие щёлочно-устойчивого HbF крови ребёнка. При рецидиве мелены, обильном кровотечении из ануса следует исключить ангиоматоз кишечника, папилломы и другую патологию хирургического профиля. Большие кровопотери приводят к анемии.
3. Поздняя ГрБН проявляется в конце периода новорождённости обширными и глубокими экхимозами и внутричерепными кровоизлияниями, значительно реже кровотечениями из желудочно-кишечного тракта и гематомезисом. Основным в генезе поздней ГрБН является нарушение абсорбции витамина «К» из кишечника, где он синтезируется бактериями (менахинон – витамин «К2») или поступает с растительной пищей (филлохинон – витамин «К1»). Дефицит витамина «К» развивается при:
- диареи с мальабсорбцией жиров в течение более 1 недели;
- атрезии жёлчевыводящих путей, гепатитах и холестазах;
- муковисцидозе, целиакии, дефиците α1-антирипсина;
- дисбактериозе в результате продолжительной антибиотикотерапии.
Поздняя ГрБН встречается преимущественно у детей, находящихся на грудном вскармливании.
Диагностика ГрБН (рис. 5).
I. Выявление факторов риска ГрБН.
II. Наличие клинических проявлений ГрБН.
III. Лабораторные данные (табл. 7):
1). Подсчёт количества тромбоцитов (нормальное число 150-400∙109/л).
2). Уровень протромбина (протромбиновый тест, ПТ) <10 % уровня взрослых.
3). Протромбиновое время (ПВ) по Quck (1935) увеличено(в норме 13-16 с), протромбиновый индекс (ПИ) > 40 %.
4). Парциальное тромбопластиновое время (ПТВ) удлинено (в норме 45-65 секунд).

 |  |  |  | ||||
|
|
|
|





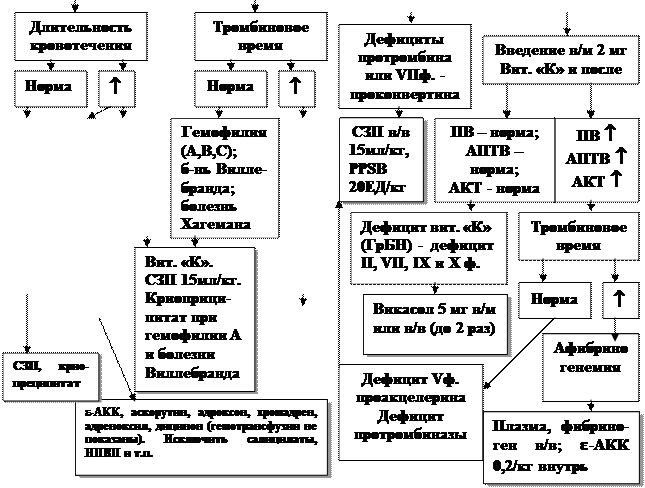
Рис. 5. Диагностико-лечебный алгоритм при кровоточивости
у клинически «здоровых» детей.
Таблица 7
Лабораторная диагностика геморрагического синдрома у новорождённых
| Болезни и синдромы | Количест- во тром-боцитов (в норме 200-400·109/л) | Парциаль-ное тром-бопласти-новое вре-мя (в нор-ме 45-65 с) | Потреб- ление протромбина, в норме 95-100 % | Протром-биновое время (в норме 13-20 с) | Фибрино-лиз (в норме 65-120 мин) | Дополни-тельные исследования |
| «Здоровые» дети | ||||||
| ГрБН | Норма | Увеличено | Норма | Увеличено | Норма | - |
| Гемофилия | Норма | Увеличено | Снижено | Норма | Норма | ↓ ф. VIII или ф. IX |
| Тромбоцитопении | Снижено | Норма | Несколько снижено | Норма | Норма или повышен | + тесты на антитром-боцитарные антитела у матери |
| Тромбоцитопатии | Норма | Норма | Норма или несколько снижено | Норма | Норма | Нарушены адгезивно- аггрега- ционные свойства и морфология тромбоцитов |
| Больные дети | ||||||
| ДВС-синдром (II и III стадии) | Снижено | Увеличено | Снижено | Увеличено | Повышен, т.е. время лизиса укорочено | + ЭТ, ПСТ, фрагмен- тированные эритроциты, фибриногенопения, ↓ ф.VIII, + ПДФ, ↑ ТВ не коррегируемое плазмой здорового донора |
| Недоста-точность белково-синтети-ческой функции печени | Норма | Увеличено | Снижено | Увеличено | Снижен, т.е. время лизиса увеличено | Часто ги-пербили- рубинемия, гипоальбу-минемия, гипоглик- емия |
5). Активированное парциальное тромбопластиновое время (АПТВ) по Coen et al.
6). Тромбиновый тест по Biggs, McFarlane (1962). Тромбиновое время (ТВ) нормальное (10-16 с).
6). Определение количества фибриногена кинетическим методом по Clauss (1957). Фибриноген в норме (1,5-3 г/л).
7). Определение растворимого фибрина с помощью ОФТ-теста. Продукты деградации фибриногена (ПДФ) в норме (0-7 мг/мл).
8). Микрокоагуляционный тест (МКТ) <10 %.
9). Агрегационная функция тромбоцитов.
10). Определение активности протеина С.
11). Определение фибринолитической активности крови (XIIа-зависимой).
1.3.4. Дифференциальная диагностика ГрБН и ГСН
I.Исключить «фоновые» заболевания, сочетающиеся с гипопродукцией витамин-К-зависимых факторов и геморрагическим синдромом (внутриутробные инфекции, сепсис, респираторный дистресс-синдром у недоношенных и др.).
II.От синдрома «заглоченной материнской крови» (тест Апта).
III. ДВС-синдром (рис. 6) характеризуется образованием внутрисосу-дистых микротромбов с потреблением в них прокоагулянтов и тромбоцитов, а также патологическим фибринолизом с развитием кровоточивости из-за дефицита гемостатических факторов (табл. 9 и 10). У новорождённых ДВС-синдром может сопровождать заболевания с осложнениями в виде сердечно-сосудистого коллапса или шока (бактериальный сепсис, генерализованный кандидоз, TORCH-инфекция, тяжёлая асфиксия в родах, постгеморрагический шок, холодовая травма, дегидратационный шок, РДС, пневмонии, лёгочные геморрагии, полицитемия, молниеносная пурпура, некротизирующий энтероколит, повреждения мозга с некрозами и геморрагиями, гемолитическая болезнь новорождённых, гепатиты, гигантская гемангиома).
Предрасполагают к развитию ДВС-синдрома у новорождённых:
1. Низкая белково-синтетическая способность печени в производстве про- и антикоагулянтов.
2. Слабая функциональная способность моноцитарно-макрофагальной системы (РЭС в старой трактовке).
3. Особенности системы микроциркуляции (трудность поддержания адекватной перфузии в микрососудах).
4. Низкий уровень антитромбина III и плазминогена у недоношенных детей.
Клинические проявления ДВС-синдрома:
1. Длительное кровотечение из мест инъекций.
2. Пурпура в виде экхимозов, некрозы кожи.
3. Острая почечная недостаточность (ОПН).
4. Спонтанные кровотечения (лёгочные, кишечные, носовые).
5. Кровоизлияния во внутренние органы и головной мозг.
6. Типично волнообразное течение.
Лабораторные показатели системы гемостаза при ДВС-синдроме:
- снижено число тромбоцитов (тромбоцитопения < 100 ·109/л);
- в 2 раза по сравнению со здоровыми детьми удлинены ПВ, время свёртывания (МА) в МКТ, тромбиновое время (ТВ), парциальное тромбопластиновое время (ПТВ);
- снижен уровень фибриногена (ф. I < 1,5 г/л), проакселерина (ф. V), АГГ(ф.VIII), антитромбина III(< 50 % норматива);
- положительные паракоагуляционные тесты (ОФТ – ортофенантроли-новый тест, ЭТ – этаноловый тест, ПСТ – протаминсульфатный тест);
- ПДФболее 10 мг/мл;
- положителен тест склеивания стафилококков (отражает соотношение растворимых фибринмономерных комплексов к ПДФ).
Из-за трудности забора крови, у новорождённых при ДВС-синдроме достаточно провести 4 исследования: число тромбоцитов, МКТ, ПВ и ТВ (табл. 7).

Рис. 6. Диагностико-лечебный алгоритм при кровоточивости
у больных новорождённых детей.
IV. При гемофилии А (дефицит ф. VIII ) и В (дефицит ф. IX) удлиняется МА в МКТ (дефицит внутреннего звена гемокоагуляции), ПТВ увеличено (см. табл. 7), остальные показатели гемостаза в норме (см. рис. 5). Кровоточивость при гемофилии очень редко манифестирует в периоде новорождённости по сравнению с ГрБН.
V. Наследственный дефицит VII ф. (проконвертина) определяется по следующим гемостазиологическим тестам:
1. Удлинение времени свёртывания в протромбиновом тесте (ПТ) при нормальных параметрах МКТ.
2. Коагуляционные пробы с ядами гюрзы и эфры не нарушаются, а при ГрБН в этих пробах выявляется гипокоагуляция.
3. Нарушения показаний ПТ стабильно и не устраняется внутривенным введением препаратов витамина «К», а при ГрБН имеется положительный эффект от викасола.
4. Протромбиновое время (ПВ) удлинено и коррекционный эффект после трансфузии свежей плазмы сохраняется короткое время, т.к. период полувыведения ф.VII составляет 2-6 ч, тогда как при дефиците ф. Х и ф. V этот эффект длится 24-48 ч, а при дефиците протромбина – более 3 суток.
VI. Наследственные дефициты ф. Х (фактора Стюарта-Прауэра), ф. V (проакселерина) или ф. II (протромбина) встречаются очень редко. При этих болезнях, также как и при ГрБН, увеличены показания ПТ и МКТ. Эти нарушения стабильны и введение викасола не дает эффекта. Яд гюрзы вызывает свертывание, активируя ф. Х, а яд эфры активирует ф. II (см. табл. 8).
Таблица 8
Дифференциальная диагностика различных видов дефицита
витамин-К-зависимых факторов с использованием тестов
со змеиными ядами
| Заболевания | Показания коагуляционных тестов с ядами | |
| гюрзы | эфры | |
| ГрБН | Нарушение | Нарушение |
| Дефицит VII ф. | Норма | Норма |
| Дефицит Х ф. | Нарушение | Норма |
| Дефицит II ф. | Норма | Нарушение |
VII. Наследственный дефицит ф. XIII (афибриназемия, или отсутствие фибринстабилизирующего фактора, или отсутствие трансглутаминазы) проявляется тяжелой кровоточивостью у 90 % больных (при дефиците ф. XIII < 1 %). Характерны нормальные показатели всех коагуляционных тестов и вместе с тем растворимость образовавшихся сгустков в 6-7 М растворе мочевины происходит в течение часа, чего не отмечается при ГрБН.
VIII. Тромбоцитопении у новорождённых (табл. 9) развиваются при снижении числа тромбоцитов в крови менее 100-150·109/л.
1. При аллоиммунной (изоиммунной)тромбоцитопенической пурпуре (АТП) происходит тромбоцитолиз у плода, т.к. в сенсибилизированном организме матери появляются антитромбоцитарные антитела, проникающие через плаценту. Обычно мать в этом случае не имеет тромбоцитарного антигена PLа1, а у плода он унаследован от отца.
Среди человеческой популяции PLa1 встречается в 98 %, а отрицательными являются 2 %. Конфликт по пластинчатому антигену развивается уже при первой беременности. Клинически АТП протекает в виде обильных петехий и экхимозов. Редко встречаются мелена и носовые кровотечения. Геморрагии появляются в первые дни жизни. Наиболее опасны кровоизлияния в мозг (до 30 % случаев), которые могут быть и антенатальными. У 20 % детей с АТП развивается желтуха. Летальность составляет 10-15 %. Наиболее тяжёлое течение при поздней манифестации АТП после рождения. Длительность АТП до 2-10 нед. Геморрагический синдром обычно купируется в первые часы жизни. Диагностируют АТП при положительной реакции агглютинации тромбоцитов новорождённых в сыворотке крови матери.
Таблица 9
Дифференциальная диагностика трёх видов
геморрагического синдрома у новорождённых
| Параметры гемостаза | ГрБН | ДВС-синдром | Тромбоцито- пении |
| Количество тромбоцитов | Нормальное | Сниженное | Сниженное |
| Протромбиновое время | Удлинено | Удлинено | Нормальное |
| Время свертывания (МА) в МКТ | Удлинено | Удлинено | Нормальное |
| Тромбиновое время | Нормальное | Удлинено | Нормальное |
| Паракоагуляционные тесты (ОФТ, ЭТ, ПСТ) | Отрицатель-ные | Положитель-ные | Отрицательные |
| Тест склеивания стафило-кокков | Норма | Повышенное содержание РФМК/ПДФ | Норма |
Примечания. МА в МКТ – время свёртывания в микрокоагуляционном тесте (внутренний механизм гемокоагуляции), ОФТ – ортофенантролиновый тест, ЭТ – этаноловый тест, ПСТ – протаминсульфатный тест, РФМК/ПДФ – соотношение растворимых фибринмономерных комплексов к продуктам деградации фибриногена, ГрБН – геморрагическая болезнь новорождённых.