 |
|
Основні положення МКТ.
На початку минулого століття англійський учений Д.Дальтон показав, що більшість закономірностей явищ природи можна пояснити, використовуючи уявлення про атоми і молекули, і науково обґрунтував молекулярну будову речовини. На початок нашого століття була врешті побудована і підтверджена багатьма дослідами МКТ будови речовини.
МКТ – вчення, що пояснює будову і властивості тіл рухом і взаємодією атомів, молекул і іонів, з яких складаються тіла.
В основі МКТ лежать 3 найважливіших положення, які повністю підтверджені експериментально і теоретично.
І положення:
Всі тіла складаються з частинок – атомів, молекул і іонів, в склад яких входять ще менші частинки, які умовно називають елементарними.
Молекулою(від латинського „молес” – маса, „кула” – зменшувальний суфікс) називають найменшу частинку речовини, здатну до самостійного існування, яка зберігає хімічні властивості цієї речовини.
Молекули складаються з атомів(від грецького „атомос” – неподільний). Якщо при деякому явищі природи молекули залишаються незмінними, то речовина зберігає свої хімічні властивості.
Якщо ж молекули змінюють свою будову чи розпадаються на окремі атоми, що утворюються нові види речовини з іншими хімічними і фізичними властивостями.
Речовини, які не можна розкласти на більш прості складові частини, називаються хімічними елементами. Кожному хімічному елементу відповідають атоми, які мають певне місце (номер) в таблиці Мендєлєєва.
Кількість сортів(видів) атомів порівняно невелика і дорівнює числу хімічних елементів та їх ізотопів(на сьогодні відомо 108 елементів і  1,5 тисячі ізотопів).
1,5 тисячі ізотопів).
Різні комбінації цих атомів і створюють всю множину видів молекул. Молекули, що утворюють дану речовину, однакові, але відрізняються швидкостями.
Різні речовини складаються з різних молекул. Молекули характеризуються певними константами. До них відносяться розміри молекули; число Авогадро і маса молекул. Розміри молекул мають порядок 1 ангстрема.

Розмір молекул становить деяку умовну величину. Дійсно, молекула має певну форму, але оточена складним електромагнітним полем, яке простягається нескінченно, проте швидко зменшується з відстанню і на деякій відстані ним можна знехтувати. Ця відстань і називається радіусом молекули, а молекулі приписують форму кулі. Розміри атомів і молекул мають в середньому порядок  . Розроблено значну кількість методів, за допомогою яких можна досить точно визначити розміри і масу молекули. Але ці способи, як правило, досить складні і громіздкі.
. Розроблено значну кількість методів, за допомогою яких можна досить точно визначити розміри і масу молекули. Але ці способи, як правило, досить складні і громіздкі.
Маси молекул дуже малі(у звичних для нас масштабах). Наприклад, маса молекули кисню
 г
г
 г
г
 г
г
Тому була введена нова додаткова одиниця вимірювання – атомна одиниця маси.
Атомною одиницею маси називається  маси ізотопу вуглецю
маси ізотопу вуглецю  .
.
Маса молекули(атома), виражена в атомних одиницях маси, називається відносно молекулярною(атомною) масою А. Вона показує у скільки разів маса молекули речовини більша  маси ізотопу вуглецю
маси ізотопу вуглецю  .
.
Атомна одиниця маси

 кг
кг
Отже, масу молекули можна знайти за відомою відносною молекулярною масою.
 кг
кг
Атоми різних хімічних елементів мають різну атомну масу, тому, наприклад, в 1 кг свинцю Pb і в 1 кг алюмінію Al міститься різна кількість атомів.
Тому для кількісної характеристики однорідних тіл по кількості атомів і молекул, що містяться в них, вводиться поняття кількості речовини.
Кількістю речовини називається фізична величина, що визначається кількістю специфічних структурних елементів, атомів, молекул або іонів, - з яких складається речовина. Так як маси окремих структурних елементів, наприклад, молекул, відрізняються, то однакові кількості різних речовин мають різну масу. Підкреслимо, що маса не є мірою кількості речовини.
В СІ за одиницю вимірювання кількості речовини прийнято 1 моль – кількості речовини, що містить стільки ж молекул(атомів), скільки атомів міститься в 0,012 кг вуглецю  .
.
Кількість атомів чи молекул, що містяться в 1 молі речовини, називається числом Авогадро(  ).
).
 моль-1
моль-1
Визначення числа Авогадро відноситься до числа особливо важливих подій в зв’язку з тим, що це число безпосередньо пов’язано з існуванням атомної будови речовини. Число Авогадро пов’язує мікроскопічний масштаб з макроскопічним, бо моль будь якої речовини як правило містить тіло звичних для нас розмірів, тобто макротіло. Наприклад, при нормальному атмосферному тиску і  , моль будь якого газу займає об’єм
, моль будь якого газу займає об’єм 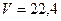 л.
л.
Масу однієї молекули чи атома можна отримати із співвідношення
 (1)
(1)
 (2)
(2)
ІІ положення:
Між частинками любого тіла(атомами, молекулами і іонами) одночасно діють сили взаємного притягання і сили взаємного відштовхування.
Закони сил, що діють між атомами, молекулами і іонами, зовсім не схожі на кулонівські, хоча ці сили врешті мають електромагнітне походження. Точний вигляд закону взаємодії частинок такого роду дуже складний. Зокрема, сила їх взаємодії виявляється залежно не тільки від відстані між частинками, що взаємодіють, але і від їх взаємної орієнтації. Однак, в більшості випадків достатньо знати силу взаємодії, середню по всім їх можливим орієнтаціям.
Закон дії усереднених сил виявляється порівняно простим і має вигляд:
1) для сил притягання
 (2)
(2)
2) для сил відштовхування
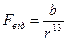 (3)
(3)
де a і b – коефіцієнти пропорційності, що залежать від будови молекул, які взаємодіють.
Одночасне існування сил притягання і відштовхування означає, що на молекулу діє рівнодійна сила міжмолекулярної взаємодії.
 |
Одну молекулу вважаємо нерухомою і розміщеною в початку системи координат  , а друга молекула змінює свою відстань відносно першої вздовж осі
, а друга молекула змінює свою відстань відносно першої вздовж осі  .
.
Величина сил міжмолекулярної взаємодії не залежить від загального числа молекул. Наприклад, густина або пружні властивості рідини і твердих тіл не залежать від розмірів дослідного зразка: крапля води і вода в Дніпрі за однакової температури і однакового зовнішнього тиску мають рівну густину і стискуваність. Ця властивість міжмолекулярних сил називається насичуваністю. Цим міжмолекулярні сили принципово відрізняються від гравітаційних чи кулонівських сил, для яких рівнодійна визначається дією всіх тіл, що входять в систему.
Сили міжмолекулярної взаємодії мають електромагнітну природу, зумовлену тим, що молекули складаються із електрично заряджених частинок, яки властива взаємодія.
Правда, в цілому молекула електрично нейтральна, однак заряди в молекулі розміщуються в процесі її наближення до іншої молекули несиметрично.
Завдяки цьому молекули виявляються полярними, подібними електричним диполям: між різнойменно зарядженими полюсами виникають сили притягання, що переважають сили відштовхування однойменних „полюсів”.
Якщо ж молекули дуже близько підійдуть одна до одної, то вирішальну роль в їх взаємодії починають відігравати сили відштовхування між електронними оболонками атомів, що складають цю молекулу.
ІІІ положення:
Атоми, молекули і іони перебувають в неперервному хаотичному русі.
Хаотичний рух частинок, що утворюють макроскопічне тіло, називається тепловим. Тепловий рух визначає внутрішній стан кожного макроскопічного тіла. За винятком особливих випадків, які мають місце в квантовій фізиці, тепловий рух є нерелятивістським, тобто швидкість молекул набагато менше швидкості світла.
Відмітимо, що про тепловий рух можна говорити тільки в тих випадках, коли розглядувана фізична система є макроскопічною.
Не має сенсу вести мову про тепловий рух, коли система, наприклад, складається з однієї чи кількох молекул(атомів чи іонів).
Знаходячись у стані неперервного хаотичного руху молекули „зтикаються” одна з одною і змінюють свою швидкість як за напрямком, так і за величиною.
Правда, зіткнення при цьому у звичайному розумінні цього слова не відбувається, бо безпосередньому зтиканню молекул заважають сили відштовхування, що різко зростають при їх наближенні. Але дія цих сил приводить до того ж результату, що при звичайному зіткненні, тобто відскакуванню молекул, що наблизились, одна від одної.