 |
|
Розподіл числа молекул за швидкостями(розподіл Максвела).
Серед квадратична швидкість – менше статистична характеристика руху молекул, отримана шляхом усереднення різних значень швидкостей значної кількості молекул.
В дійсності ж молекули рухаються з різними швидкостями  навіть при деякий заданій температурі
навіть при деякий заданій температурі  .
.
Розіб’ємо весь діапазон цих швидкостей на малі інтервали  . Тоді на кожний інтервал швидкості буде припадати деяке число молекул
. Тоді на кожний інтервал швидкості буде припадати деяке число молекул  , що мають швидкість, обмежену цим інтервалом. Відношення
, що мають швидкість, обмежену цим інтервалом. Відношення 
 показує, скільки молекул припадає на кожний одиничний інтервал швидкості. Іншими словами, який розподіл числа молекул за швидкостями.
показує, скільки молекул припадає на кожний одиничний інтервал швидкості. Іншими словами, який розподіл числа молекул за швидкостями.
 залежить від швидкості і називається функцією розподілу числа молекул за швидкостями.
залежить від швидкості і називається функцією розподілу числа молекул за швидкостями.
Цю функцію розподілу вперше визначив англ. фізик Джеймс Клерк Максвелл теоретичним шляхом, застосувавши теорію ймовірностей.
Максвелівська функція розподілу представлена формулою, яка називається законом Максвела і має такий вид:
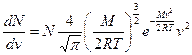 (1)
(1)
де 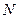 - загальна кількість молекул газу
- загальна кількість молекул газу
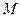 - молярна маса
- молярна маса
 - універсальна газова постійна
- універсальна газова постійна
При  і при
і при  функція розподілу прагне до нуля.
функція розподілу прагне до нуля.
Знайдемо найбільш ймовірну швидкість, при якій функція розподілу має максимум.
Для цього першу похідну функції розподілу по  прирівняємо до нуля.
прирівняємо до нуля.
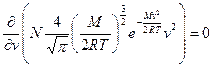


 при
при  не має фізичного змісту
не має фізичного змісту

 (2)
(2)
Найбільш ймовірною називається швидкість, поблизу якої на одиничний інтервал припадає найбільша кількість молекул.
Вона розраховується за формулою (2).
Графічно закон Максвела представлено кривою, що починається в початку координат, досягає максимуму при  і потім асимптотично наближається до осі абсцис(мал.1).
і потім асимптотично наближається до осі абсцис(мал.1).





Графік точно показує, що молекул з малими і великими швидкостями мало і що більшість молекул має швидкості, близькі до найбільш ймовірної швидкості.
Із закону Максвелла можна отримати вираз для середньої арифметичної швидкості  .
.
Вона дорівнює




Ці вирази показують, що дані швидкості розрізняються між собою тільки коефіцієнтами:

Виділимо на осі абсцис елементарний інтервал швидкостей  і проведемо ординати його меж. Тоді площа дуже вузького прямокутника дорівнюватиме
і проведемо ординати його меж. Тоді площа дуже вузького прямокутника дорівнюватиме
 ,
,
тобто числу молекул, що мають швидкість в інтервалі  . Отже, площа, обмежена кривою розподілу і віссю абсцис дорівнює загальній кількості молекул газу
. Отже, площа, обмежена кривою розподілу і віссю абсцис дорівнює загальній кількості молекул газу 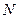 .
.
При зміні температури газу змінюються швидкості руху всіх молекул, а отже і найбільш ймовірна швидкість. Тому максимум кривої буде зміщуватись вправо, при підвищені температури, або вліво при зниженні температури, однак площа, обмежена кривою, залишається незмінною, бо загальна кількість молекул газу не залежить від температури.
Розподіл Максвелла за швидкостями був підтверджений експериментально німецьким фізиком Штерном у 1920 р.