 |
|
И ДЕТЕЙ РАННЕГО ВОЗРАСТА
Классификация врождённой и приобретённой кишечной непроходимости приведена в таблице 20.
У новорождённых детей отмечается высокая частота динамической кишечной непроходимости, обусловленной вегетативной дисфункцией и водно-электролитными нарушениями (гипо- и гиперкалиемия, дегидратация), при которых отсутствуют перистальтические сокращения кишечника, что задерживает пассаж кишечного содержимого. Выделяют паралитическую и спастическую динамическую непроходимость.
Паралитическая (паретическая) непроходимость кишечника возникает рефлекторно при многих заболеваниях с инфекционным токсикозом (абсцедирующая пневмония, стеноз устья мочеточников, пузырно-мочеточниково-лоханочный рефлюкс, менингит, внутричерепная гипертензия, диабетический псевдоперитонит).
Спастическая непроходимость кишечника у детей встречается редко и проявляется у новорождённых детей при гипоксически-ишемической энцефалопатии (церебральной ишемии).
Механическая кишечная непроходимость обусловлена пороками развития пищеварительного тракта (атрезии, стенозы и др.), заболеваниями с закупоркой (обтурацией) просвета кишечника (например, мекониевый илеус встречается в 10-20 % случаев кишечной формы муковисцидоза) или сдавлением кишечной трубки извне (завороты, сосудистые аномалии, внутрибрюшные перетяжки, спайки, перекруты, опухоли). Во всех случаях механической кишечной непроходимости, в результате нарушения кровоснабжения кишки, некроза и перитонита при отсутствии лечения, она переходит в паралитическую кишечную непроходимость. Промежуточная фаза обозначается как смешанная кишечная непроходимость.
Если препятствия для кишечного содержимого локализуются в области duodenum, то диагностируют высокую кишечную непроходимость. Для неё характерна нечастая обильная рвота содержимым желудка (возможно и с желчью) с первых суток (часов) жизни. Объём рвотных масс может превышать количество съеденной пищи. Возможно быстрое развитие обезвоживания или аспирационной пневмонии. Регистрируется вздутие живота в эпигастрии и его западение в остальных отделах. Меконий отходит малыми порциями в течение 5-6 суток, но в последующие дни стула не отмечается.
Низкая кишечная непроходимость выявляется в области тонкой, подвздошной и толстой кишок (преимущественно тонкокишечная). Характерна частая «каловая рвота» и вздутие живота, которое не исчезает после опорожнения желудка. Меконий не отходит, а только иногда выделяется небольшое количество зеленоватой слизи. Развивается интоксикация, а при поздней диагностике присоединяется перитонит. Врождённая низкая кишечная непроходимость преимущественно бывает полной, поэтому показана экстренная хирургическая операция.
Таблица 20
Классификация врождённой и приобретённой кишечной
непроходимости (Красовская Т.В., Кобзева Т.Н., 2001)
| Врождённая | Приобретённая | ||
| Механическая | Механическая | Динамическая | |
| А. Полная | |||
| I. Странгуляционная | |||
| Высокая | Низкая | Низкая | Низкая |
| 1. Синдром Ледда 2. Заворот средней кишки 3. Ущемлённая грыжа Трейца | 1. Заворот изолированной кишечной петли 2. Ущемлённая внутренняя грыжа | 1. Ущемлённые наружные грыжи 2. Заворот кишечной петли 3. Спаечная кишечная непроходимость (поздняя) 4. Инвагинация | I. Спастическая 1. Вегетативная дисфункция 2. Постгипоксичес-кая II. Паралитическая при заболеваниях: 1.Некротический энтероколит 2. ОРВИ 3. Пневмония 4. Отит 5. Менингит 6. Сепсис 7. Перитонит |
| II. Обтурационная | |||
| 1. Атрезия привратника 2. Атрезия duodenum 3. Кольцевидная поджелудочная железа 4. Аномальные сосуды | 1. Атрезия тонкой и толстой кишок 2. Энтерокистомы 3. Болезнь Гиршпрунга 4. Микониевый илеус | 1. Спаечная кишечная непроходимость (ранняя) | |
| Б. Частичная | |||
| I. Странгуляционная | |||
| 1. Варианты незавершенного поворота кишечника | - | 1. Спаечная кишечная непроходимость (поздняя) | |
| II. Обтурационная | |||
| 1. Пилоростеноз 2. Перегиб желудка 3. Стеноз duodenum 4. Кольцевидная поджелудочная железа 5. Аномальные сосуды | 1. Стеноз тонкой и толстой кишок 2. Энтеростомы 3. Болезнь Гиршпрунга | 1. Спаечная кишечная непроходимость (ранняя) |
1. Спастическая непроходимость кишечника при поражении ЦНС у новорождённых детей возникает в результате спастического сокращения на отдельных участках кишечной трубки. Патологические сокращения развиваются на 1-2-й день жизни. После обычного отхождения мекония возникает частая рвота. В рвотных массах появляется примесь жёлчи или кишечного содержимого. Живот не вздут, мягкий. На обзорной рентгенограмме органов брюшной полости определяется незначительно увеличенный газовый пузырь желудка и отдельные скопления газа в кишечных петлях.
Для исключения пороков развития проводится УЗИ и рентгенологическое исследование с контрастной массой. Бариевая смесь у новорождённых противопоказана. Используется перитраст или йодолипол. Контрастное вещество останавливается в определённом участке кишечника или очень медленно продвигается по кишечным петлям. Над местом задержки контрастной массы отсутствует расширение кишечной петли (при врождённой непроходимости они расширены).
Неотложная помощь
Лечение только консервативное. Проводится патогенетическая терапия гипоксически-ишемического поражения ЦНС, включая ликвидацию отёка головного мозга, который клинически характеризуется судорожным синдромом и глубоким коматозным состоянием (ИВЛ в режиме гипервентиляции, антиконвульсанты, лазикс, ноотропил).
Для нормализации функции кишечника:
1) пресакральная (паранефральная) блокада (0,25 % раствор новокаина);
2) при метеоризме и спазмах – ветрогонные и спазмолитические средства:
бебинос (Babynos) внутрь по 3-6-10 капель 3 раза в день; эспумизан (Espumisan) внутрь 1 ч. ложке эмульсии 3-5 раз/сут; 2 % раствор но-шпы по 0,1-0,2 мл внутримышечно; свечи с папаверином по 0,003;
3) микроклизмы (при спастических запорах 25-30 мл кипячёной воды, имеющей температуру 37°С, для усиления перистальтики можно добавить глицерин или растительное масло из расчёта 1 мл на 10 мл воды).
2. При мекониевом илеусе отсутствует отхождение мекония с момента рождения. Мекониевая пробка закупоривает просвет подвздошной кишки с последующим развитием полной низкой кишечной непроходимости. Иногда может быть скудное, однократное отхождение плотного мекония. Появляется вначале редкая рвота, она становится неукротимой с примесью желчи (к концу 1-х и на 2-3 сутки), затем «каловая».
Вздувается живот, перистальтика кишечника усилена, особенно в первые дни. Глубокая пальпация затруднена. Пальпируются шнуровидные уплотнения по ходу кишечника. Возможны осложнения в виде заворота кишечника, перфорации стенки кишки с развитием мекониевого перитонита. Рентгенологически выявляется низкая кишечная непроходимость с растянутыми петлями кишечника, иногда горизонтальные уровни жидкости.
Отличительным признаком мекониевой непроходимости кишечника от атрезии тонкой кишки является наличие на рентгенограмме наряду с резко расширенными кишечными петлями участков кишечных петель обычного диаметра.
Неотложная помощь
1). Введение назогастрального зонда для абдоминальной декомпрессии и профилактики аспирации желудочного содержимого.
2). Неполную кишечную непроходимость можно устранить, разжижая меконий водно-солевыми рентгеноконтрастными или сифонными клизмами (лучше с йодированным высокоосмолярным контрастным веществом – гастрографином, можно с 5% раствором панкреатина). Эффективна внутривенная инфузионная терапия:
10 % раствор глюкозы 10 мл/кг + реополиглюкин 10 мл/кг + 3 % раствор калия хлорида 3-4 мл/кг.
3). С целью растворения пробки с последующим отхождением мекония назначают внутрь 4 % раствор ацетилцистеина (мукомист), разведённый в физиологическом растворе. Возможно использование панкреатина внутрь по 0,5 г каждые 4 ч или других ферментных препаратов (креон, абомин, панзинорм форте, панкурмен, мезим форте и др.).
4). При полной кишечной непроходимости и неэффективности консервативного лечения необходимо срочно госпитализировать в хирургическое отделение для оперативного лечения. Прогноз неблагоприятный, так как регистрируется высокая послеоперационная летальность.
3. Неотложная помощь при паралитическом илеусе (парез кишечника).
А. При гипокалиемии (калий в сыворотке меньше 3,5 ммоль/л) необходимо быстро ликвидировать дефицит калия, для чего используют следующую формулу:
Дефицит К+ (ммоль/л) = (К+ норма – К+ больного) × массу тела в кг × 0,35.
В 1 мл 7,5% раствора калия хлорида содержится 1 ммоль К+. При ургентной ситуации калия хлорид можно ввести в вену в дозе 0,5 ммоль/кг массы тела в течение 1 часа с помощью инфузионного насоса.
Б. При гиперкалиемии, наряду с паралитической кишечной непроходимостью (паралитический илеус), отмечаются слабость, срыгивания, рвоты, гипотензия, аритмии сердца (вплоть до остановки сердца), олигурия (уремия), снижение рефлексов. Причинами гиперкалиемии (уровень калия в сыворотке более 6,5 ммоль/л) могут быть:
1) избыточное ведение препаратов калия (ятрогения);
2) массивная потеря внутриклеточного калия (тяжёлый ацидоз, поздняя перевязка пуповины, внутрисосудистый гемолиз, ДВС-синдром);
3) острая почечная недостаточность, незрелость канальцев;
4) острая надпочечниковая недостаточность (адреногенитальный синдром, кровоизлияния в надпочечники и др., ассоциируется с гипонатриемией).
Лечение гиперкалиемии:
1). Внутривенно 10-20 % раствор глюкозы с инсулином (1ED на 25 мл 20% раствора глюкозы).
2). Для уменьшения токсического влияния избытка калия на миокард одновременно вливают кальция глюконат 10 % раствор 0,5-1 мл/кг.
3). Введение 1 ммоль/кг натрия гидрокарбоната снижает уровень калия в сыворотке крови на 1 ммоль/л.
4). Если отсутствует надпочечниковая недостаточность, назначают фуросемид 1 мг/кг, ограничивают белок в пище.
5). Исключить введение препаратов, которые выводятся почками и могут их повредить.
6). Иногда прибегают к гемодиализу.
7). Лечение надпочечниковой недостаточности при ранней диагностике.
В. Стимуляция моторики кишечника при его парезе
(атонический запор):
1). Прозерин подкожно 0,05% раствор 0,009 мг/кг (антихолинэстеразный эффект) на 1 подкожную или внутримышечную инъекцию 2-3 раза в сутки.
2). Питуитрин (окситоцин+вазопрессин) 0,1 мл внутримышечно (в 1 мл содержится 5 ЕD) – повышает сокращение гладкой мускулатуры кишечника.
3). Калимин (местинон) 0,5% раствор 0,1 мл внутримышечно или внутривенно (антихолинэстеразный эффект).
4). Витамин В1 5 % раствор 0,1 мл/кг внутримышечно 1 раз в сутки.
5). Масляные компрессы на область живота.
6). Гипертонические клизмы с 10 % раствором натрия хлорида или 20-30 % раствором магния сульфата в объеме 25-30 мл при температуре 25-30°С (послабляющий эффект через 20-30 мин).
4. Болезнь Гиршпрунгасопровождается динамической кишечной непроходимостью вследствие аганглиоза сплетений Мейсснера и Ауэрбаха, расположенных в стенке кишечника. В поражённом сегменте кишки отсутствует перистальтика. Рентгенография брюшной полости в горизонтальном и вертикальном положениях позволяют выявить вздутие петель кишечника с множественными уровнями жидкости (как при мекониевой пробке). Также проводится ирригография с перитрастом или 15 % раствором верографина (в возрасте старше 2 нед жизни более достоверные данные). Клизма с контрастным веществом и последующей рентгенографией брюшной полости даёт возможность определить суженный аганглионарный сегмент и расширенный проксимальный сегмент кишки. Затем проводят диагностическую ректальную биопсию. При подтверждении диагноза болезни Гиршпрунга накладывают колостому между ганглиарной и аганглиарной частью кишки и в конце 1 года жизни проводится оперативное лечение.
5. Ущемлённые грыжи.
К кишечной непроходимости, перитониту и смерти могут приводить ущемлённые наружные и внутренние грыжи. Внутренние грыжи связаны с дислокацией органов брюшной полости в грудную через естественные или патологические отверстия в диафрагме или с выпадением кишечных петель в карманы брюшной полости или через дефект в брыжейке.
Наружные грыжи в основном бывают:
- паховыми (в 70 % выявляются на первом году жизни, соотношение мальчиков к девочкам составляет 8-10:1, правосторонние – в 60%, левосторонние – в 20 %);
- пупочные (ущемляются очень редко).
При ущемлении грыж развивается типичная клиническая картина кишечной непроходимости. Дети очень беспокойны, кричат от боли. При пальпации живота выражена болезненность. На обзорных рентгенограммах в вертикальном положении видно перемещение петель кишечника в грудную клетку при диафрагмальной грыже и горизонтальные уровни в брюшной полости. При ущемлении паховых грыж в паховой области пальпируется болезненное выпячивание. Пальцевое исследование прямой кишки у грудных детей позволяет пропальпировать паховое кольцо и иногда выпавшие в него петли кишки. Это исследование помогает дифференцировать грыжу от водянки семенного канатика.
Внутренние ущемлённые грыжи немедленно лечатся хирургическим путём. При ущемлении паховых грыж допускается осторожное их вправление, а если оно не удаётся, то также дети срочно оперируются. Если удалось вправить паховую грыжу, то операцию проводят в ближайшее время, так как часто возникают повторные ущемления с развитием некроза кишки.
При выпадении яичника немедленно проводится хирургическая операция.
Дифференциальная диагностика пороков развития кишечника и тактика лечения представлены в табл. 21.
Таблица 21
Дифференциальная диагностика пороков развития кишечника
у новорождённых и тактика их лечения
(Красовская Т.В., Кобзева Т.Н., 2001)
| Диагностические признаки | Пороки развития кишечника | ||||
| Атрезия duodenum | Синдром Ледда | Атрезия тонкой кишки | Болезнь Гиршпрунга (острая форма) | Мекониевый илеус | |
| Начало болезни | С первых суток жизни | Остро с 3-5 суток жизни | С первых суток жизни | С первых суток жизни | С первых суток жизни |
| Поведение ребёнка | Спокойное, эксикоз | Периодически беспокойство, прогрессирующий эксикоз | Спокойное, нарастание эксикоза | Спокойное, нарастание эксикоза | Спокойное, нарастание эксикоза |
| Характер и время возникновения рвоты | С рождения с зеленью, застойная | С начала заболевания с желчью, рефлекторная | С конца первых суток буро-коричневого цвета, застойная | Со 2 суток с жёлчью, застойная | Необильные срыгивания желудочным содержимым |
| Характер стула | Серые слизистые пробки | Слизь с алой кровью | Серые слизистые пробки | Слизисто-меконеальные пробки, скудные | Серые слизистые пробки |
| Живот | Запавший, мягкий и безболезненный | Запавший, болезненный, напряженный | Вздутый, мягкий, безболезненный | Вздутый, мягкий, безболез-ненный | Значительно вздутый, мягкий, безболезненный |
| Продолжение таблицы21 | |||||
| Рентгенологические данные | Наличие двух уровней жидкости, затемнение в нижних отделах живота | Наличие одного уровня жидкости, затемнение в нижних отделах живота. При контрастном исследовании через 40 мин скудная первичная эвакуация в тощую кишку, расположенную справа | Множественные уровни жидкости в кишечных петлях | Вздутая в виде арки толстая кишка с уровнем жидкости, вздутие тонкой кишки. На ирригограмме – зона сужения и супрастенотического расширения | Вздутые петли кишечника без уровней. Иногда видны петрифицированные меконеальные пробки. При ирригографии – узкая атрофичная толстая кишка на всем протяжении |
| Тактика лечения | Предоперационная подготовка в зависимости от дегидратации. Операция наложения дуодено-еюноанастомоза | Кратковременная подготовка. Операция Ледда | Предоперационная подготовка в зависимости от дегидратации. Операция наложения энтеро-еюноанастомоза | Предоперационная подготовка в зависимости от дегидратации. Операция наложения противоестественного заднего прохода по Микуличу | Предоперационная подготовка в зависимости от дегидратации. Ферментные препараты и ацетилцистеин внутрь. Операция наложения энтеротомы. Промывание просвета кишки ацетилцстеином, ферментотерапия. |
Дифференциальная диагностика синдрома рвоты у новорождённых и детей грудного возраста и тактика лечения представлена в табл. 22.
Таблица 22
Дифференциальная диагностика синдрома рвоты у новорождённых и детей грудного возраста и тактика лечения (Красовская Т.В., Кобзева Т.Н., 2001)
| Симптомы | Пилороспазм | Пилоростеноз | Рефлюкс-эзофагит | Псевдо- пилоростеноз | |||
| Природа заболевания | Гипертонус симпатической нервной системы у новорожденных с перинатальной гипоксией (спазм сфинктеров, атония полых органов, гипосекреция) | Генетически обусловленный порок развития циркулярного мышечного слоя и нервных ганглиев привратника. Частота 1:1000 новорожденных детей | А. Грыжа пищеводного отверстия диафрагмы. Б. Гипертонус парасимпатической нервной системы (атония сфинктеров, повышение тонуса и перистальтики желудка и кишечника, гиперсекреция) | Врожденные нарушения обмена веществ при солетеряющей форме адреногенитального синдрома | |||
| Начало болезни | С первых дней жизни | Чаще со 2-4 недели жизни | С первых дней жизни | Чаще с 3-4 недели жизни | |||
| Продолжение таблицы 22 | |||||||
| Характер рвоты | Аэрофагия, нерегулярные срыгивания во время и после кормления неизмененным молоком | Обильная рвота («фонтаном») кислым створоженным молоком, при декомпенсации прогрессирующая рвота «кофейной гущей» | Рвота, регургитация после кормления, усиливающаяся в горизонтальном положении, возможны буро-коричневые прожилки. Поперхивания и кашель во время сна | Упорная обильная рвота («фонтаном») молоком | |||
| Живот | Умеренно вздут | Вздут в эпигастрии, видна перистальтика желудка в виде «песочных часов» | Обычной формы | Обычной формы | |||
| Стул | Наклонность к запорам | Запоры | Нормальный | Поносы | |||
| Мочеиспускание | Нормальное | Олигурия | Нормальное | Полиурия | |||
| КОС | Норма | Метаболический алкалоз | Норма | Метаболический ацидоз | |||
| Водно-солевой обмен | Норма | Гипохлоремия, гипокалиемия, гипомагниемия | Норма | Гипонатриемия, относительная гиперкалиемия | |||
| УЗИ | Норма | Сужение пилорического канала, утолщение циркулярного мышечного слоя, отсутствие эвакуации содержимого из желудка, расширение полости желудка, расширение полости желудка и утолщение его стенок | Желудок и привратник без патологии | Желудок и привратник без патологии. Увеличение надпочечников | |||
| Эзофагогастро-дуденоскопия | Привратник свободно проходим | Привратник не раскрывается, антрум-гастрит, терминальный геморрагический эзофагит | Фиброзно-язвенный геморрагический эзофагит, халазия кардии. При грыже смещение Z-линии | Без патологии | |||
| Рентгенография | Повышенное, равномерное газонаполнение ЖКТ. Первичная эвакуация контрастной массы из желудка через 40 мин не нарушена | Увеличенный в размерах желудок с большим количеством жидкости натощак, сниженное газонаполнение кишечника. Отсутствие первичной эвакуации контрастной массы через 40 мин, симптом «клюва» на боковой рентгенограмме | Пищевод расширенный, извитой. Гастроэзофагеальный рефлюкс в положении Тренделенбурга. При грыже – кардиальный отдел пищевода перемещен в грудную полость | Без патологии | |||
| Тактика лечения | Консервативное лечение (спазмолитики но-шпа, папаверин внутрь) | Операция пилоромиотомии Рамштедта | Функциональный – консервативно. Грыжа – антирефлюксная операция | Определение полового хроматина, кариотипа, 17-кетостероидов. Консервативное лечение | |||
1.6. ОСТРАЯ ДЫХАТЕЛЬНАЯ НЕДОСТАТОЧНОСТЬ
Принципы лечения дыхательной недостаточности
1. Удаление мокроты после её разжижения:
- носовые ходы промыть изотоническим раствором NaCl (tº 37ºС) или увлажняющим спреем для носа «Салин»;
- слизь отсосать через рот резиновой грушей или электроотсосом (длительность манипуляции не > 30 секунд);
- стимуляция кашля шпателем, интраназальным катетером, введённым на глубину 5-7 см;
- у интубированных больных – катетером через интубационную трубку.
2. Оксигенотерапия40–45 % О2 вдыхаемым через носовой катетер, который вводится на глубину, равную расстоянию от козелка уха до ноздри ребёнка или подача О2 в кувез, кислородную палатку. Насыщение крови О2 (РаО2) должно быть около 100 mmHg. Сохранение гипоксемии указывает на шунтирование крови, при котором более эффективны СДППД (спонтанное дыхание с постоянным положительным давлением при использовании методики Грегори и соавт., 1971) или же аппаратная ВИВЛ (вспомогательная искусственная вентиляция легких), ИВЛ. Уровень сатурации О2 для избежания гипероксии должен быть не > 90-92%. Оксигенотерапия различными методиками представлена в табл. 23.
3. Мониторинггазового состава крови (транскутантная пульсоксиметрия или на газоанализаторе), КОС и адекватная коррекция ацидоза или алкалоза (осложнение гипервентиляции). По показаниям [рН < 7,25 у детей со смешанным ацидозом или с «не-дельта-ацидозом» при анионной разнице < 15 ммоль/л (Na+–Cl-–HCO3-), остановка дыхания > 20 с или остановка сердца после выведения новорождённого из терминального состояния] внутривенно вводится чаще всего 2 % раствор натрия гидрокарбоната (осмолярность 360 мосм/л) или в исключительных случаях 4 % гиперосмолярный раствор (764 мосм/л), содержащий 0,5 ммоль натрия гидрокарбоната. Расчётная доза обычно составляет 1-2 ммоль/кг, которую вводят внутривенно со скоростью 1 ммоль/кг/мин (половину дозы вливают медленно струйно, другую половину – капельно). Введение 2 ммоль/кг натрия гидрокарбоната повышает рН крови на 0,1 ед.
Осложнения длительной гипероксии
при вдыхании высоких концентраций О2
1. Местное повреждающее действие на дыхательные пути и паренхиму лёгких:
- обструктивный синдром;
- ускоренное разрушение сурфактанта;
- утолщение альвеолярно-капиллярной мембраны с затруднением диффузии газов;
- денитрогенация альвеолярного газа с развитием ателектазов и увеличением внутрилёгочного шунтирования кровотока.
2. Спазм периферических сосудов, который приводит:
- к артериальной гипертензии;
- сокращению мозгового кровотока.
3. У недоношенных детей возможна ретролентальная фиброплазия с последующим развитием слепоты.
4. Бронхолёгочная дисплазия у детей с низкой массой тела.
Таблица 23
Параметры при различных методиках оксигенотерапии
| Метод оксигенотерапии | Максимальная концентрация О2 в дыхательных путях | Поток 100% О2 (л/мин) | tº газа (º С) | Влажность газа (%) |
| 1. Ингаляция через воронку | 25-30 | 5-6 | 26-28 | 60-80 |
| 2. Кислородная палатка (тент) | 60-70 | 5-10 | 26-28 | 60-80 |
| 3. Ротоносовая маска | 80-90 | 6-8 | 26-28 | 60-80 |
| 4. Носоглоточный катетер | 1-2 | 32-34 | 70-90 | |
| 5. Кувез | 60-70 | 5-10 | 26-28 | 60-80 |
| 6. Ингаляция через тройник Айра в эндотрахеальную трубку | 6-8 | 37-37,5 | 90-100 |
Примечание. Предельное «безопасное» время для ингаляции 100% О2 в течение 2-3 ч, 80% - 4-5 ч, 60% - 8-12 ч, 45% - > 1 суток.
Параметры КОС:
1) рН – концентрация водородных ионов в капиллярной крови, взятой из пальца (пределы изменения, совместимые с жизнью 7-7,8; < 7,35 – ацидоз, > 7,45 – алкалоз);
2) ВЕ– избыток или дефицит оснований, показывает какое количество ммоль NaHCO3 необходимо добавить (или условно удалить), чтобы рН стало равным 7,38 (при рСО2 – 40 mmHg и tº тела 38ºС); положительное значение указывает на избыток оснований, а отрицательное – на дефицит оснований (или избыток кислот);
3) АВ – истинный гидрокарбонат крови, т.е. содержание НСО3- в крови, взятой у конкретного пациента в данных конкретных обстоятельствах;
4) SB – стандартный гидрокарбонат – тот же HCO3- крови пациента, но приведенный к стандартным условиям, т.е. в среде с рСО2 = 40 mmHg, при содержании HbО2 = 100% и при tº38ºС;
5) ВВ – сумма оснований всех буферных систем крови, т.е. сумма оснований бикарбонатной, фосфатной, белковой и гемоглобиновой буферных систем;
6) РСО2– парциальное давление углекислого газа над жидкостью (в норме РаСО2 = 40 mmHg, смещение величины вправо > 40 mmHg отражает накопление и избыток в крови СО2, т.е. дыхательный ацидоз, а смещение влево < 40 mmHg – недостаточное количество СО2 в крови, т.е. дыхательный алкалоз);
7) 1 mmHg = 0,133 кПа.
Клинико-лабораторные признаки острой дыхательной недостаточности представлены в табл. 24.
Таблица 24
Клинико-лабораторные признаки
острой дыхательной недостаточности (ОДН)
| Признаки ОДН | I степень (компенсация) | II степень (субкомпенсация) | III степень (декомпенсация) |
| 1. Одышка (частота дыхания > 60/мин) | Периодическая, без участия вспомогательной дыхательной мускулатуры в акте дыхания. Отсутствует в покое. | Имеется в покое, посто-янная, дыхательная мускулатура напряже-на, втяжение податли-вых мест грудной клетки на вдохе, дыхание «свистящее» с «кряхтящим» выдохом. | Очень выраженная (ЧД в 1,5 раза больше нормы). Дыхание аритмичное, приступы брадипноэ, периодически парадоксальные типы дыхания. |
| 2. Хрипы в легких | Влажные (мелкопузыр-чатые), крепитация над областью поражения. | Распространённые раз-нокалиберные влажные («влажное лёгкое») | Уменьшение или исчезновение на вдохе. |
| 3. Цианоз (появляется при гипоксемии PaO2 < 70 mmHg и содержании восстановленного Hb >50 г/л) | Периоральный, периодический, более выражен при возбуждении, исчезает при дыхании 40-45% О2, выражена бледность лица. | Периоральный, в области лица и верхних конечностей постоян-ный, не исчезает при дыхании 40-45% О2, но отсутствует при помещении в кислородную палатку; отмечается распространенная бледность кожи, ногте-вых лож, усилена потливость (в области лба, ладоней и стоп). | Распространенный (слизистые оболочки, губы и т.д.), не исчезает после дыхания 100% О2 (при резкой гиперкапнии – ухудшение состояния); бледность и мраморность кожи распространены по телу ребенка, липкий пот. |
| 4. Реакция сердеч-но-сосудистой системы: а) соотношение пульс/дыхание (П/Д) б) артериальное давление в) сердечный ритм | 3,5-2,5 : 1 | 2-1,5 : 1 | Варьирует, т.к. часто брадикардия и брадипноэ. |
| Нормальное или умеренная (компенсаторная) гипертензия. | Повышено | Артериальная гипотензия | |
| Тахикардия | Тахикардия | Аритмия, брадикардия | |
| 5. Газовый состав крови (в норме парци-альное давление в крови: РаО2 от 78,9±3,0 mmHg до 83,5±3,0 mmHg, или (90-100 mmHg); PaCO2 от 32,6±2,3 до 36,8±1,5 mmHg, или в | Не изменен или РО2 умеренно снижено до 90% от нормы (65,4-75,2 mmHg) и при дыхании 40-45% О2 нормализуется. РСО2 снижено (< 30 mmHg) или в норме. | Гипоксемия до 70-85% от нормы (РО2 < 55,1 – 64,1mmHg; РаО2 < 70 mmHg). При преобла-дании диффузионно-распределительных расстройств чаще отме-чается нормокапния. При преобладании | Выраженная гипоксемия (< 70% от нормы), РО2 < 40,1 mmHg. Гиперкапния (РСО2 > 74,4 mmHg) |
| Продолжение таблицы 24 | |||
| среднем 40 mmHg | вентиляционных рас-стройств – гиперкапния (РСО2 > 45,1 mmHg; РаСО2 > 45-60 mmHg), при гипервентиляции – гипокапния РаСО2 < 35 mmHg. | ||
| 6. Кислотно-основ-ное состояние (КОС): а) pH (норма 7,35-7,45; при рождении 7,27, а через 12-14 ч жизни 7,35) | Не изменено Не изменена | Дыхательный или ме-таболический ацидоз, при интестинальном синдроме - алкалоз. Из-менения зависят от сос-тояния гемодинамики. 7,34-7,25 (дыхательный или метаболический ацидоз) | Декомпенсированный смешанный ацидоз (при выраженных диарее и рвоте – алкалоз). < 7,2 |
| б) ВЕ (норма при рождении ~ 10, в возрасте 1-14 суток от –9,2±0,8 до – 1,2± 0,8; в возрасте >2 нед 0±2,3 ммоль/л) | Норма | Увеличен или снижен (компенсирует гиперкапнию) | Увеличен (> 6-8) |
| в) АВ (норма от 16,1±0,8 до 23,0±1,0 ммоль/л) | Норма | Вариабелен, в зависи-мости от характера ацидоза | Снижен |
| г) SB (норма от 17,1 ± 0,6 до 23,5 ± 0,8 ммоль/л) | Норма | Вариабелен, в зависи-мости от характера ацидоза | Снижен |
| д) ВВ (норма от 38,3 ± 1,0 до 47,6 ± 1,5 ммоль/л) | Норма | Вариабелен | Снижен |
При рождении у 80 % здоровых новорождённых детей отмечается транзиторный метаболический ацидоз (рН = 7,27; ВЕ = 10 ммоль/л), у 20 % новорождённых – смешанный метаболически-респираторный ацидоз.
Различают 2 типа метаболического ацидоза:
1. Дельта-ацидоз, при котором повышена (> 15 ммоль/л) анионная разница (Na+ – Cl- – HCO3-), составляющая в норме у новорожденных детей 5-15 ммоль/л, т.е. в среднем 140–105–20=15(ммоль/л).
2. Не-дельта-ацидоз с нормальной анионной разницей (< 15 ммоль/л).
Изменения показателей КОС при метаболическом ацидозе представлены в табл. 25.
Таблица 25
Показатели компенсированного и декомпенсированного
метаболического ацидоза
| Показатель | Компенсированный ацидоз | Декомпенсированный ацидоз |
| 1. рН | 7,35-7,45 | < 7,35 |
| 2. РаСО2 | < 36 mmHg | Норма (40 mmHg = 5,32 кПа) или > 40 mmHg |
| 3. АВ и SB | Снижены, при этом АВ > SB в связи со пониженным РаСО2 | Снижены, при этом АВ = SB |
| 4. ВЕ | С отрицательным знаком | С отрицательным знаком |
Изменения параметров КОС при дыхательном ацидозе и метаболическом алкалозе представлены в табл. 26.
Таблица 26
Показатели дыхательного ацидоза и метаболического алкалоза
| Показатель | Дыхательный ацидоз | Метаболический алкалоз |
| 1. рН | < 7,35 | > 7,4 |
| 2. РаСО2 | > 45 mmHg | Норма, пониженное или повышенное |
| 3. АВ и SB | Повышены | Повышены |
| 4. ВЕ | С положительным знаком | Повышен |
| 5. Электролиты крови | Норма | Гипокалиемия и гипокальциемия |
| 6. рН мочи | Норма, слабокислая | Щелочная (при потери К+ - кислая) |
Примечание. Дыхательный ацидоз компенсируется путем развития метаболического алкалоза, т.к. почки усиленно выводят Н+ (ацидогенез) и реабсорбируют ионы НСО3- (в виде NaHCO3), что приводит к повышению АВ, SB и ВЕ. В конечном итоге к дыхательному ацидозу может присоединиться метаболический алкалоз, что практически встречается редко.
1.7. СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ У НОВОРОЖДЁННЫХ
У новорождённых детей недостаточность кровообращения в основном обусловлена сердечной недостаточностью (СН). Последняя определяется, как нарушение способности сердца поддерживать кровообращение, необходимое для метаболических потребностей организма, которое сопровождается:
1) циркуляторными нарушениями (снижение сердечного выброса, диастолическая перегрузка, снижение артериального давления, централизация кровообращения);
2) нейроэндокринными изменениями (повышение активности симпатико-адреналовой системы, системы ренин-ангиотензин-альдостерон, что ведёт к задержки воды и натрия почками с развитием гиперволемии).
У новорождённых сердечная недостаточность преимущественно левожелудочковая, т.к. мышечная сила левого желудочка меньше правого и перегрузка объёмом и давлением после рождения выше на левые отделы сердца.
Сердце новорождённого ребёнка имеет значительно меньший функциональный резерв по сравнению со старшими детьми, что связано с анатомо-физиологическими особенностями:
1) меньшее количество миофибрилл;
2) актомиозин (белок саркомера) преимущественно состоит из β-изомеров миозина с низкой АТФ-азной активностью (при созревании к 2 месяцам жизни они сменяются α-изомерами с высокой АТФ-азной активностью, которые обеспечивают тонус миокарда);
3) сниженная функция белков ионной помпы (снижена плотность кальциевого насоса на мембране, большая зависимость внутриклеточной концентрации кальция от внеклеточной);
4) отсутствие выраженной зависимости эффекта сокращения от величины остаточного натяжения (преднагрузки при диастолическом наполнении сердца) по закону Старлинга;
5) инотропный эффект миокарда снижен, т.к. его податливость на преднагрузку в 2 раза ниже, чем у старших детей, что обусловлено высоким содержанием стромы, чем сократительных элементов;
6) увеличение частоты сердечных сокращений в ответ на повышение потребления О2, как компенсаторная реакция, ограничено в связи с малыми запасами норадреналина в миокарде и сниженной чувствительностью симпатических рецепторов к связыванию его;
7) уменьшение времени диастолического наполнения сердца при тахикардии ведёт к снижению коронарного кровотока;
8) относительно большой минутный объём сердца (400 мл/кг/мин) по сравнению с взрослыми (100 мл/кг/мин) используется новорождёнными неэффективно (в 2 раза ниже, чем у взрослых, т.к. на утилизацию 1 мл/кг/мин О2 новорождённому требуется 52 мл крови, а взрослому – 24 мл).
Причины сердечной недостаточности (табл. 27):
1. Врождённые пороки сердца (известны > 90 видов ВПС и их комбинаций) и транзиторные нарушения кровообращения (персистирующее фетальное кровообращение или персистирующая лёгочная гипертензия новорождённых, широкий открытый артериальный проток) сопровождаются большой преднагрузкой(степень растяжения кардиомиоцитов перед систолой) и постнагрузкой(сила сокращений миокарда, необходимая для преодоления общего периферического сосудистого сопротивления), а также перегрузкой давлением и объёмом.
2. Снижение сократительной способности миокарда при кардиомиопатии, миокардитах, перикардитах, метаболических нарушениях (ацидоз, гипогликемия, гипокальциемия, гипокалиемия и др.), тяжёлой анемии, полицитемии.
3. Аритмии сердца (тахи- и брадиаритмии).
Патогенез сердечной недостаточности представлен на рис. 9.
Таблица 27
Причины сердечной недостаточности (СН) у новорождённых
| Сроки манифестации СН | Причины СН |
| 1-й день жизни 2-3 сутки жизни 4-7 сутки жизни 8-30 сутки жизни | 1. Врождённый миокардит 2. Недостаточность атриовентрикулярных клапанов 3. Атрезия аорты 4. Гипоплазия левого желудочка 1. Ишемия миокарда (постасфиксическая транзиторная) 2. Кардиомиопатия у детей с диабетической фетопатией 3. Метаболические расстройства (гипогликемия, гипокальциемия, гипокалиемия, ацидоз и др.) 4. Аритмии сердца 5. Тяжёлая анемия (снижение Hb < 70 г/л) 1. Персистирующие фетальные коммуникации 2. Транспозиция крупных сосудов 3. Артериовенозные свищи 1. Врождённые пороки сердца с нарушением выхода из левого желудочка или с перегрузкой объёмом: - коарктация аорты; - стеноз аорты; - транспозиция магистральных сосудов с большим ДМЖП |
Врождённые пороки сердца у новорождённых детей
Частота врождённых пороков сердца (ВПС) среди новорождённых составляет 0,8–1 %. По статистическим данным в России ежегодно рождается 40-45000 детей с ВПС. Среди них отмечается высокая естественная смертность: в первую неделю жизни – 14-22 %, в течение 1-го месяца – 19-27 %, не доживают до 1 года – 30-80 %. Поэтому в кардиохирургии интенсивно разрабатывается проблема неотложной хирургии новорождённых и грудных детей с ВПС. Разработаны методы лечения для всех ВПС, включая пересадку сердца или комплекса сердце-лёгкие.
Большинство фатальных исходов от ВПС (в среднем 79 %) приходится на 1-й год жизни (табл. 28), из них более половины – на период новорождённости и первых 3 мес. жизни. Неоперабельными ВПС (12-25 %) являются СГЛС, сложные ВПС с гетеротаксией внутренних органов и с одновременной кардиомиопатией, эндокардиальным фиброэластозом. Тяжесть состояния больных с ВПС усугубляется наличием других факторов риска (аномалии развития, не поддающиеся лечению; недоношенность с массой тела менее 2000 г), которые увеличивают естественную смертность на 20-50 %.
Первичная диагностика ВПС
1. Точный диагноз ВПС не может быть поставлен без эхокардиографии (ЭхоКГ), катетеризации полостей сердца и ангиокардиографии (АКГ). На первом этапе основной задачей неонатологов и участковых педиатров является только своевременное выявление ВПС и направление пациентов на консультацию к кардиохирургам, а не к кардиоревматологам, чтобы исключить задержку перевода ребёнка в специализированный центр.
Выявляемость ВПС отстаёт от ожидаемого уровня по статистическим данным на 40-80 %. В последние годы разрабатываются методики ультразвукового сканирования плода, которые позволяют выявить ряд ВПС ещё внутриутробно и своевременно, при необходимости, прервать беременность.
2. Предположить ВПС можно уже на основании простых методов обследования – осмотра, пальпации, аускультации и определения артериального давления на верхних и нижних конечностях. Наиболее важными признаками ВПС являются цианоз, застойная сердечная недостаточность, расстройства дыхания, беспокойство, летаргия ребёнка.
Цианоз слизистых оболочек является частым симптомом ВПС. В первые часы жизни он может быть связан и с асфиксией, СДР, массивным ателектазом лёгких, метаболическими нарушениями. Во всех случаях наличие артериальной гипоксемии (РаО2 менее 75 мм рт.ст.) должно иметь объяснения и требует соответствующего лечения.


 I этап
I этап
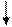 |




 |

 II этап
II этап
 | |||
 |

 III этап
III этап



Рис. 9. Патогенез сердечной недостаточности у новорождённых
(Шабалов Н.П. с соавт., 1996).
Таблица 28
Группировка врождённых пороков сердца у новорождённых
и грудных детей в зависимости от тяжести порока и прогноза
| Естественная смертность на 1-м году жизни | |||
| I группа | II группа | III группа | IV группа |
| 8-11 % (благоприятный прогноз) | 24-36 % | 36-52 % | 73-97 % |
| 1. ОАП 2. ДМЖП 3. ДМПП 4. СЛА | 1. Тетрада Фалло 2. Болезни миокарда | 1. ТМС 2. КА 3. СА 4. ТА 5. ТАДЛВ 6. ЕЖ 7. ДОМС 8. ОАВК | 1. СГЛС 2. АЛА+ИМЖП 3. ОАС |
Примечание. ОАП – открытый артериальный проток, ДМЖП – дефект межжелудочковой перегородки, ДМПП – дефект межпредсердной перегородки, СЛА – стеноз легочной артерии, ТМС – транспозиция магистральных сосудов, КА – коарктация аорты, СА – стеноз аорты, ТА – трикуспидальная атрезия, ТАДЛВ – тотальный аномальный дренаж легочных вен, ЕЖ – единственный желудочек, ДОМС – двойное отхождение магистральных сосудов от правого желудочка, ОАВК – открытый атрио-вентрикулярный канал, СГЛС – синдром гипоплазии левого сердца, АЛА+ИМЖП – атрезия легочной артерии с интактной межжелудочковой перегородкой, ОАС – общий артериальный ствол.
3. В первую очередь необходимо провести дифференциальный диагноз ВПС с лёгочными заболеваниями. Последние можно предположить:
- у детей от матерей с осложнённым течением беременности и родов;
- у недоношенных;
- при асфиксии в родах;
- при появлении цианоза через несколько часов после родов.
Важно провести рентгенографию грудной клетки, позволяющей исключить пневмоторакс, диафрагмальную грыжу, СДР. При ВПС на рентгенограмме отмечается кардиомегалия и признаки отека легких.
Повышение уровня РаСО2 чаще встречается при нарушении вентиляции, чем при цианозе кардиального генеза.
4. Ценными являются тесты с дыханием 100 % кислородом (гипероксидная проба) и с повышенным давлением в дыхательных путях (ПДКВ). При дыхании в течение 10-15 мин чистым кислородом у новорождённых с сердечным цианозом (ВПС с обеднением малого круга, выраженный право-левый шунт кровотока или леёгочная гипертензия) РаО2 возрастает не более чем на 10 мм Hg и цианоз сохраняется (отрицательная проба). При лёгочных заболеваниях (СДР, РДС II типа, пневмония), а так же при ВПС с обогащением малого круга и кардиомиопатиях РаО2 может достигать до 150 мм Hg (положительная проба, цианоз исчезает). Эффект от ПДКВ (8-10 см вод.ст.) наблюдается при выраженных вентиляционно-перфузионных нарушениях (аспирация мекония, болезнь гиалиновых мембран). При ВПС с перегрузкой малого круга такой эффект тоже происходит, а при ВПС с внутрисердечными шунтами оксигенация ухудшается (цианоз усиливается) при проведении ПДКВ.
5. Сердечная недостаточность проявляется в виде застойных явлений в большом или малом кругах кровообращения и в нарушениях деятельности сердца. Гиперволемию в лёгких можно предположить на основании одышки, затрудняющей кормление ребёнка. Влажные хрипы в лёгких характерны для выраженной левожелудочковой недостаточности.
Застойные явления по большому кругу кровообращения клинически проявляются увеличением печени более 3 см из подреберья по срединноключичной линии, олигурии (диурез < 0,5 мл/кг/ч), расширении вен на шее, появлении отеёков вокруг глаз или в сакральной области.
Частыми признаками нарушения функции миокарда являются тахикардия, кардиомегалия, ритм галопа, снижение артериальной пульсации на руках. Шумы над областью сердца при ВПС могут быть на первых неделях жизни лишь в 10 % случаев. Значительно чаще кардиальные шумы в первые 2 суток жизни отражают постнатальную перестройку кровообращения. Со 2-3 суток шумы выслушиваются при кардиомиопатиях и расстройствах транзиторного кровообращения. Шумы при дефектах кардиальных перегородок увеличивают свою интенсивность к 4-5 суткам жизни после ликвидации лёгочной гипертензии. Сердечный шум продолжающийся после 3 суток вероятнее всего связан с ВПС, особенно при наличии признаков сердечной недостаточности.
Однако, если сердечный шум отсутствует, но у ребёнка имеются клинические признаки ВПС, то в такой ситуации прогноз чаще неблагоприятный. Функциональные («физиологические») сердечные шумы всегда систолические и с небольшой интенсивностью.
6. При патологической неврологической симптоматике следует иметь в виду не только гипоксически-ишемическую энцефалопатию, внутричерепную патологию, гипогликемию, внутриутробные инфекции, сепсис, но и метаболический ацидоз из-за гипоксемии сердечного генеза.
7. Важным является определение особенностей пульса и артериального давления на конечностях. При СГЛС артериальная пульсация ослаблена как на руках, так и на ногах. Для коарктации аорты и перерыва дуги аорты патогномоничным является ослабление пульса и снижение артериального давления (АД) на нижних конечностях по сравнению с верхними (при отсутствии коарктации аорты АД на ногах больше чем на руках только на 10 мм рт. ст.). Однако надо помнить, что у новорожденных имеется физиологическое сужение перешейка аорты, которое может давать градиент систолического давления между верхними и нижними конечностями до 30 мм рт.ст., поэтому целесообразно многократное измерение артериального давления. При аномально отходящей подключичной артерии от нисходящей аорты можно выявить снижение пульсации и артериального давления на соответствующей руке по сравнению с противоположной.
8. На ЭКГ выявляют признаки перегрузки и гипертрофии желудочков сердца, аритмии и др. ЭхоКГ даёт возможность уточнить топические признаки ВПС, характер и величину шунтирования кровотока.
Классификация ВПС по патофизиологическому принципу представлена в табл. 29.
Таблица 29
Классификация врождённых пороков сердца
(по патофизиологическому принципу)
| Нарушения гемодинамики | Без цианоза (артерио-венозный шунт) | С цианозом (венозно-артериальный шунт) |
| С обогащением малого круга | Открытый артериальный проток, дефекты межпредсердной и межжелудочковой перегородок, атриовентрикулярная коммуникация, дефект аорто-лёгочной перегородки, аномальный дренаж легочных вен | Комплекс Эйзенменгера, транспозиция магистральных сосудов, общий артериальный ствол |
| С обеднением малого круга | Изолированный стеноз легочной артерии | Болезнь Фалло, атрезия трехстворчатого клапана, транспозиция магистральных сосудов со стенозом лёгочной артерии, общий ложный артериальный ствол, болезнь Эбштейна |
| С препятствием выбросу крови из желудочков | Изолированный стеноз лёгочной артерии, изолированный аортальный стеноз, коарктация аорты | |
| Без нарушений гемодинамики | Истинная и ложная декстракардия, аномалии положения дуги аорты и ее ветвей, небольшой дефект межжелудочковой перегородки (в мышечной части) |
Интенсивная терапия сердечной недостаточности
у новорождённых детей
I. Уменьшение преднагрузки сердца:
1. Ограничение жидкости до 80 % от возрастной нормы.
2.Назначение в экстренных случаях салуретика фуросемида (лазикса) внутривенно или внутрь 1-3 мг/кг/сут (максимум действия через 1-2 часа). При длительном лечении СН и при артериальной гипертензии применяют гипотиазид 1-3 мг/кг/сут в 2 приёма (максимум эффекта через 2-8 ч), калийсберегающие диуретики – верошпирон внутрь 3 мг/кг/сут (пик эффекта на 2-3 сутки).
II. При отсутствии эффектаот вышеперечисленных мероприятий:
1. Ограничение физической нагрузки в виде перевода на зондовое кормление. Поддержание нормальной температуры тела младенца в кувезе.
2. Оксигенотерапияпод положительным давлением (FiO2 не > 0,5). Коррекция гипогликемии, метаболического ацидоза (при рН < 7,25 с помощью натрия гидрокарбоната). Ликвидация дыхательных нарушений путём удаления слизи из дыхательных путей, интубации трахеи и вспомогательной ИВЛ увлажнённой и подогретой газовой смесью.
3. Улучшение производительности сердца:
А). Назначение дигоксина (табл. 30) при ВПС с лево-правым шунтированием кровотока, миокардитах или дилятационных кардиомиопатиях в течение нескольких месяцев или лет. Дигоксин не назначают при СН с наличием брадикардии, синдрома WPW и синдрома малого сердечного выброса (гипертрофическая кардиомиопатия). Внутривенно вводится доза насыщения 0,03 мг/кг для недоношенных и 0,04 мг/кг для доношенных (в три приёма через 6-8 ч, вначале ½ общей дозы, а затем 2 приёма по ¼ дозы). Поддерживающая доза составляет 1/8 дозы насыщения с интервалом каждые 12 ч. Чем младше ребёнок, тем быстрее проявляются токсические эффекты сердечных гликозидов, особенно на фоне гипоксии, ацидоза, гипокалиемии и при одновременном назначении с индометацином (с целью медикаментозного закрытия ОАП) и амиодароном (снижается канальцевая секреция дигоксина).
Таблица 30
Применение дигоксина при СН у новорождённых детей
| Масса тела при рождении | Доза насыщения (мкг/кг) 1-е введение и дважды с интервалом в 6 ч | Поддерживающая доза (мкг/кг) |
| Недоношенные дети | ||
| Менее 1500 г | А. В вену: 10 – 5 – 5.
Б. Внутрь: 12,5 – 6,25 – ©2015 arhivinfo.ru Все права принадлежат авторам размещенных материалов.
|